
已知X、Y是原子核电荷数不大于18的元素。若X、Y两元素化合物组成是YX3,已知X原子的最外层电子数为a+2,次外层电子数为a+3;Y原子的最外层电子数为b-3,次外层电子数为b。则a和b的值分别是( )
A、3,2 B、2,3 C、5,6 D、5,8
科目:高中化学 来源: 题型:
已知反应:①101 时,
时,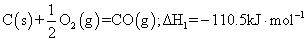
②稀溶液中: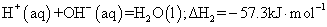
下列说中正确的是
A、若碳的燃烧热用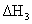 表示,则B、若碳的燃烧热用
表示,则B、若碳的燃烧热用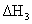 表示,则
表示,则
C、浓硫酸与稀 溶液反应的中和热值为57.3kJ·mol-1
溶液反应的中和热值为57.3kJ·mol-1
D、稀醋酸与稀 溶液反应生成1mol水,放出57.3kJ的热量
溶液反应生成1mol水,放出57.3kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分类,完全正确的是
| A | B | C | D | |
| 强电解质 | H2SO4 | NaCl | HClO | HNO3 |
| 弱电解质 | HF | NH3 | CaCO3 | H2CO3 |
| 非电解质 | Cl2 | CH3COOH | C2H5OH | SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一洁净锥形瓶中,先用酸式滴定管准确移取25.00mL某未知浓度的盐酸于其中,再用0.20mol·L-1的NaOH溶液(指示剂为酚酞)进行滴定。滴定结果如下:
| 滴定次数 | NaOH起始读数 | NaOH终点读数 |
| 第一次 | 0.10 mL | 18.60 mL |
| 第二次 | 0.30 mL | 18.00 mL |
(1)根据以上表格中数据可以计算出盐酸的物质的量浓度为 mol·L-1
(2)达到滴定终点的标志是
(3)以下操作造成测定结果偏高的原因可能是 。
A.未用标准液润洗碱式滴定管
B.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
C.配制标准溶液的氢氧化钠中混有Na2CO3杂质
D.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
E.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素A、B、C、D,原子序数依次增大;A、C的原子序数的差为8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。下列叙述正确的是( )
A、原子半径:A<B<C<D B、非金属性:A>C
C、最高价氧化物对应水化物的酸性:D<C D、单质B在常温下能溶于浓硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
常温常压下,可能含有N2、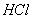 、CO、CO2的混合气体,依次通过足量的碳酸氢钠溶液和灼热的氧化铜,恢复到原来的温度和压强,气体体积没有变化;再通过足量的氧化钠,气 体积减少,最后通过灼热的铜网,恢复到原来的温度压强,体积又减少,并有剩余气体,若上述各步反应均完全,则对混合成分的判断正确的是( )
、CO、CO2的混合气体,依次通过足量的碳酸氢钠溶液和灼热的氧化铜,恢复到原来的温度和压强,气体体积没有变化;再通过足量的氧化钠,气 体积减少,最后通过灼热的铜网,恢复到原来的温度压强,体积又减少,并有剩余气体,若上述各步反应均完全,则对混合成分的判断正确的是( )
A、一定有N2和CO2,可能有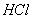 和CO
和CO
B、一定有N2,且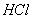 、CO、CO2中至少含有一种
、CO、CO2中至少含有一种
C、一定有N2、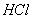 、CO、CO2
、CO、CO2
D、一定有N2、CO、CO2,一定没有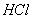
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2CO(g)+O2(g)=2CO2(g) ΔH= -566 kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+ 1/2O2(g) ΔH= -226 kJ/mol
根据以上热化学方程式判断,下列说法正确的是
A.CO的燃烧热ΔH= -566 kJ/mol B.CO的热值约为10.1kJ/g
C.2Na2O2(s) + 2CO2(s)= 2Na2CO3(s) + O2(g) ΔH< -452 kJ/mol
D.CO(g)与Na2O2(s)反应放出50.9 kJ热量时,电子转移为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
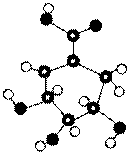
三种元素,其分子结构如图所示。请回答下列问题:
(1)M的结构简式是 。[来源:学科网ZXXK]
(2)下列关于M的说法,正确的是 。
A.遇FeCl3溶液呈紫色 B. 遇紫色石蕊试液变红
C.遇溴水发生取代反应 D. 能缩聚为高分子化合物
 (3)M在一定条件下发生消去反应,生成 ,该反应的化学方程
(3)M在一定条件下发生消去反应,生成 ,该反应的化学方程
式是 。
(4)M与有机物A在一定条件下可生成一种相对分子质量为202的酯类物质。A可能的
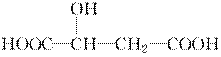 结构简式 。
结构简式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com