
科目:高中化学 来源:2015-2016学年河北省高二上学期10月月考化学试卷(解析版) 题型:选择题
根据反应:S2O32﹣+2H+═SO2+S↓+H2O,下表各组实验最快出现浑浊的是
Na2S2O3溶液 | 稀H2SO4 | H2O | 温度/℃ | |||
c(mol·L﹣1) | V(mL) | c(mol·L﹣1) | V(mL) | V(mL) | ||
A | 0.1 | 5 | 0.1 | 5 | 5 | 10 |
B | 0.2 | 5 | 0.1 | 5 | 10 | 10 |
C | 0.1 | 5 | 0.1 | 5 | 10 | 30 |
D | 0.2 | 5 | 0.1 | 5 | 10 | 30 |
查看答案和解析>>
科目:高中化学 来源:2016届浙江省温州市高三上学期返校联考化学试卷(解析版) 题型:选择题
下列化学用语中,正确的是
A.乙炔的结构简式 CHCH
B.乙醇的比例模型
C.NaCl的电子式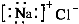
D.S原子结构示意图 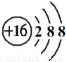
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高一上学期第二次诊断性测试化学试卷(解析版) 题型:填空题
铁是应用最广泛的金属,铁的卤化物也是一种重要化合物。
(1)在实验室中,FeCl2可用铁粉和___________反应制取,FeCl3可用铁粉和___________反应制取。现有含FeCl2和FeCl3的混合物样品,测得n(Fe):n(Cl)=1:2.4,则该样品中FeCl3的物质的量分数为________________。
(2)FeCl2易被氧化,检验一瓶FeCl2溶液是否被氧化的方法(写出操作步骤、现象及结论)是______________。向FeCl2溶液中加入NaOH溶液,开始时生成白色沉淀,后马上变成灰绿色,最终变成红褐色,沉淀变色发生反应的化学方程式为_________________。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省枣阳市高三上学期第一次月考化学试卷(解析版) 题型:填空题
【化学——选修2:化学与技术】(15分)丙酮和苯酚都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚和丙酮,其反应和工艺流程示意图如下:
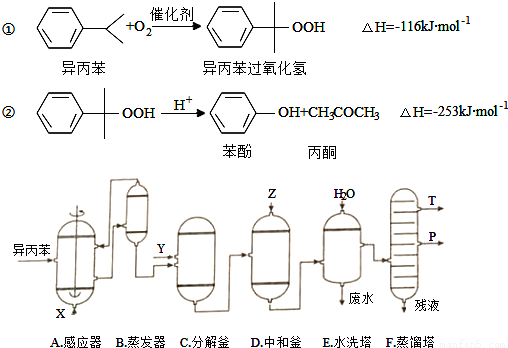
相关化合物的物理常数
物质 | 相对分子质量 | 密度(g/cm﹣3) | 沸点/℃ |
苯酚 | 94 | 1.0722 | 182 |
丙酮 | 58 | 0.7898 | 56.5 |
异丙苯 | 120 | 0.8640 | 153 |
回答下列问题:
(1)反应①和②分别在装置 和 中进行(填装置符号).
(2)反应②为 (填“放热”或“吸热”)反应.反应温度控制在50﹣60℃,温度过高的安全隐患是 .
(3)在反应器A中通入的X是 .
(4)在分解釜C中加入的Y为少量浓硫酸,其作用是 ,优点是用量少,缺点是 .
(5)中和釜D中加入的Z最适宜的是 (填编号.已知苯酚是一种弱酸)
a.NaOH b.CaCO3 c.NaHCO3 d.CaO
(6)蒸馏塔F中的馏出物T和P分别为 和 ,判断的依据是 .
(7)用该方法合成苯酚和丙酮的优点是 .
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期第二次月考化学试卷(解析版) 题型:计算题
(8分)工业合成氨的反应为N2(g)+3H2(g) 2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为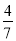 计算:
计算:
(1)该条件下N2的平衡转化率;(小数点后保留一位)
(2)该条件下反应2NH3(g) N2(g)+3H2(g)的平衡常数。(不带单位)
N2(g)+3H2(g)的平衡常数。(不带单位)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期第二次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)能自发进行,则△H<0
B.铁片镀锌时,铁片与外电源的正极相连
C.以熔融Al2O3为电解质进行电解冶炼铝,熔融体中Al3+向阳极移动
D.t℃时,恒容密闭容器中反应:NO2(g)+SO2(g)?NO(g)+SO3(g),通入少量O2, 的值及SO2转化率不变
的值及SO2转化率不变
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高一上第一次联考化学试卷(解析版) 题型:实验题
(11分)下图是我校实验室化学试剂浓硫酸标签上的部分内容。现需要480 mL 1 mol·L-1的稀硫酸。用该浓硫酸和蒸馏水配制,可供选用的仪器有:① 胶头滴管;②玻璃棒;③烧杯;④量筒。

请回答下列问题:
(1)配制稀硫酸时,还缺少的仪器有______________(写仪器名称)。
(2)该硫酸的物质的量浓度为 mol/L;所需浓硫酸的体积 约为___________mL;若将该浓硫酸与等体积的水混合,所得溶液中溶质的质量分数____________49%(填“>” 、“<” 或“=”)。
(3)定容时,若加入的水超过刻度线,必须采取的措施是
(4)下列操作对H2SO4的物质的量浓度有什么影响(偏高、偏低或无影响)?
①转移溶液后,未洗涤烧杯: ;
②容量瓶用水洗净后未烘干: ;
③定容时俯视容量瓶的刻度线: 。
(5)在配置过程中,下列操作不正确的是(填序号) 。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.将准确量取的18.4mol·L-1的硫酸,注入已盛有100mL水的500mL的容量瓶中,加水至刻度线.
D.将硫酸溶于水后需冷却至室温再转移到容量瓶中
E.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手掌托住瓶底,把容量瓶倒转摇匀
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
可逆反应①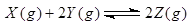 、②
、②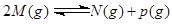 分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
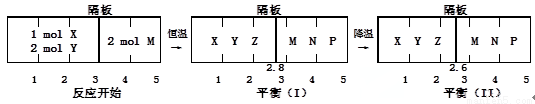
下列判断正确的是:
A.反应①的正反应是吸热反应
B.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15
C.达平衡(I)时X的转化率为5/11
D.在平衡(I)和平衡(II)中的M的体积分数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com