

| 试剂 | KOH | NaOH | Ca(OH)2 |
| 价格(元/吨) | 6800 | 3200 | 1200 |

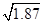 ×10-6mol/L(2分,回答1.36×10-6mol/L也可);Ca(OH)2(1分);以海边的贝壳高温分解制生石灰,生石灰与水反应制得石灰乳(2分)
×10-6mol/L(2分,回答1.36×10-6mol/L也可);Ca(OH)2(1分);以海边的贝壳高温分解制生石灰,生石灰与水反应制得石灰乳(2分)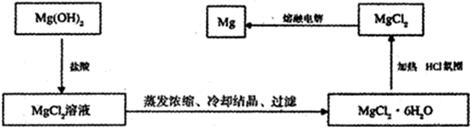 (2分)
(2分)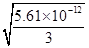 =
=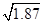 ×10-6mol/L;从经济效益和来源来看,最合理的沉淀剂应该是氢氧化钙。产生氢氧化钙的方法是以海边的贝壳高温分解制生石灰,生石灰与水反应制得石灰乳。
×10-6mol/L;从经济效益和来源来看,最合理的沉淀剂应该是氢氧化钙。产生氢氧化钙的方法是以海边的贝壳高温分解制生石灰,生石灰与水反应制得石灰乳。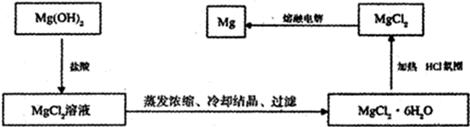 。
。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| 选项 | 物质 | 加入试剂 | 方法 |
| A. | 甲苯(苯酚) | 浓溴水 | 过滤 |
| B. | 溴乙烷(溴单质) | 热氢氧化钠溶液 | 分液 |
| C. | 乙酸乙酯(乙酸) | 饱和碳酸钠 | 过滤 |
| D. | NaOH(s)(少量NaCl) | 水 | 重结晶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.②③ | C.①③④ | D.①②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
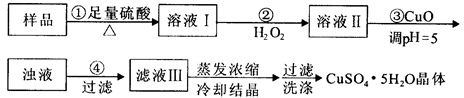
| A.利用CuCO3替代CuO也可调节溶液的pH,不影响实验结果 |
| B.步骤②中发生的主要反应为:H2O2+Fe2++2H+=Fe3++2H2O |
| C.洗涤晶体:向滤出晶体的漏斗中加少量水至浸没晶体,待自然流下后,重复2~3次 |
| D.配制240 mL1mol/L的CuSO4溶液,需称量CuSO4·5H2O的质量为62.5g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
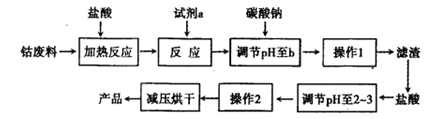
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用无水硫酸铜检验乙醇中是否含水 |
| B.用溴水检验汽油中是否含有不饱和脂肪烃 |
| C.用蒸馏的方法可以分离醋酸与乙醇的混合物 |
| D.检验某卤代烃中是否含溴:加入NaOH溶液,加热,冷却,再加入硝酸银溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 试管序号 | 1 | 2 | 3 | 4 | 5 |
| 通入CO2时间/min | 0 | 1 | 5 | | |
| 滴加盐酸/滴 | 0 | | | 3 | 6 |
| 溶液中颜色对比 | 无色 | 浅黄色→黄色(依次加深) | |||
| 滴加淀粉溶液后的颜色对比 | 无色 | 浅蓝色→蓝色(依次加深) | |||
| 实验步骤 | 预期现象和结论 |
| ①取一份纯净的KI固体,分成两等份; | |
| ②一份加入到装有 的集气瓶A中; 一份加入到装有 的集气瓶A中; ③几天后观察。 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.从碘水中提取单质碘时,不能用无水乙醇代替CCl4 |
| B.可用新制的Cu(OH)2悬浊液检验牙膏中存在的甘油 |
| C.纸层析实验中,须将滤纸上的试样点浸入展开剂中 |
| D.实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.C2H6中混有的C2H4,可以将混合气体先通过溴水,然后用碱石灰干燥 |
| B.CaCO3中混有的少量NaHCO3,可以用加热的方法除去 |
| C.乙烯中混有的SO2气体,可以通过酸性高锰酸钾溶液除去 |
| D.H2S中混有的水蒸气,可以用浓硫酸除去 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com