
| A.HCO3- | B.SO42- | C.SO32- | D.OH- |
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定含CO32- |
| B.加入KSCN溶液,无明显现象,再滴加几滴新制氯水,溶液变为血红色,则试样中一定含Fe2+ |
| C.加入BaCl2溶液,产生白色沉淀,再加入过量的稀盐酸酸化,沉淀不溶解,则试样中一定含SO42- |
| D.在酒精灯火焰上灼烧,火焰为黄色,则试样中一定含钠元素,一定不含钾元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
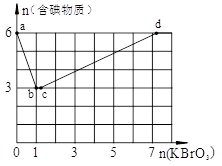
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有⑥ | B.④⑥ | C.③④⑥ | D.①②⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 Cu (HDZ)2+2H+,再加入CCl4、Cu (HDZ)2就很容易被萃取到CCl4中。
Cu (HDZ)2+2H+,再加入CCl4、Cu (HDZ)2就很容易被萃取到CCl4中。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
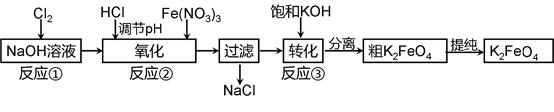
 4Fe(OH)3↓+8OH—+3O2↑,则K2FeO4可以在水处理中的作用是 。
4Fe(OH)3↓+8OH—+3O2↑,则K2FeO4可以在水处理中的作用是 。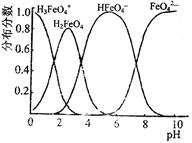
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.NaHSO4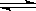 Na++H++SO42一 Na++H++SO42一 | B.NaHCO3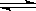 Na++ HCO3一 Na++ HCO3一 |
C.H2S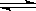 2H++S2- 2H++S2- | D.Mg(OH)2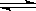 Mg2++2OH- Mg2++2OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,则原溶液中一定有SO42- |
| B.通入Cl2后,溶液变为黄色,加入淀粉后溶液变蓝,则原溶液中一定有I- |
| C.加入碳酸钠溶液有白色沉淀生成,再加盐酸,沉淀消失,则原溶液中一定有Ba2+- |
| D.加入NaOH溶液并加热,产生使湿润的蓝色石蕊试纸变红的气体,则原溶液一定有NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com