
【题目】下列叙述正确的是( )
A.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、AlO2-、SO42-
B.往等c(H+)和等体积的盐酸和醋酸中,分别加足量相同的锌片,相同状况下,与醋酸反应产生的气体体积更大
C.已知H2CO3 的 Ka1= 4.30×10-7,Ka2= 5.61×10-11,HClO的 Ka = 3.0×10-8,则反应CO2+H2O+2NaClO=Na2CO3+2HClO能够成立
D.等c(H+)的盐酸和醋酸,加水稀释100倍后,c(H+)前者大于后者
【答案】B
【解析】
A. 水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液为酸性或者碱性溶液,偏铝酸根离子能够与氢离子反应;
B. 醋酸是弱酸,所以当c(H+)相同时,醋酸物质的量浓度大,含溶质物质的量多,所以反应放出的氢气多;
C. 已知H2CO3 的Ka1= 4.30×10-7,Ka2= 5.61×10-11,HClO的Ka = 3.0×10-8,所以酸性:H2CO3>HClO>HCO3-,这个反应只能生成碳酸氢钠,不能生成碳酸钠,因为次氯酸的酸性介于碳酸和碳酸氢根离子之间,故C错误;
D. 相同c(H+)的盐酸、醋酸均稀释100倍后,盐酸中氢离子浓度都变为原先的![]() ,而醋酸为弱酸,稀释后醋酸的电离程度增大,醋酸中氢离子浓度大于原先溶液中氢离子浓度的
,而醋酸为弱酸,稀释后醋酸的电离程度增大,醋酸中氢离子浓度大于原先溶液中氢离子浓度的![]() ,所以稀释后溶液中c(H+)由大到小的顺序是:醋酸>盐酸,故D错误;
,所以稀释后溶液中c(H+)由大到小的顺序是:醋酸>盐酸,故D错误;
正确答案是B。


 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源: 题型:
【题目】某无色溶液X,由![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的若干种离子组成,取溶液进行如图连续实验
中的若干种离子组成,取溶液进行如图连续实验![]()

A.气体A是![]() ,白色沉淀甲是氢氧化铝
,白色沉淀甲是氢氧化铝
B.溶液中一定不含![]() 、
、![]() 、
、![]()
C.溶液Ⅱ是硫酸钠、碳酸氢铵、氯化钠的混合物
D.溶液中一定存在的离子有![]() 、
、![]() 、
、![]() 和
和![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是( )
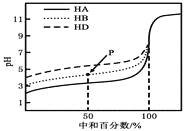
A. 三种酸的电离常数关系:KHA>KHB>KHD
B. 滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C. pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D. 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2RO3是一种二元酸,常温下用1L1mol·L-1Na2RO3溶液吸收RO2气体,溶液的pH随RO2气体的物质的量的变化如图所示。下列说法正确的是

A.a点溶液中2c(Na+)=3c(RO32-)
B.向b点溶液中加水可使溶液的pH由6.2升高到7.4
C.常温下,NaHRO3溶液中c(HRO3-)>c(RO32-)>c(H2RO3)
D.当吸收RO2的溶液呈中性时,c(Na+)=c(RO32-)+c(HRO3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 C(s)+H2O(g)![]() CO(g)+H2(g)在一个可变容积的密闭容器中进行,下列条件的改变 对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一个可变容积的密闭容器中进行,下列条件的改变 对其反应速率几乎无影响的是( )
①增加碳的量且表面积保持不变 ②加热③保持体积不变,充入 He,使体系压强增大 ④保持压强不变,充入 He,使容器体积变大
A.②④B.②③C.①④D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度、容积相同的3个密闭容器中,按不同方式投入反应,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g) + 3H2(g)![]() 2NH3(g) △H=-92.4kJ/mol):
2NH3(g) △H=-92.4kJ/mol):
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1molN2、3molH2 | 2molNH3 | 1molNH3 |
NH3的浓度(mol/L) | c1 | c2 | c3 |
反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
体系压强 | P1 | P2 | P3 |
反应物转化率 | α1 | α2 | α3 |
下列说法不正确的是( )
A.![]() >c3B.a + b=92.4C.P2>2P3D.α1 +α3>1
>c3B.a + b=92.4C.P2>2P3D.α1 +α3>1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的说法正确的是( )
A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式(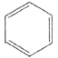 )看,78g苯中含有碳碳双键数为3NA
)看,78g苯中含有碳碳双键数为3NA
C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的化学键完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“五水共治”是浙江治水的成功典范,其中含氮废水处理是污水治理的一个重要课题,图3是高含氰![]() 废水处理方案:
废水处理方案:
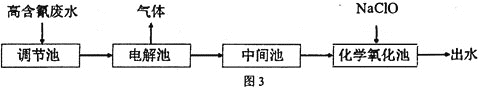
![]() 高含氰废水可以通过电解法进行处理,阳极反应分两个阶段,第一阶段电极反应式:
高含氰废水可以通过电解法进行处理,阳极反应分两个阶段,第一阶段电极反应式:![]() ,请写出第二阶段的电极反应式________。
,请写出第二阶段的电极反应式________。
![]() 电解后低含氰废水通过化学氧化方法处理:在碱性条件下加入NaClO,将
电解后低含氰废水通过化学氧化方法处理:在碱性条件下加入NaClO,将![]() 氧化为碳酸盐与对环境友好气体。请写出相关离子反应方程式________。
氧化为碳酸盐与对环境友好气体。请写出相关离子反应方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿素是从复合花序植物黄花蒿中提取得到的一种有效的疟疾治疗药物。查阅资料知:常温下,青蒿素为无色针状晶体,味道较苦,难溶于水,易溶于有机溶剂,熔点为![]() ;从青蒿中提取青蒿素的方法主要有乙醚浸提法和溶剂汽油浸提法。
;从青蒿中提取青蒿素的方法主要有乙醚浸提法和溶剂汽油浸提法。
回答下列问题:
(一)用乙醚浸提法提取青蒿素的流程如下图:

(1)对青蒿进行破碎的目的是______。
(2)操作Ⅰ所用到的玻璃仪器是______,操作Ⅱ的仪器选择及安装都正确的是______(填标号)。

(3)操作Ⅲ的主要过程可能是______。
a.加水溶解,蒸发浓缩、冷却结晶
b.加95%乙醇,浓缩、结晶、过滤
c.加入乙醚进行萃取分液
(二)青蒿素分子式的测定
用如图所示的实验装置测定青蒿素的分子式,将28.2 g青蒿素放在燃烧管C中充分燃烧:

(4)①仪器各接口的连接顺序从左到右依次为______![]() 每个装置限用一次
每个装置限用一次![]() ;
;
②装置E中干燥管的作用是______;
③装置D中的试剂为______;
④已知青蒿素分子中只含碳、氢、氧三种元素,用合理连接后的装置进行实验,测量数据如表:
装置质量 | 实验前/g | 实验后/g |
B | 22.6 | 42.4 |
E(不含干燥管) | 80.2 | 146.2 |
则青蒿素分子中碳、氢、氧三种原子的个数比为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com