
| A. | 用聚光手电筒照射,产生丁达尔效应 | |
| B. | 加入碘水,溶液变蓝 | |
| C. | 加入稀硫酸振荡并加热,再加入新制Cu(OH)2悬浊液,有红色沉淀生成 | |
| D. | 加入碘化钾溶液后,无明显现象 |
分析 A.淀粉溶液属于胶体;
B.淀粉遇碘变蓝色;
C.淀粉在稀硫酸催化作用下水解所得溶液呈酸性;
D.淀粉和碘化钾不发生反应.
解答 解:A.淀粉溶液属于胶体,所以用聚光手电筒照射,产生丁达尔效应,故A正确;
B.淀粉遇碘变蓝色,因此淀粉溶液中加入碘水,溶液变蓝,故B正确;
C.淀粉在稀硫酸催化作用下水解所得溶液呈酸性,需要加入适量氢氧化钠溶液中和后,再加入新制Cu(OH)2悬浊液,才有红色沉淀生成,故C错误;
D.淀粉和碘化钾不发生反应,因此淀粉溶液中加入碘化钾溶液后,无明显现象,故D正确;
故选C.
点评 本题考查了淀粉的性质,难度不大,掌握淀粉的性质以及葡萄糖的特征反应是解题关键,注意葡萄糖发生特征反应时溶液需要具备碱性环境.


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:解答题
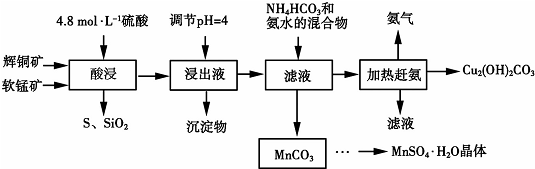
| 物质 | Cu(OH)2 | Fe(OH)2 | Mn(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 8.3 | 1.4 |
| 沉淀完全pH | 13 | 14 | 9.8 | 3.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉是纯净物,漂白液是混合物 | |
| B. | 漂白粉中含有次氯酸,所以漂白粉能使燃料等有机色素褪色 | |
| C. | 工业上将氯气通入澄清石灰水制取漂白粉 | |
| D. | 次氯酸能杀死病菌,所以氯气可用于自来水的消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质:硫磺、石英、水银 | B. | 化合物:盐酸、食盐、烧碱 | ||
| C. | 混合物:空气、胶体、海水 | D. | 非电解质:铜、蔗糖、酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中生成(2g+h)molH2O | B. | 2d+3f=3g+h | ||
| C. | 2<3g+h<3 | D. | h随着d增大而增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
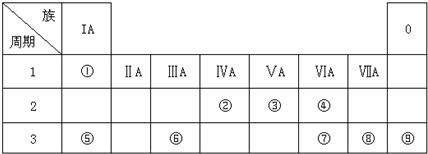

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式符合CnH2n+2的烃一定是烷烃 | |
| B. | 烷烃均能与氯水发生取代反应 | |
| C. | 正戊烷的熔沸点比异戊烷的高 | |
| D. | 烷烃不能被酸性高锰酸钾等强氧化剂氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com