
һ���¶��£����淴Ӧ2NO2(g)  2NO(g)��O2(g)������̶����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
2NO(g)��O2(g)������̶����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
�ٵ�λʱ��������n mol O2��ͬʱ����2n mol NO2
�ڵ�λʱ��������n mol O2��ͬʱ����2n mol NO
����NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1
�ܻ�������ѹǿ���ٸı�
�ݻ���������ɫ���ٸı�
��������ƽ����Է����������ٸı�
A���٢ܢݢ� B���٢ڢۢ� C���ڢۢܢ� D������ȫ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016������ʡ������12��ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�Ԫ�ػ������˵����ȷ����
A�������£�1molͭƬͶ�뺬��4mol HNO3��Ũ�����У�ͭƬ������ȫ�ܽ�
B��Al��Sֱ�ӻ��Ͽ��Եõ�Al2S3,Fe��Sֱ�ӻ���Ҳ���Եõ�Fe2S3
C�����AlCl3��FeCl3��CuCl2�Ļ����Һ�У���������������Al��Fe��Cu
D���������������Ͻ������ĺ���Խ�����������ᷴӦʱ�ų�������Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡ��һ��ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ��ƶ���
���п�ͼ�е����ʾ�Ϊ��ѧ��ѧ�г������ʣ����мס���Ϊ���ʣ������Ϊ�����BΪ����Һ̬�����AΪ����ɫ���壬F��G����Ԫ����ͬ�Ҿ�Ϊ�Ȼ��G��KSCN��Һ�Ժ�ɫ��
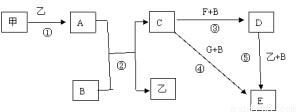
���ʴ��������⣺
��1��A��____________��G��______________�����ѧʽ��
��2����Ӧ��-���У�����������ԭ��Ӧ����________________������ţ���
��3����Ӧ�ݵĻ�ѧ����ʽΪ_________________________��
����B��Ӧ�����ӷ���ʽ ___________________________��
��4����ʵ���ҽ�C��Һ����F��Һ�У��۲쵽��������___________________��
��5����F��Һ�м�������ʵ�����A��������Ӧ���ܵ����ӷ���ʽ�� ____________________��
��6����֪����̪��c(OH��) Ϊ1.0��10��4mol/L��2.5mol/Lʱ�ʺ�ɫ���Ұ�����ڲ���ɫ����3.9g A�� 100g B��Ϻ����Һ�е���2�η�̪��Һ����Һ���ɫ��Ƭ�̺�ɫ��ȥ�������������Һ��������䣩�ټ�ͬѧ��Ϊ����ɫѸ����ȥ����������Һ��c(OH-)������ɵġ�
�����۵��Ƿ���ȷ ����ͨ������Ա����ݼ���˵��_____________________��
����ͬѧ��Ϊ����ɫѸ����ȥ��������A + B = �� + H2O2 ��H2O2���������Ժ�Ư���Ե��µġ�����Ƽ�ʵ��֤����ƿ����Һ�к�H2O2������ʵ��ԭ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡ�߶���ѧ�ڵ�һ���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ڳ��ͷŵ�ʱ�����ķ�Ӧ��Fe+ NiO2+2H2O Fe(OH)2+Ni(OH)2�����и������ƶϲ���ȷ����
Fe(OH)2+Ni(OH)2�����и������ƶϲ���ȷ����
A���ŵ�ʱ��Fe���븺����Ӧ��NiO2����������Ӧ
B�����ʱ�������ϵĵ缫��ӦʽΪ��Fe(OH)2 + 2e- = Fe + 2OH-
C�����صĵ缫�������ij�ּ��Ե������Һ��
D���ŵ�ʱ���������Һ�е������������������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡ�߶���ѧ�ڵ�һ���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ��һ��һ���Լ��ȱ���ʾ��ͼ����ˮ������ʱ��ˮ���������ͣ�����ʳ���¶�������������˼��ȱ���ѡ�õĹ��������

A������� B����ʯ�� C���Ȼ�þ D��ʳ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡͩ���и߶������У���ͨ�ࣩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͼ��ʾ�����������Ʋ�ͬ���������������������У��ټ��뺬��������̪��NaCl����֬����Һ����ȴ���γ������������������ڿ����ƶ���������������ȷ����
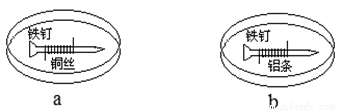
A��a�������������ֺ�ɫ B��b�������Ϸ�����ԭ��Ӧ
C��a��ͭ˿�Ϸ���������Ӧ D��b���������������ݲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡͩ���и߶������У�ʵ��ࣩ��ѧ�Ծ��������棩 ���ͣ������
Һ�������ֽ��������������Ϊ����ȼ�ϵ�ص�ȼ�ϡ������ֽⷴӦ���Ȼ�ѧ����ʽ���£�
2NH3(g)  N2 (g) + 3H2(g) ?H = + a kJ��mol-1
N2 (g) + 3H2(g) ?H = + a kJ��mol-1
��ش��������⣺
��1����֪��2H2 (g) + O2 (g) =2H2O(l) ?H = - b kJ��mol-1
NH3 (g)  NH3(l) ?H = - c kJ��mol-1
NH3(l) ?H = - c kJ��mol-1
��4NH3(l) + 3O2 (g) = 2N2 (g) + 6H2O(l) ��?H = kJ��mol-1��
��2��ˮ�ܷ������룺2H2O(l)  H3O++OH-��Һ��Ҳ�ܷ������Ƶĵ��롣��д��Һ���ĵ��뷽��ʽ ��
H3O++OH-��Һ��Ҳ�ܷ������Ƶĵ��롣��д��Һ���ĵ��뷽��ʽ ��
��3��ʵ������Pt�缫��Һ�����е����Եõ�H2��N2 �����������������ռ��õ�4.48L���壨���������ת�Ƶĵ��ӵ���Ŀ�� ����״���������õ������������Ϊ g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʡ�߶��ϵ�һ�β⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
���ݻ�һ�����ܱ������У�����һ������NO(g)������C(s)��������ӦC(s)+2NO(g) CO2(g)+N2(g)��ƽ��״̬ʱNO(g)�����ʵ�����Һc(NO)���¶�T�Ĺ�ϵ����ͼ��ʾ��������˵���У���ȷ����( )
CO2(g)+N2(g)��ƽ��״̬ʱNO(g)�����ʵ�����Һc(NO)���¶�T�Ĺ�ϵ����ͼ��ʾ��������˵���У���ȷ����( )
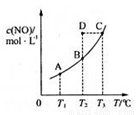
A���÷�Ӧ�ġ�H��0
B�����÷�Ӧ��T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2
C����T2ʱ������Ӧ��ϵ����״̬D������ʱһ����v����v��
D����T3ʱ�������������ܶȲ��ٱ仯��������жϷ�Ӧ�ﵽƽ��״̬C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����Һ��pH��4������Һ��pH��5������Һ������Һ��c(H��)֮��Ϊ( )��
A��10��1 B��1��10 C��2��1 D��1��2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com