
����Ŀ����A��B��C��D����ǿ����ʣ�������ˮ�е���ʱ�ɲ�����������(ÿ������ֻ��һ�������Ӻ�һ���������һ����ظ�)��
������ | K����Na����Ba2����NH |
������ | CH3COO����Cl����OH����SO |
��֪����A��C��Һ��pH������7��B��Һ��pHС��7��A��B��Һ��ˮ�ĵ���̶���ͬ��D���ʵ���ɫ��Ӧ�ʻ�ɫ����C��Һ��D��Һ����ʱֻ���ɰ�ɫ������B��Һ��C��Һ����ʱֻ�����д̼�����ζ�����壬A��Һ��D��Һ���ʱ����������
(1)A��������_______B�Ļ�ѧʽ_______
(2)д��C��Һ��D��Һ��Ӧ�Ļ�ѧ����ʽ___________
(3)25 ��ʱ��pH��9��A��Һ��pH��9��C��Һ��ˮ�ĵ���̶�С����___(��A��C)��
(4) A��Һ��pH����7�������ӷ���ʽ��ʾԭ��______��
���𰸡������ NH4Cl ![]() C
C ![]()
��������
��A��C��Һ��pH������7��ӦΪ�����κͼ���Һ��B��Һ��pHС��7��ӦΪ�����Һ��A��B����Һ��ˮ�ĵ���̶���ͬ������Һˮ��̶���ͬ��D��Һ��ɫ��Ӧ�Ի�ɫ����Һ�к��������ӣ�����AΪ����أ���C��Һ��D��Һ����ʱֻ���ɰ�ɫ������B��Һ��C��Һ����ʱֻ���ɴ̼�����ζ�����壬A��Һ��D��Һ���ʱ������������˵��CΪBa��OH��2��DΪNa2SO4����BΪNH4Cl��
(1) A�������Ǵ���أ�B�Ļ�ѧʽ��NH4Cl��
(2) C��Һ��D��Һ��Ӧ�Ļ�ѧ����ʽ��![]() ��
��
(3)�������ˮ�ĵ��룬�δٽ�ˮ�ĵ��룬��25 ��ʱ��pH��9��A��Һ��pH��9��C��Һ��ˮ�ĵ���̶�С����C��
(4) A��Һ�д��������ˮ��������������ӣ�����Һ��pH����7��![]() ��
��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯���������������ϵ���С������������գ�
��1��ijѧУ��ѧѧϰС��Ϊ̽���������������ʣ�����ͼ��ʾװ�ý���ʵ�顣

��װ�ü���ʢ��Ũ���������A��������__________________�� װ�ñ��е��Թ��ڷ�����Ӧ�����ӷ���ʽΪ��______________________________��
��ʵ�������װ���ҡ����г��ֵ�����ֱ���________________________��______________��
��2��NO��ҽ��������Ҫ��Ӧ�ã�������ѧ����Ϊ�о�����Ҫ���ʡ������ݻ�ΪaL���Թ�ʢ��NO����ˮ���У������Թ���ͨ��һ�����O2���Թ�����������Ϊ�Թ��ݻ���һ�룬��ͨ���O2������ͬ���������Ϊ____________��
A.0.75aL B.0.375aL C.0.625aL D.1.25aL
��3����ʢ��һ����Ũ������Թ��м���12.8g��ͭƬ������Ӧ����ش��������⣺
�ٿ�ʼ��,��Ӧ�Ļ�ѧ����ʽΪ_______________________________����һ�����ɵ�����Ϊ
_______,������ǡ����ȫ��Ӧ������Ӧ���̹�������״��������2.24L����Ӧ�����б���ԭ��HNO3�����ʵ���Ϊ__________ mol.,�μӷ�Ӧ��HNO3�����ʵ���Ϊ__________ mol.��
�ڷ�Ӧ���������Թ��м���ͭƬ���ټ�������20%��ϡ���ᣬ��ʱͭƬ���������ݲ�������Ӧ�����ӷ���ʽΪ____________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С����̽��̼��Ũ���ᷴӦ���������ͬѧ�����ͼ1װ�ã���Ϊ���к���ɫ���������˵��̼��Ũ���ᷢ���˷�Ӧ��
��1����ͬѧ��Ϊ��ͬѧ�Ľ����Ǵ���ģ�����������__________________________(�û�ѧ����ʽ��ʾ)����������ΪӦ�ü���__________(�ѧʽ)�IJ�����֤��̼��Ũ���ᷴӦ��Ϊ����ͬѧ����������ϵ�֪��0��ʱ����������ΪҺ�������Ӷ��Ľ���ʵ��װ����ͼ2��ʾ��

��2��Ϊ�˼��ٸ��ţ�����Aװ��������4�ֲ���������������������ǣ���д������ţ�_______��
�ٽ�̿��Ũ����һͬ����װ���м��ȣ����ȼ���Ũ���ᣬȻ��̿Ͷ�����У�
���ȼ���̿���ټ�����Ũ��� ���ȼ���̿���ٽ�̿Ͷ����Ũ���ᡣ
��3������ƽ���ƶ�ԭ������Bװ�õ�����____________________________________��
��4��Cװ���г��ֵ�������_______________________________________________�������C����Һ�л�����������Ԫ�أ�ֻ��NO3����ʽ���ڣ�д�����ɸ����ӵĻ�ѧ����ʽ___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л��������ұ���G2762011���涨���Ѿ���c���ʹ����Ϊ0.25g/L.ij��ȤС����ͼװ�ã��г�װ���ԣ��ռ�ij���Ѿ���SO2�����Ժ������вⶨ��
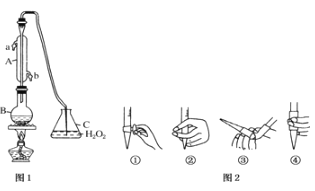
��1������A��������________��ˮͨ��A�Ľ���Ϊ_______________
��2��B�м���300.0ml���Ѿƺ��������ᣬ����ʹSO2ȫ���ݳ���C��H2O2��ȫ��Ӧ�仯ѧ����ʽΪ_________________________________
��3����ȥC�й�����H2O2��Ȼ����0.0900mol/LNaOH����Һ���еζ����ζ�ǰ������ʱ��Ӧѡ��ͼ2�е�________�����ζ��յ�ʱ��Һ��pH=8.8����ѡ���ָʾ��Ϊ________������50mL�ζ��ܽ���ʵ�飬���ζ����е�Һ���ڿ̶ȡ�20�����������Һ������______������ţ�
����=20mL����=30mL���ۣ�20mL���ܣ�30mL����
��4���ζ����յ�ʱ������NaOH��Һ12.50mL�������Ѿ���SO2����Ϊ:___g/L
��5���òⶨ�����ʵ��ֵƫ�ߣ�����ԭ����������װ������Ľ���ʩ______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��������
(1)����25 ��ʱ������Һ��pH��
��1 mL pH��2��H2SO4��ˮϡ����100 mL��pH��________��
��0.001 mol/L�����ᣬpH��________��
��0.01 mol/L��NaOH��Һ��pH��________��
��0.015 mol/L��������0.01 mol/L��NaOH�������ϣ������Һ��pH��________��
(2)H2S����ˮ�ĵ��뷽��ʽΪ_______________________________________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E����Ԫ������֪��
��Aԭ�ӵ������������Ǵ�����������������B����������C�������Ӹ���ԭ�ӵĵ��Ӳ�ṹ��ͬ��Eԭ�ӵ�������ϵĵ����������ڲ��5��
�ڳ�����B2��������������Է���������������16����
��C�ĵ�����B2��ȼ�������ɵ���ɫ����F��F��AB2��Ӧ������B2��
��D�ĵ�����B2��ȼ������������ɫ�����������д̼�����ζ������DB2��D��DB2�еĺ���Ϊ50%��������������ش�:
(1)Eλ�ڵ�___����___����
(2)C�����ӽṹʾ��ͼ��_____��F�еĻ�ѧ��Ϊ______��
(3)AB2�ĵ���ʽΪ___�� F��AB2��Ӧ�Ļ�ѧ����ʽΪ_______��
(4)C��D��E����Ԫ�ص�ԭ�Ӱ뾶��С�����˳��Ϊ___�� (��Ԫ�ط��Żش�)
(5)��������E�ĵ�����C������������Ӧˮ�����ˮ��Һ��Ӧ�����ӷ���ʽΪ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؾ���������У�����ȷ����(����)
A.���ʯΪ��״�ṹ���ɹ��ۼ��γɵ�̼ԭ�ӻ��У���С�Ļ�����6��̼ԭ��
B.�Ȼ��ƾ����У�ÿ��Na����Χ�����Ҿ�����ȵ�Na������6��
C.�Ȼ�菉����У�ÿ��Cs����Χ�����Ҿ�����ȵ�Cl����8��
D.�ɱ������У�ÿ��CO2������Χ�����Ҿ�����ȵ�CO2������12��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯�������л���ѧ��Ӧ�ù㷺�������л��ϳ��У������������Ὣ��������NO2����ԭΪ��������NH2�����ڱ��������Ӧ�����廯����������
��1��N��ԭ�ӽṹʾ��ͼΪ_______��Fe��̬ԭ�Ӻ�������Ų�ʽΪ_______��
��2��H��N��O �ĵ縺�Դ�С�����˳����_______��
��3����NO2+��Ϊ�ȵ������һ�ַ���Ϊ_____���ѧʽ������������NH2���е�ԭ�ӵ��ӻ�����Ϊ_____��
��4��1mol�������к��ЦҼ������ʵ���Ϊ______��
��5��Fe �� N �γɵ�ij�����ᄃ����ͼ��ʾ����þ���Ļ�ѧʽΪ_______��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ��2NO2(g)![]() 2NO(g) + O2(g)�������������ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��( )
2NO(g) + O2(g)�������������ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��( )
����λʱ��������n mol O2��ͬʱ����2 n mol NO2
����λʱ��������n mol O2��ͬʱ����2 n mol NO
����NO2��NO��O2��ʾ�ķ�Ӧ������ֵ֮��Ϊ2��2��1��״̬
������������ɫ���ٸı��״̬
A.�٢�B.�ڢ�C.�٢ۢ�D.�٢ڢۢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com