
| A. | 若反应物总能量大于生成物总能量则反应为放热反应 | |
| B. | 电池工作时将化学能转变成电能 | |
| C. | 绿色植物光合作用过程中太阳能转变成化学能 | |
| D. | 生物质能只能通过含有生物质能的物质的直接燃烧转化成热能从而被利用 |
分析 A.放热反应反应物总能量大于生成物总能量;
B.电池工作时将化学能转变成电能;
C.太阳能可以转化为多种形式的能量,但绿色植物的光合作用是将太阳能转化为化学能;
D.生物质能源是将生物或生物废料,以原始状态或经加工转化之后,取来作为能源.
解答 解:A.反应物总能量大于生成物总能量则反应为放热反应,故A正确;
B.电池工作时,发生氧化还原反应,将化学能转变成电能,故B正确;
C.绿色植物可以通过光合作用将太阳能转化为化学能储存起来,供植物生长,故C正确;
D.生物质能以原始状态或经加工转化之后,取来作为能源,不一定是通过含有生物质能的物质的直接燃烧转化成热能从而被利用的,故D错误.
故选D.
点评 本题考查了化学反应能量变化、原电池原理、化学能源等方面的知识,属于基本知识的考查,注意知识的归纳和整理是关键,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | F-的结构示意图: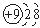 | B. | O-18的原子符号:${\;}_{10}^{18}$O | ||
| C. | NaCl的电子式: | D. | N2的结构式::N≡N: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 请回答下列问题:
请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
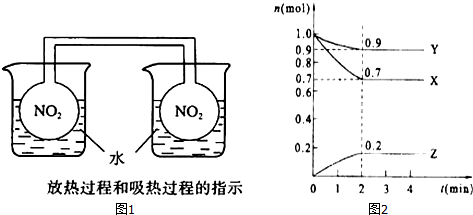
 2Z;
2Z;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 红色、黑色、白色 | B. | 红色、白色、白色 | C. | 红色、红色、红色 | D. | 黑色、红色、白色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
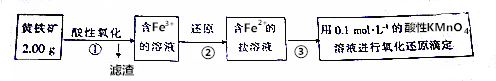
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com