
铈、铬、钴、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。
(1)二氧化铈 (CeO2)在平板电视显示屏中有着重要应用。CeO2在稀硫酸和H2O2的作用下可生成Ce3+,CeO2在该反应中作_____剂。
 (2)自然界Cr主要以+3价和+6价存在。+6价的Cr能引起细胞的突变,可以用亚硫酸钠将其还原为+3价的铬。完成并配平下列离子方程式:
(2)自然界Cr主要以+3价和+6价存在。+6价的Cr能引起细胞的突变,可以用亚硫酸钠将其还原为+3价的铬。完成并配平下列离子方程式:
 __Cr2O72-+__SO32-+__ =__Cr3++__SO42-+ __H2O
__Cr2O72-+__SO32-+__ =__Cr3++__SO42-+ __H2O
(3)某锂离子电池用含有Li+的导电固体作为电解质。充电时,Li+还原为Li,并以原子形式嵌入电极材料C6中,以LiC6表示,电池反应为CoO2+LiC6  LiCoO2+C6。放电时的正极反应式为___________。右图表示该装置工作时电子和离子的移动方向,此时C6电极作____极。
LiCoO2+C6。放电时的正极反应式为___________。右图表示该装置工作时电子和离子的移动方向,此时C6电极作____极。
(4)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ•mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160kJ•mol-1
甲烷直接将NO2还原为N2的热化学方程式为 _________________________________ 。
(5)NiSO4·6H2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、锌、铁等元素)为原料获得。操作步骤如下:


①向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质,除去Cu2+的离子方程式为__________。
②对滤液Ⅱ调pH的目的是除去Fe3+,其原理是Fe3++3H2O Fe(OH)3+3H+,已知25℃时Ksp[Fe(OH)3]=2.8×10-39,则该温度下上述反应的平衡常数K= 。
Fe(OH)3+3H+,已知25℃时Ksp[Fe(OH)3]=2.8×10-39,则该温度下上述反应的平衡常数K= 。
③滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是______________。
科目:高中化学 来源: 题型:
某有机物的结构为右图所示,下列有关它的叙述不正确的是( )
①分子式为C11H14O3 ②能使酸性KMnO4溶液褪色,不能使溴水褪色
③能跟NaOH溶液反应 ④能发生酯化反应
⑤能发生加聚反应 ⑥有四种官能团 ⑦1mol该物质最多和4molH2反应
⑧两份等量的该物质分别和足量Na、NaHCO3反应得到气体物质的量之比为1∶2
A.②⑦⑧ B.①②⑥⑧ C.⑤⑦⑧ D.①②⑥
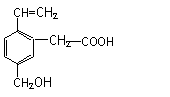 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各表述与示意图一致的是

A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO2(g) + O2(g) 2SO3(g) ΔH < 0 正、逆反应的平衡常数K随温度的变化
2SO3(g) ΔH < 0 正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.01 mol·L-1 KMnO4 酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2 (g) + H2(g) CH3CH3(g);ΔH< 0使用和未使用催化剂时,反应过程中的能量变化
CH3CH3(g);ΔH< 0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25℃时
① HF(aq)+OH—(aq)=F—(aq)+H2O(l) △H=—67.7 KJ·mol—1
② H+(aq)+OH—(aq)=H2O(l) △H=—57.3 KJ·mol—1
在20 mL 0.1 mol·L—1氢氟酸中加入V mL 0.1 mol·L—1 NaOH溶液,下列有关说法正确的是
A.氢氟酸的电离方程式及热效应可表示为:HF(aq)=H+(aq) +F—(aq) △H=+10.4 KJ·mol—1
B.当V=20时,溶液中:c(OH—)=c(HF) +c(H+)
C.当V=20时,溶液中:c(F—)<c(Na+)=0.1mol·L—1
D.当V>0时,溶液中一定存在:c(Na+)>c(F—)>c(OH—)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中微粒的物质的量浓度关系一定正确的是
A.pH=9的NaHA溶液:c(Na+)>c(HA-)>c(A2-)>c(H2A)
B.Na2CO3溶液:c(H+)-c(OH-) = c(HCO3-) +2c(CO32-)-c(Na+)
C.稀盐酸中加入一定量氨水后溶液显碱性:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
D.将0.1mol·L-1 HF溶液与0.1mol·L-1 KF溶液等体积混合:c(F-)+c(HF)=0.2mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
丙烯酸(CH2 = CH — COOH)的性质可能有:( )
① 加成反应 ②取代反应 ③酯化反应 ④中和反应 ⑤氧化反应
A.只有①③ B.只有①③④
C.只有①③④⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
把500mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含bmol硝酸银的溶液,恰好使氯离子完全沉淀。则该溶液中钾离子浓度为( )
A.0.1(b-2a)mol·L-1 B.10(2a-b)mol·L-1
C.10(b-a)mol·L-1 D.10(b-2a)mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
国际无机化学命名委员会在1989年作出决定,把长式周期表原先的主、副族及族号取消,由从左至右改为18列,碱金属族为第1列,稀有气体为第18列。按这个规定,下列说法不正确的是
A.第15列元素的最高价氧化物为R2O5 B.第2列元素中肯定没有非金属元素
C.第17列元素中的第一种元素的非金属性最强D.第16、17列元素都是非金属元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com