
【题目】两种气态烃以任意比例混合,105℃时,1 L该混合烃与9 L O2混合,充分燃烧后恢复到原状况,所得气体体积仍为10 L。下列各组混合烃中不符合此条件的是 ( )
A.CH4、C2H4B.CH4、C3H6
C.C2H4、C3H4D.CH4、C3H4
【答案】B
【解析】
设有机物的平均式为CxHy,则有:CxHy+![]() O2
O2![]() xCO2+
xCO2+![]() H2O,105℃时H2O呈气态,有机物燃烧前后体积不变,则1+
H2O,105℃时H2O呈气态,有机物燃烧前后体积不变,则1+![]() =x+
=x+![]() ,解得y=4,即混合气中平均含有H原子数为4,
,解得y=4,即混合气中平均含有H原子数为4,
A.CH4、C2H4中H原子数都为4,不论两者以何种比例混合,H原子平均值恒为4,符合前后体积不变,故A符合条件;
B.CH4、C3H6中H原子数分别为4、6,平均值介于4和6之间,故B不符合条件;
C.C2H4、C3H4中H原子数都为4,不论两者以何种比例混合,H原子平均值恒为4,符合前后体积不变,故C符合条件;
D.CH4、C3H4中H原子数都为4,不论两者以何种比例混合,H原子平均值恒为4,符合前后体积不变,故D符合条件;
答案选B。


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】化学反应原理在科研和工农业生产中有广泛应用。
(1)某化学兴趣小组进行工业合成氨的模拟研究,反应的方程式为N2(g)+3H2(g)![]() 2NH3(g) △H<0。在1L蜜闭容器中加入0.1molN2和0.3molH2,实验①、②、③中c(N2)随时间(t)的变化如图所示:
2NH3(g) △H<0。在1L蜜闭容器中加入0.1molN2和0.3molH2,实验①、②、③中c(N2)随时间(t)的变化如图所示:
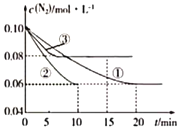
实验②从初始到平衡的过程中,该反应的平均反应速率v(NH3)=___;与实验①相比,实验②和实验③所改变的实验条件分别为下列选项中的___(填字母编号)。
a.增大压强 b.减小压强 c.升高温度 d.降低温度 e.使用催化剂
(2)800K时向下列起始体积相同的密闭容器中充入2molN2、3molH2,甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙是绝热容器,三容器各自建立化学平衡。
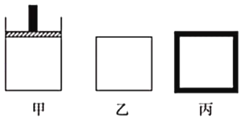
①达到平衡时,平衡常数K甲___K乙___K丙(填“>”“<“或“=”)。
②达到平衡时N2的浓度c(N2)甲___c(N2)乙,c(N2)乙___c(N2)丙(填“>”<”或“=”)
③对甲、乙、丙三容器的描述,以下说法正确的是___。
A.乙容器气体密度不再变化时,说明此反应已达到平衡状态
B.在甲中充入稀有气体He,化学反应速率加快
C.向甲容器中充入氨气,正向速率减小,逆向速率增大
D.丙容器温度不再变化时说明已达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值。下列说法错误的是
A.反应![]() 中,每生成294 g
中,每生成294 g![]() g释放的中子数为3NA
g释放的中子数为3NA
B.常温常压下,22.4 L乙烷和丙烯(C3 H6)的混合物中氢原子数目为6NA
C.1 L0.5 mol. L-1'碳酸钠溶液含有的CO32- 数目小于0.5NA
D.0.1 mol H2O2与MnO2充分作用生成O2,转移的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】列有机化合物中都含有多个官能团:
A.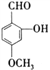 B.
B.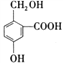 C.
C.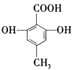 D.
D.![]() E.
E.![]()
(1)可以看作醇类的是________.
(2)可以看作酚类的是________.
(3)可以看作羧酸类的是________.
(4)可以看作酯类的是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO、SO2是常见的大气污染物,应用化学原理变废为宝,意义重大。
(1)CO与SO2用铝矾土作催化剂、475 ℃条件下反应生成CO2和硫蒸气,该反应可用于从烟道气中回收硫,反应过程中各组分的物质的量与反应时间的关系如图所示,该反应的化学方程式为________。
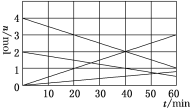
(2)利用CO可以合成新能源物质——甲醇。其原理为CO(g)+2H2(g)![]() CH3OH(g) ΔH。在压强分别为p1、p2,体积均为V L的两个容器中充入a mol CO、2a mol H2,在催化剂作用下反应生成甲醇,平衡时转化率与温度、压强的关系有下表数据:
CH3OH(g) ΔH。在压强分别为p1、p2,体积均为V L的两个容器中充入a mol CO、2a mol H2,在催化剂作用下反应生成甲醇,平衡时转化率与温度、压强的关系有下表数据:
50 ℃ | 100 ℃ | 200 ℃ | 300 ℃ | 400 ℃ | |
p1 | 0.65 | 0.50 | 0.40 | 0.32 | 0.24 |
p2 | 0.80 | 0.70 | 0.65 | 0.50 | 0.41 |
①ΔH________0,p1________p2。(填“>”“<”或“=”)。
②压强为p2,温度为300 ℃时,该反应的平衡常数K=________。
③压强为p1,温度为100 ℃时,达到平衡后,继续向其中通入0.5a mol CO、a mol H2、0.5a mol CH3OH,则平衡时CH3OH的体积分数________(填“增大”“减小”或“不变”)。
④下列说法正确的是________。
a.当n(CO)∶n(H2)∶n(CH3OH)=1∶2∶1时,可逆反应达到平衡状态
b.平衡后向体积为V L的容器内继续充入He,平衡不移动
c.使用新型催化剂,可提高CO的平衡转化率
(3)MnO2悬浊液、NaOH溶液都是SO2气体常用的吸收剂。
①已知MnO2+SO2=MnSO4,吸收SO2的装置如图所示。反应过程中,为使SO2尽可能转化完全,可采取的合理措施有___________、__________。
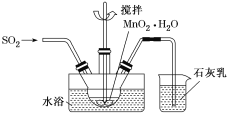
②将标准状况下4.48 L SO2气体缓缓通入100 mL 3 mol·L-1 NaOH溶液中,充分反应后c(Na+)=___ (填几种粒子浓度之和)。
③取②中所得溶液10 mL,加水稀释成1 L,向其中加入CaCl2固体至有沉淀CaSO3(Ksp=3.1×10-7)生成,则所加CaCl2固体的质量为_____mg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室制取乙炔并验证其性质的装置图。下列说法不合理的是 ( )
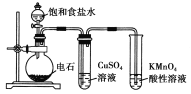
A.用Br2的CCl4溶液验证乙炔的性质,不需要除杂
B.KMnO4酸性溶液褪色,说明乙炔具有还原性
C.逐滴加入饱和食盐水可控制生成乙炔的速率
D.将纯净的乙炔点燃,有浓烈的黑烟,说明乙炔不饱和程度高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2O是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或加热时会发生燃烧并爆炸。一种制取Cl2O的装置如图所示。
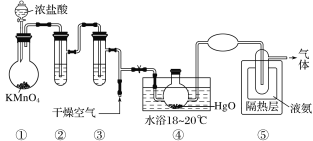
已知:Cl2O的熔点为-116℃,沸点为3.8℃;Cl2的沸点为-34.6℃;HgO+2Cl2=HgCl2+Cl2O。
下列说法中不正确的是( )
A.装置②③中盛装的试剂依次是饱和食盐水和浓硫酸
B.通入干燥空气的目的是将生成的Cl2O稀释,减小爆炸危险
C.从装置⑤中逸出气体的主要成分是Cl2
D.装置④与⑤之间不用橡胶管连接,是为了防止橡胶管燃烧和爆炸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某有机物分子的比例模型,有关该物质的推断不正确的是( )

A.分子中可能含有羟基
B.分子中可能含有羧基
C.分子中可能含有氨基
D.该物质的化学式可能为C3H6O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】呋喃酚是合成农药的重要中间体,其合成路线如下:
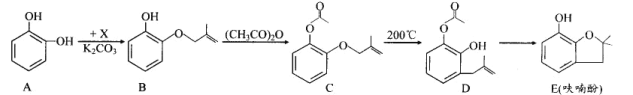
(1)A 物质核磁共振氢谱共有___________个峰,B→C 的反应类型是_____;E 中含有 的官能团名称是_____,D不能够发生的反应有_________(填代号)。
①氧化反应 ②取代反应 ③加成还原 ④消去反应
(2)已知 X 的分子式为 C4H7Cl,写出 A→B 的化学方程式:_____________。
(3)Y 是 X 的同分异构体,分子中无支链且不含甲基,则 Y 的名称(系统命名)是 ________。
(4)下列有关化合物 C、D 的说法正确的是_____________。
①可用氯化铁溶液鉴别 C 和 D ②C、D 含有的官能团完全相同
③C、D 互为同分异构体 ④C、D 均能使溴水褪色
(5)E 的同分异构体很多,写出符合下列条件的芳香族同分异构体的结构简式:____________。
①环上的一氯代物只有一种 ②含有酯基 ③能发生银镜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com