

分析 (1)装置气密性检验的原理是:通过气体发生器与附设的液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏;
(2)制取无水氯化亚铁,需要HCl气体,尾气的成分是剩余HCl和生成的氢气,HCl极易溶解于水,缺少防止水蒸汽进入C中装置,氢气不能溶于水;若要制取纯净的FeCl2,需先点燃A处的酒精灯排除装置中的空气,再点燃C处的酒精灯;
(3)从明矾[KAl(SO4)2•12H2O]制备Al、K2SO4和H2SO4的流程:过程①明矾和硫焙烧,4KAl(SO4)2•12H2O+3S=2K2SO4+2Al2O3+9SO2↑+48H2O,气体二氧化硫与氧气在五氧化二矾作催化剂的作用下生成三氧化硫,三氧化硫用98.3%的浓硫酸吸收,SO3+H2O=H2SO4,制得硫酸;过程②焙烧所得固体混合物,用水浸,为提高浸出率,可采取粉碎固体混合物、不断搅拌,从水浸后的滤液中蒸发结晶得到K2SO4晶体,步骤③电解Al2O3,制得Al.
①“焙烧”过程中得到SO2与固体混合物,而固体混合物进行水浸,过滤得到Al2O3与K2SO4,则焙烧”过程中得到SO2、Al2O3、K2SO4,同时有水生成,配平是化学方程式;
②从溶液中获得晶体,需要经过蒸发浓缩、冷却结晶、过滤等操作;步骤③为氧化铝电解生成铝和氧气;
③将SO2的利用率转化为KAl(SO4)2•12H2O的利用率,由焙烧”过程中反应方程式,及硫元素守恒,可得关系式:4KAl(SO4)2•12H2O~9H2SO4,据此计算.
解答 解:(1)装置气密性检验的原理是:通过气体发生器与附设的液体构成封闭体系,改变体系内压强,生成气泡或形成水柱是常用的方法,所以图1装置,检查装置的气密性,把B、D中导管下端浸入水中,用洒精灯给烧瓶微热,看到B、D中导管下口有气泡冒出,停止加热后,有一段稳定的水柱,说明装置不漏气,
故答案为:把B、D中导管下端浸入水中,用洒精灯给烧瓶微热,看到B、D中导管下口有气泡冒出,停止加热后,有一段稳定的水柱,说明装置不漏气;
(2)制取无水氯化亚铁,需要HCl气体,故A装置制取的是HCl,反应方程式为:Fe+2HCl$\frac{\underline{\;\;△\;\;}}{\;}$FeCl2+H2,故尾气的成分为未反应的HCl和生成的氢气,由于HCl极易溶于水,故若仍然采用D装置进行尾气处理,很容易造成倒吸,且缺少防止水蒸汽进入C中装置,氢气不溶于水,不利于氢气的吸收,氢气易燃,造成安全隐患,若要制取纯净的FeCl2,需先排净装置中的空气,防止在加热时Fe与O2反应,故先点燃A处的酒精灯,再点燃C处的酒精灯,
故答案为:HCl; 易发生倒吸,缺少防止水蒸汽进入C中装置; 通入氯化氢(赶尽装置中的空气);
(3)①“焙烧”过程中得到SO2与固体混合物,而固体混合物进行水浸,过滤得到Al2O3与K2SO4,则焙烧”过程中得到SO2、Al2O3、K2SO4,同时有水生成,发生反应为:4KAl(SO4)2•12H2O+3S$\frac{\underline{\;高温\;}}{\;}$2Al2O3+2K2SO4+9SO2↑+48H2O,
故答案为:4KAl(SO4)2•12H2O+3S=2K2SO4+2Al2O3+9SO2↑+48H2O;
②从溶液中获得晶体,需要经过蒸发浓缩、冷却结晶、过滤等操作,步骤③为电解氧化铝,氧化铝熔点高,用冰晶石作助熔剂,电解氧化铝生成铝和氧气,反应为:2Al2O3$\frac{\underline{\;\;\;\;\;冰晶石\;\;\;\;\;}}{970℃电解}$4Al+3O2↑,
故答案为:蒸发、结晶;2Al2O3$\frac{\underline{\;\;\;\;\;冰晶石\;\;\;\;\;}}{970℃电解}$4Al+3O2↑;
③设可生产x吨质量分数为98%的硫酸,则:
4KAl(SO4)2•12H2O~9H2SO4,
4×b 9×98
at×96% xt×98% 解得:x=$\frac{216a}{b}$,
故答案为:$\frac{216a}{b}$.
点评 本题以氯化铁以及氯化亚铁、Al、K2SO4和H2SO4制取为载体,考查的是实验室中氯气的制取方法、常见尾气的处理方法以及铁离子的检验等,是对学生综合能力的考查,需要学生具备扎实的基础,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | c mol/L | B. | 3c mol/L | C. | $\frac{3c{V}_{1}}{{V}_{2}}$mol/L | D. | $\frac{c{V}_{1}}{{V}_{2}}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
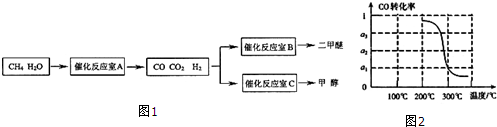
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
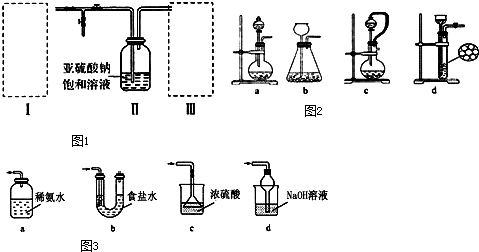
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
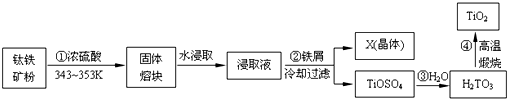
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
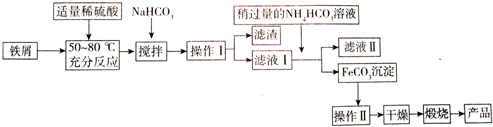
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 沉淀完全 | 3.2 | 9.7 | 4.4 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 消耗1molA的同时消耗1mol B | B. | 消耗n molA,同时生成2nmolC | ||
| C. | 气体的总体积不变 | D. | 容器内气体密度不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com