
| A. | 由上述反应可知,ClO-的氧化性强于FeO42- | |
| B. | 高铁酸钾中铁显+6价 | |
| C. | 上述反应中氧化剂和还原剂的物质的量之比为2:3 | |
| D. | K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
分析 A.氧化剂的氧化性强于氧化产物的氧化性.据此判断.
B.离子中各元素化合价代数和等于离子所带电荷.据此计算.
C.反应中Fe(OH)3是还原剂,C1O-是还原剂,根据电子转移守恒计算二者物质的量之比.
D.K2FeO4中铁为高价铁,具有强氧化性能杀菌,Fe(OH)3(胶体)具有净水作用.
解答 解:A.反应Fe(OH)3+C1O-+OH-→FeO42-+C1-+H2O中,氯元素化合价降低,C1O-是氧化剂,铁元素化合价升高,Fe(OH)3是还原剂,FeO42-是氧化产物,氧化性C1O->FeO42-,故A正确;
B.令FeO42-中,铁元素的化合价为x,则x+4×(-2)=-2,解得x=+6,故B正确;
C.反应Fe(OH)3+C1O-+OH-→FeO42-+C1-+H2O中,氯元素化合价由+1降低为-1价,C1O-是氧化剂,铁元素化合价由+3价升高为+6价,Fe(OH)3是还原剂,所以反应中氧化剂和还原剂的物质的量之比为(6-3):2=3:2,故C错误;
D.K2FeO4具有氧化性所以能杀菌,高铁酸钾被还原为Fe3+,Fe3+水解生成的Fe(OH)3(胶体)具有净水作用,故D正确.
故选:C.
点评 本题考查氧化还原反应基本概念与计算,题目难度不大,根据化合价判断氧化剂、还原剂与氧化产物、还原产物是关键,侧重于考查学生的分析能力和计算能力.


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:高中化学 来源: 题型:选择题
| A. | HCN分子的结构式:H-C≡N | B. | Se的简化电子排布式:[Ar]4s24p4 | ||
| C. | F-离子的结构示意图: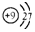 | D. | 二氧化碳的电子式 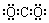 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
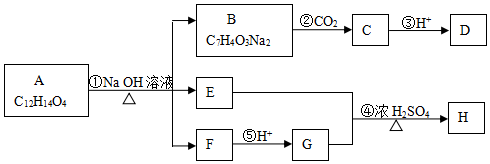
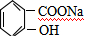 .
.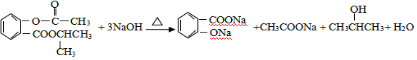 .
.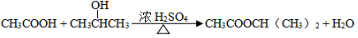 .
.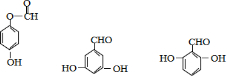 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
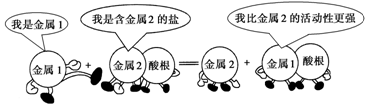
| A. | 此反应不可能是复分解反应 | |
| B. | 若金属1是锌,则金属2可能是铁 | |
| C. | 还原性:金属1>金属2 | |
| D. | 若金属2是铜,则生成2 mol铜时反应过程中转移2 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏法是海水谈化的方法之一 | |
| B. | 海水中的${\;}_{92}^{235}$U元素经浓缩提炼后可作核反应堆燃料 | |
| C. | 海水中的Li元素属于微量元素,提炼后可作Li电池原料 | |
| D. | 0℃以上,温度越高,水的密度越小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.1g | B. | 3.6g | C. | 7.2g | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
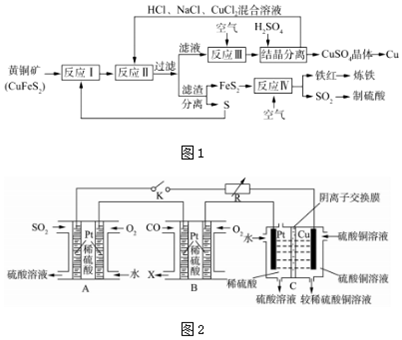
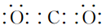 ,若在C池中生成64gCu,则整个装置中共生成H2SO42mol.
,若在C池中生成64gCu,则整个装置中共生成H2SO42mol.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com