
| A、①② | B、②③ | C、③④ | D、①④ |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、NaAlO2溶液中滴加过量盐酸:AlO2-+H2O+H+=Al(OH)3 | ||||
B、NH4HSO3溶液与足量浓NaOH溶液共热:NH4++HSO3-+2OH-
| ||||
| C、明矾溶于水产生Al(OH)3 胶体:Al3++3H2O=Al(OH)3↓+3H+ | ||||
| D、FeCl3溶液与Cu反应:Fe3++Cu=Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
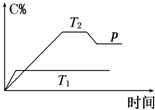 在一定条件下,可逆反应A+B?m C变化如图所示.已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:
在一定条件下,可逆反应A+B?m C变化如图所示.已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热23.15kJ |
| ② | 0.6 | 1.8 | 0.8 | Q(Q>0) |
| A、容器①、②中反应的平衡常数相等 |
| B、达平衡时,两个容器中XY3的物质的量浓度均为2mol?L-1 |
| C、容器②中反应达到平衡时放出的热量为Q |
| D、若将容器①体积缩小为0.20L,则达平衡时放出的热量大于23.15kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、取无水硫酸铜16 g溶于水配1L溶液 |
| B、取25 g胆矾溶于水配成1L溶液 |
| C、取16 g胆矾溶于1L水中配成 |
| D、取25 g胆矾溶于1L水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com