
工业上制备BaCl2的工艺流程图如下:

某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaSO4(s) + 4C(s)  4CO(g) + BaS(s) △H1 = 571.2
4CO(g) + BaS(s) △H1 = 571.2 kJ·mol-1 ①
kJ·mol-1 ①
BaSO4(s) + 2C(s)  2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
⑴气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。
⑵向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,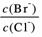 = 。
= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
⑶反应C(s) + CO2(g)  2CO(g)的△H= kJ·mol-1。
2CO(g)的△H= kJ·mol-1。
⑷实际生产中必须加入过量的炭,同时还要通入空气,其目的是 , 。
【答案】
⑴S2- + H2O HS- +OH- HS- + H2O
HS- +OH- HS- + H2O H2S +OH-(可不写)
H2S +OH-(可不写)
⑵2.7×10-3
⑶172.5
⑷使BaSO4得到充分的还原(或提高BaS的产量)
①②为吸热反应,炭和氧气反应放 热维持反应所需高温
热维持反应所需高温
【解析】(1)S2-水解以第一步为主。
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,在溶液中有如下关系:
AgCl(s) Ag+(aq)+Cl-(aq) AgBr(s)
Ag+(aq)+Cl-(aq) AgBr(s) Ag+(aq)+Br-(aq)
Ag+(aq)+Br-(aq)
由Ksp=(AgCl)=2.0×10-10=c1(Ag+)·c(Cl-)得c1(Ag+)=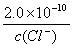
由Ksp=(AgBr)=5.4×10-13=c2(Ag+)·c(Br-)得c2(Ag+)=
同一溶液中c1( Ag+)=c2(Ag+)即
Ag+)=c2(Ag+)即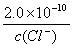 =
= 。
。
得出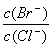 =2.7×10-3。
=2.7×10-3。
(3)根据盖斯定律,①-②得:
C(s)+CO2(g) 2CO(g);ΔH=172.5 kJ·mol-1。
2CO(g);ΔH=172.5 kJ·mol-1。
(4)在实际生产中加入过量的炭,可使BaSO4充分被还原,提高BaS的产量;又由于①②均为吸热反应,过量的炭与氧气反应放出的热量可维持反应所需的高温。


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
下列说法正确的是
A.有机物种类繁多的主要原因是有机物分子结构十分复杂
B.烃类分子中的碳原子与氢原子是通过非极性键结合的
C.同分异构 现象的广泛存在是造成有机物种类繁多的唯一原因
现象的广泛存在是造成有机物种类繁多的唯一原因
D.烷烃的结构特点是碳原子通过单键连成链状,剩余价键均与氢原子结合
查看答案和解析>>
科目:高中化学 来源: 题型:
⑴某烯烃与H2发生加成反应后得到的产物是CH3—CH(CH3)2.该产物的名称是 ;原来烯烃的结构简式为: ;
(2)今有化合物:

① 请写出化合物丙中官能团的名称: 。
② 请判别上述化合物互为同分异构体的是: 。
③ 请按酸性由强至弱排列甲、乙、丙的顺序: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn(s、白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1
②Sn(s、灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2
③Sn(s、灰) Sn(s、白) △H3=+2.1kJ/mol
Sn(s、白) △H3=+2.1kJ/mol
下列说法正确的是
A △H1>△H2
B 锡在常温下以灰锡状态存在
C 灰锡转化为白锡的反应是放热反应
D 锡制器皿长期处于低于13.2℃的环境中,会自行毁坏
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:①1 mol H2分子中化学键断裂时需要吸收436kJ的能量
②1 mol Cl2分子中化学键断裂时需要吸收243kJ的能量
③由H原子和Cl原子形成1 mol HCl分子时释放431kJ的能量
下列叙述正确的是
A.氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)=2HCl(g)
B.氢气和氯气反应生成2 mol氯化氢气体,反应的△H=183kJ/mol
C.氢气和氯气反应生成2 mol氯化氢气体,反应的△H=-183kJ/mol
D.氢气和氯气反应生成1 mol氯化氢气体,反应的△H=-183kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2均为正值):
H2(g)+Cl2(g)  2HCl(g)+Q1
2HCl(g)+Q1
H2(g)+Br2(g)  2HBr(g)+Q2
2HBr(g)+Q2
有关上述反应的叙述正确的是( )
A.Q1>Q2
B.生成物总能量均高于反应物总能量
C.生成1 mol HCl气体时放出Q1热量
D.1 mol HBr(g)具有的能量大于1 mol HBr(l)具有的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
某钠盐溶液中可能含有 等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
①用pH计测得溶液pH大于7
②加入盐酸,产生有色刺激性气体
③加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体
④加足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色。
⑤加足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)溶液,再滴加KSCN溶液,显红色
该同学最终确定在上述六种离子中公含 三种阴离子。
三种阴离子。
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
A. ①②④⑤ B. ③④ C. ③④⑤ D. ②③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com