
�����ʽṹ�����ʡ�
�Ե�����(GaN)Ϊ�����ĵ������뵼�����Ŀǰ�ѳ�Ϊȫ��뵼���о���ǰ�غ��ȵ㡣�ش��������⣺
��1����ΪԪ�����ڱ���31��Ԫ�أ���ԭ�Ӽ۲�����Ų�ͼΪ___________��
��2�������������е�һ����������Ԫ����________����Ԫ�ط��ţ���ͬ���������������е縺������Ԫ����____________________��
��3����ͳ�ĵ������Ʊ������Dz���GaCl3��NH3��һ�������·�Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ______________��
��4������������ʯ�������Ƶľ���ṹ���������е�ԭ������ԭ��֮����____���ϣ�����������_______���塣
��5����ͼ�ǵ����صľ���ģ�ͣ�
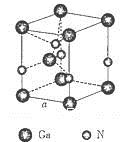
�ٵ���������ԭ�ӵ��ӻ���ʽΪ__________����ԭ�ӵ���λ��Ϊ___________��
�ڵ�����Ϊ���������������ص��ܶ�Ϊd g/cm3���г����㵪���ؾ����߳�a�ı���ʽ��a=_______cm��
��1��
��2��N ��B
��3��GaCl3+NH3=GaN+3HCl
��4�����ۼ� ԭ��
��5����sp2 4 �� 
����������1����ԭ������Ϊ31���������������Ų�ʽΪ��1s22s22p63s23p63d104s24p1����������Ϊ�۵��ӣ��۵����Ų�ʽΪ��4s24p1����4s�����һ�������෴�ĵ��ӣ�4p���ֻ��һ�����ӣ��ʴ�Ϊ�� ��
��
��2����һ������ͬ������ϵ��£�Խ��ԽС��NԪ��Ϊ�������������Ԫ�أ���һ��������縺�Դ��ϵ��£�Խ��ԽС�����������������Ԫ��ΪB��
��3����Ӧ��ΪNH3��GaCl3��������ΪGaN�������жϳ���һ�ֲ���ΪHCl������ԭ���غ�д����ѧ����ʽ���ʴ�Ϊ��GaCl3+NH3=GaN+3HCl��
��4�����ڵ���������ʯ�������Ƶľ���ṹ�����Ե�����Ϊԭ�Ӿ��壬ԭ��֮���Թ��ۼ������һ��
��5���ٸ��ݾ������Կ���Ga�������ڵ�����N�γɹ��ۼ�����Ga�γ��������ۼ��������ӻ�����Ϊsp2�ӻ����۲쾧���ṹ����Nԭ����Χ���������Ga��ĿΪ4������λ��Ϊ4��
��GaN�����У�Gaλ�ڶ�������ģ����Ժ���Ga��Ϊ��8�� +1=2��Nԭ��λ��������ģ�����N��Ϊ��4��
+1=2��Nԭ��λ��������ģ�����N��Ϊ��4�� +1=2��GaN�����к�������GaN�������߳�Ϊ
+1=2��GaN�����к�������GaN�������߳�Ϊ


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��15 ���ͣ������
����ѧ�뼼����
��Ƴ���ͭ��ˮ�к���CN-��Cr2O72-���ӣ���Ҫ������������ŷš��ó��ⶨ�������̽��з�ˮ�������ش��������⣺

��1������������ˮ��������Ҫʹ�õķ�����______��
��2�����з�Ӧ��������ų����÷�Ӧ�����ӷ���ʽΪ ��
��3��������У�ÿ����0.4mol Cr2O72-ʱת�Ƶ���2.4mol���÷�Ӧ���ӷ���ʽΪ ��
��4��ȡ��������ˮ�����Թ��У�����NaOH��Һ���۲쵽����ɫ�������ɣ��ټ�Na2S��Һ�� ��ɫ����ת���ɺ�ɫ��������ʹ�û�ѧ��������ֽ��Ͳ����������ԭ�� ��
��5��Ŀǰ��������Cr2O72-��ˮ������������巨���÷������ˮ�м���FeSO4��7H2O��Cr2O72-��ԭ��Cr3+������pH��Fe��Crת�����൱��FeII[FeCr]O4���������壬�������ֱ�ʾԪ�ؼ�̬���ij���������1mol Cr2O72-�������a mol FeSO4?7H2O�����н�����ȷ����_______��
A��x =0.5 ��a =8 B��x =0.5�� a = 10
C��x = 1.5 ��a =8 D��x = 1.5 ��a = 10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��14 ���ͣ�ѡ����
����ѡ���е�ͼ������ʾ����������Ӧ��Ӧ���ϵ���(a��b��c��d������0)

A��4NH3(g)��5O2(g)  4NO(g)��6H2O(g) ��H����a kJ��mol��1
4NO(g)��6H2O(g) ��H����a kJ��mol��1
B��N2(g)��3H2(g)  2NH3(g)����H����b kJ��mol��1
2NH3(g)����H����b kJ��mol��1
C��2SO3(g)  2SO2(g)��O2(g)����H����c kJ��mol��1
2SO2(g)��O2(g)����H����c kJ��mol��1
D��2N2O5(g)  4NO2(g)��O2(g) ��H����d kJ��mol��1
4NO2(g)��O2(g) ��H����d kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��13 ���ͣ�ѡ����
�����±���CuFeS2�ķ�Ӧ֮һΪ2CuFeS2+7O2=CuSO4+CuO+Fe2O3+3SO2�����й��ڸ÷�Ӧ��������ȷ����
A��CuFeS2����Ļ��ϼ�Ϊ-1
B��CuFeS2������ԭ��Ӧ
C��1 mol CuFeS2��ȫ��Ӧת��13 mol����
D��CuSO4��SO2��������������ǻ�ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��13 ���ͣ�ѡ����
��ͼ�ǽ�SO2ת��Ϊ��Ҫ�Ļ���ԭ��H2SO4��ԭ��ʾ��ͼ������˵������ȷ����

A����װ�ý���ѧ��ת��Ϊ����
B������b����O2������ԭ��Ӧ���丽��������ǿ
C������a����ķ�Ӧ��SO2��2H2O��2e��===SO42-��4H��
D�����õ�������Ũ����Ϊ49%���������ϲμӷ�Ӧ��SO2������H2O��������Ϊ8��15
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��12 ���ͣ�ѡ����
���и������ӿ��ܴ����������
A����ʹ�⻯�ص�����ֽ��������Һ��Na����NH��S2����Br��
B����pH��ֽ���ɫ����Һ��Fe2+��S2O��SO42����Na+
C��ˮ�������c(H��) ?c(OH��) =10��28����Һ��Na����S2����NO3�� ��SO32 ��
D����ʹKSCN�Ժ�ɫ����Һ��Na����NH4����AlO��CO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��12 ���ͣ�ѡ����
����ʵ�鲽����ʵ����ʵ����Ӧ���۽�����ȷ����
ѡ�� | ʵ�鲽����ʵ����ʵ | ���۽��� |
A | Mg(OH)2��Al(OH)3������м���NaOH��Һ��Al(OH)3�ܽ��Mg(OH)2û���ܽ� | Mg(OH)2Ksp��Al(OH)3��С |
B | ZnS���ܽ���ϡ�����У�CuS�����ܽ���ϡ������ | CuS��Ksp��ZnS��С |
C | ������NH3��BaCl2��Һ��ͨ��CO2���а�ɫ�������� | NH3�ڷ�Ӧ�������� |
D | ���ʹ費����Ũ�����Ũ���� | �豻ǿ��������ۻ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��11 ���ͣ�ѡ����
����˵��һ����ȷ���ǣ�NA��ʾ�����ӵ�������
A��������4.4gN2O���״����2.24LCH4������0.1NA������
B��78g�����أ�K����ȫת��Ϊ�������أ�KO2��ʱ��ת�Ƶ�����Ϊ4NA
C��0.1mol/Lϡ�����У�H+��ĿΪ0.1NA
D��60g�������辧���У���S��O����ĿΪ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ�� ���ͣ������
���Ĺ̶�������;��������̵�����Ȼ�̵���ҵ�̵����������¡��˹��̵������о��������ڳ��¡���ѹ�����������£�N2�ڴ���(��������Fe2O3��TiO2)������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����һ���о�NH3���������¶ȵĹ�ϵ������ʵ�����ݼ��±�(���ա�N2ѹ��1.0��105 Pa����Ӧʱ��1 h)��
T/K | 303 | 313 | 323 | 353 |
NH3������/(10��6 mol) | 4.8 | 5.9 | 6.0 | 2.0 |
��Ӧ�Ļ�ѧ����ʽ��2N2(g)��6H2O(l)  4NH3(g)��3O2(g)��H��a kJ��mol��1
4NH3(g)��3O2(g)��H��a kJ��mol��1
�ش��������⣺
(1)�˺ϳɷ�Ӧ��a________0����S________0��(�����������������)
(2)��֪��N2(g)��3H2(g)  2NH3(g)����H����92 .4 kJ��mol��1
2NH3(g)����H����92 .4 kJ��mol��1
2H2(g)��O2(g) ===2H2O(l)�� ��H ����571.6 kJ��mol��1
��2N2(g)��6H2O(l)===4NH3(g)��3O2 (g)����H��________kJ��mol��1
(3)��323 K��353 K�����������������ٵĿ���ԭ��_________________��
(4)��ҵ�ϳɰ��ķ�ӦΪN2(g)��3H2(g) 2NH3(g)����H����92 .4 kJ��mol��1 ���ֱ��о���T1��T2��T3(T1<T2<T3)�����¶��ºϳɰ����Ĺ��ɡ���ͼ�����������¶��²�ͬ��H2��N2����ʼ��ɱ�(��ʼʱN2�����ʵ�����Ϊ1 mol)��N2ƽ��ת���ʵĹ�ϵ����ش�
2NH3(g)����H����92 .4 kJ��mol��1 ���ֱ��о���T1��T2��T3(T1<T2<T3)�����¶��ºϳɰ����Ĺ��ɡ���ͼ�����������¶��²�ͬ��H2��N2����ʼ��ɱ�(��ʼʱN2�����ʵ�����Ϊ1 mol)��N2ƽ��ת���ʵĹ�ϵ����ش�

�������������¶��У�����X��Ӧ���¶���________��
��a��b��c����H2��ת������С����________�㡢ת����������________�㡣
�����ݻ�Ϊ1.0 L���ܱ������г���0.30 mol N2(g)��0.80 mol H2(g)����Ӧ��һ�������´ﵽƽ��ʱ��NH3�����ʵ�������(NH3�����ʵ����뷴Ӧ��ϵ���ܵ����ʵ���֮��)Ϊ4/7���������·�Ӧ2NH3(g)  N2(g)��3H2(g)��ƽ�ⳣ��Ϊ________ ��
N2(g)��3H2(g)��ƽ�ⳣ��Ϊ________ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com