


科目:高中化学 来源:不详 题型:填空题

| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀 时的pH | 1.9 | 7.0 | — | — | 4.7 | — |
| 沉淀完全 时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaH中H的化合价为+1价,是氧化剂 |
| B.在该反应中H2O 为还原剂 |
| C.在该反应中NaH 为还原剂 |
D.该反应中电子转移的方向和数目可以表示为: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2S+2HNO3=S↓+2NO2↑+2H2O |
| B.CuO+2HNO3=Cu(NO3)2+H2O |
C.4HNO3 4NO2↑+O2↑+2H2O 4NO2↑+O2↑+2H2O |
| D.3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 离子在一定条件下可以把Mn2+离子氧化为
离子在一定条件下可以把Mn2+离子氧化为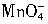 ,若反应后
,若反应后 离子变为
离子变为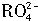 离子,
离子,| A.1 | B.2 | C.3 | D.4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaCl | B.KNO3 | C.K2SO4 | D.Na2CO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.ZnCl2既是氧化产物又是还原产物 |
| B.ZnI2既是氧化产物又是还原产物 |
| C.在ICl与水反应中,ICl是氧化剂、H2O是还原剂 |
| D.ICl与水反应是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com