
| A. | HCN的电离方程式:HCN?H++CN- | |
| B. | NaCN是一种弱电解质 | |
| C. | NaCN溶液中一定存在:c(Na+)>c(CN-) | |
| D. | 0.1mol•L-1NaCN溶液中:c(CN-)+c(HCN)=0.1mol•L-1 |
分析 某浓度NaCN(氰化钠)溶液pH=11,溶液呈碱性,说明NaCN是强碱弱酸盐,所以HCN是弱电解质,由此分析解答.
解答 解:A、HCN是弱电解,电离用可逆符号,所以HCN的电离方程式:HCN?H++CN-,故A正确;
B、NaCN是盐,是强电解质,故B错误;
C、NaCN是强碱弱酸盐,酸根离子水解,所以NaCN溶液中一定存在:c(Na+)>c(CN-),故C正确;
D、根据物料守恒,0.1mol•L-1NaCN溶液中:c(CN-)+c(HCN)=c(Na+)=0.1mol•L-1,故D正确;
故选B.
点评 本题考查离子浓度大小比较,题目难度中等,注意把握离子浓度大小的方法,解题时注意守恒思想的应用.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 甲烷燃烧 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | 铝片与盐酸反应 | D. | 氧化钙与水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.15 mol•(L•s)-1 | B. | v(B)=0.6 mol•(L•s)-1 | ||
| C. | v(C)=0.6 mol•(L•s)-1 | D. | v(D)=0.2 mol•(L•s)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液使红色石蕊试纸变蓝,结论:溶液显碱性 | |
| B. | 无色溶液焰色反应呈黄色,结论:试液是钠盐溶液 | |
| C. | 无色溶液加入Na2CO3溶液产生白色沉淀,结论:溶液中含Ca(OH)2 | |
| D. | 向溶液中加入BaCl2溶液,生成白色沉淀,再加稀HCl,沉淀不溶解,可断定含有SO42ˉ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
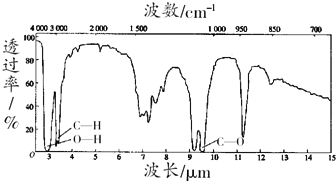
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可能是不同的分子与原子 | B. | 可能是不同的离子 | ||
| C. | 可能是一种离子和一种分子 | D. | 可能是某位素的同位素原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaNO2是还原剂 | |
| B. | NH4Cl中N元素被还原 | |
| C. | 生成1 mol N2时转移6 mol 电子 | |
| D. | 氧化剂和还原剂的物质的量之比是1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
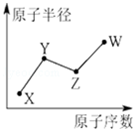 U、V、W、X、Y、Z是六种常见的短周期主族元素,其中W、X、Y、Z原子半径随原子序数的变化如图所示:
U、V、W、X、Y、Z是六种常见的短周期主族元素,其中W、X、Y、Z原子半径随原子序数的变化如图所示: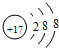 ;
;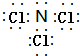 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com