
| A. | Fe$→_{点燃}^{O_{2}}$Fe2O3$\stackrel{H_{2}SO_{4}}{→}$Fe2(SO4)3 | |
| B. | 饱和食盐水$\stackrel{NH_{3},CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| C. | 海水$\stackrel{熟石灰}{→}$Mg(OH)2$\stackrel{△}{→}$MgO$\stackrel{电解}{→}$Mg | |
| D. | NH3$→_{催化剂,△}^{O_{2}}$N2$\stackrel{H_{2}O+O_{2}}{→}$HNO3 |
分析 A.铁和氧气点燃反应生成四氧化三铁,四氧化三铁和硫酸反应生成硫酸铁、硫酸亚铁;
B.饱和食盐水中通入氨气、二氧化碳会发生反应生成碳酸氢钠晶体和氯化铵溶液,过滤得到碳酸氢钠分解生成碳酸钠;
C.海水中含镁离子,加入熟石灰反应生成氢氧化镁沉淀,氢氧化镁受热分解生成氧化镁,氧化镁熔点高不能电解氧化镁制备镁,应是电解熔融氯化镁得到镁;
D.氨气氧化得到氮气,氮气和氧气在水溶液中不反应.
解答 解:A.铁和氧气点燃反应生成四氧化三铁,铁在纯净氧气中点燃不能一步生成氧化铁,四氧化三铁和硫酸反应生成硫酸铁、硫酸亚铁,故A错误;
B.饱和食盐水中通入氨气、二氧化碳会发生反应生成碳酸氢钠晶体和氯化铵溶液,NH3+CO2+NaCl+H2O=NaHCO3↓+NH4Cl,过滤得到碳酸氢钠分解生成碳酸钠,能一步实现,故B正确;
C.海水中含镁离子,加入熟石灰反应生成氢氧化镁沉淀,氢氧化镁受热分解生成氧化镁,氧化镁熔点高不能电解氧化镁制备镁,应是电解熔融氯化镁得到镁,不能一步实现各步转化,故C错误;
D.氨气氧化得到氮气,氮气和氧气在水溶液中不反应,不能生成硝酸,应是氨气催化氧化生成一氧化氮,一氧化氮和氧气水中全部转化为硝酸,故D错误;
故选B.
点评 本题考查了铁、镁、氨气等物质性质和海水资源的利用,主要是反应条件和产物的判断,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
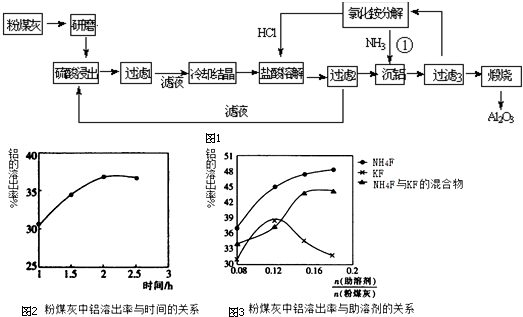
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
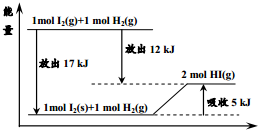
| A. | 1mol固态碘与1molH2化合生成2molHI气体时,需要吸收5kJ的能量 | |
| B. | 2molHI气体分解生成1mol碘蒸气与1molH2时需要吸收12kJ的能量 | |
| C. | 1mol固态碘变为1mol碘蒸气时需要吸收17kJ的能量 | |
| D. | 碘蒸气与H2生成HI气体的反应是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为8、中子数为10的氧原子:${\;}_{16}^{8}$O | |
| B. | 氧原子的结构示意图: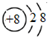 | |
| C. | 过氧化氢的电子式: | |
| D. | 乙酸甲酯的结构简式HCOOC2H5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向1mL1%的NaOH溶液中加入2mL2%的CuSO4溶液,振荡后再加入0.5mL有机物X,加热后未出现砖红色沉淀,说明X结构中不含有醛基 | |
| B. | 室温下向苯和少量苯酚的混合溶液中加入适量浓溴水,振荡、静置后过滤,可除去苯中少量苯酚 | |
| C. | 向无色的淀粉KI溶液中滴加少量氯水,溶液变成蓝色,说明氧化性:Cl2>I2 | |
| D. | 向含酚酞的氢氧化钠溶液中加入少量30%H2O2溶液,红色褪去,向褪色后的溶液再补加NaOH溶液,不显红色,说明H2O2因显酸性而使溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 装置 | 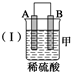 | 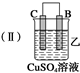 | 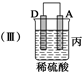 |
| 现象 | 二价金属A 不断溶解 | C的质 量增加 | A上有气 体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L CH3COOH溶液中:c(CH3COO-)+c(CH3COOH)=0.1mol/L | |
| B. | 将Al2(SO4)3溶液蒸干,灼烧得Al2O3 | |
| C. | 配制FeCl3溶液,应加少量盐酸 | |
| D. | Na2S溶液中:c(OH-)═c(H+)+c(HS-)+2c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,反应的化学方程式为
,反应的化学方程式为 +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$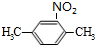 +H2O.
+H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com