
25 ℃时,用浓度为0.100 0 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.100 0 mol·L-1的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是( )
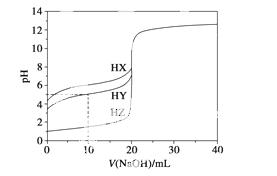
A.在相同温度下,同浓度的三种酸 溶液的导电能力顺序:HZ<HY<HX
溶液的导电能力顺序:HZ<HY<HX
B.根据滴定曲线,可得Ka(HY)≈10-5
C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:
c(X-)>c(Y-)>c(OH-)>c(H+)
D.HY与HZ混合,达到平衡时c(H+)=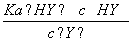 +c(Z-)+c(OH-)
+c(Z-)+c(OH-)
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
活性ZnO在橡胶、塑料、涂料工业中有重要应用,一种由粗ZnO(含FeO、CuO)制备
活性ZnO的流程如下(已知:碱式碳酸锌经焙烧可制得活性ZnO):
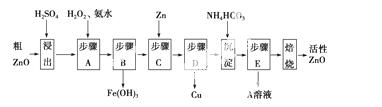
已知:几种离子生成氢氧化物沉淀时的pH如表:
| 待沉淀离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
| 开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
| 完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
请回答下列问题:
(1)步骤A加H2O2发生反应的离子方程式是_____________________________________
________________________________________________________________________,
该步骤需控制溶液pH的范围是_____________________________________________。
(2)A溶液中主要含有的溶质是____________。
(3)碱式碳酸锌经焙烧制得活性ZnO的反应ΔH>0,该反应能自发进 行的原因是ΔS________(选填“=”、“>”或“<”)0。
行的原因是ΔS________(选填“=”、“>”或“<”)0。
(4)若经处理后的废水pH=8,此时Zn2+的浓度为________mg/L(常温下,Ksp[Zn(OH)2]=1.2×10-17)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.难溶电解质作比较时,Ksp小的,溶解度一定小
B.Ksp大小取决于难溶电解质的量,所以离子浓度改变时,沉淀溶解平衡会发生移动
C.所谓沉淀完全就 是用沉淀剂将溶液中某一离子完全除去
是用沉淀剂将溶液中某一离子完全除去
D.温度一定,当溶液中Ag+和Cl-浓度的乘积等于Ksp时,溶液为AgCl的饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
在25 ℃时,将pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合后,下列关系 式中正确的是 ( )
式中正确的是 ( )
A.c(Na+)=c(CH3COO-)+c(CH3COOH)
B.c(H+)=c(CH3COO-)+c(OH-)
C.c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
A.0.1 mol·L-1CH3COONa溶液与0.1 mol·L-1HCl溶液等体积混合:
c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-)
B.0.1 mol·L-1NH4Cl溶液与0.1 mol·L-1氨水等体积混合(pH>7):
c(NH3·H2O)>c(NH )>c(Cl-)>c(OH-)
)>c(Cl-)>c(OH-)
C.0.1 mol·L-1Na2CO3溶液与0.1 mol·L -1NaHCO3溶液等体积混合:
-1NaHCO3溶液等体积混合:
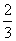 c(Na+)=c(CO
c(Na+)=c(CO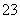 )+c(HCO
)+c(HCO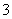 )+c(H2CO3)
)+c(H2CO3)
D.0.1 mol·L-1Na2C2O4溶液与0.1 mol·L-1HCl溶液等体积混合(H2C2O4为二元弱酸):
2c(C2O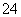 )+c(HC2O
)+c(HC2O )+c(OH-)=c(Na+)+c(H+)
)+c(OH-)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,浓度均为0.1 mol·L-1的三种溶液:①醋酸 ②氢氧化钠 ③醋酸钠,下列说法不正确的是( )
A.c(CH3COO-):③>①
B.水电离出的c(OH-):②>①
C.①和②等体积混合后的溶液:c(OH-)=c(H+)+c(CH3COOH)
D.①和③等体积混合后的溶液:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸是二元中强酸,测得0.01 mol·L-1的草酸氢钠溶液显酸性。常温下,向10 mL 0.01 mol·L-1NaHC2O4溶液中滴加0.01 mol·L-1NaOH溶液,随着NaOH溶液体积的增加,下列说法正确的是 ( )
A.V(NaOH)=0 mL时,c(Na+)>c(H+)>c(HC2O )>c(C2O
)>c(C2O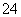 )>c(OH-)
)>c(OH-)
B.V(NaOH)=5 mL时,c(Na+)=c(C2O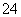 )+c(HC2O
)+c(HC2O )+c(H2C2O4)
)+c(H2C2O4)
C.V(NaOH)=10 mL时,c(Na+)=c(HC2O )+2c(C2O
)+2c(C2O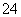 )
)
D.V(NaOH)>10 mL时,c(Na+)>c(C2O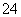 )>c(HC2O
)>c(HC2O )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,10mL0.40mol/L H2O2溶液发生催化分解。不同时刻 测定生成O2的体积(已折算为标准状况)如下表。
测定生成O2的体积(已折算为标准状况)如下表。
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L·min)
B.6~10min的平均反应速率:v(H2O2)<3.3×10-2mol/(L·min)
C.反应至6min时,c(H2O2)=0.3mol/L
D.反应至6min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,RO3﹣与R﹣可发生反应:RO3﹣+5R﹣+6H+═3R2+3H2O,下列关于R元素的叙述中,正确的是( )
|
| A. | 元素R位于周期表中第ⅤA族 |
|
| B. | RO3﹣中的R只能被还原 |
|
| C. | R2在常温常压下一定是气体 |
|
| D. | 若1molRO3﹣参与该反应,则转移的电子的物质的量为5mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com