
| A. | ①②⑤⑥ | B. | ⑤③④⑥ | C. | ⑤②③⑧ | D. | ②③④⑦ |
分析  发生消去反应所生产的环己烯(发生反应为
发生消去反应所生产的环己烯(发生反应为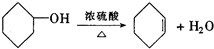 ),环己烯与臭氧(O3)反应,再在锌粉存在下水解生成OHCCH2CH2CH2CH2CHO(发生反应为
),环己烯与臭氧(O3)反应,再在锌粉存在下水解生成OHCCH2CH2CH2CH2CHO(发生反应为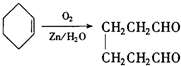 ),与新制氢氧化铜反应生成HOOCCH2CH2CH2CH2COOH(发生反应为
),与新制氢氧化铜反应生成HOOCCH2CH2CH2CH2COOH(发生反应为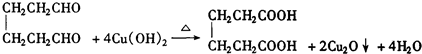 ),OHCCH2CH2CH2CH2CHO发生还原反应生成HOH2CCH2CH2CH2CH2CH2OH,最后HOOCCH2CH2CH2CH2COOH与HOH2CCH2CH2CH2CH2CH2OH发生酯化反应生成己二酸己二酯,以此来解答.
),OHCCH2CH2CH2CH2CHO发生还原反应生成HOH2CCH2CH2CH2CH2CH2OH,最后HOOCCH2CH2CH2CH2COOH与HOH2CCH2CH2CH2CH2CH2OH发生酯化反应生成己二酸己二酯,以此来解答.
解答 解:由环己醇制取己二酸己二酯,最简单的流程途径顺序为⑤消去反应(制环己烯)、③氧化反应(制备己二醛和己二酸)、④还原反应(制备己二醇)、⑥酯化反应(制备己二酸己二酯),
故选B.
点评 本题考查有机物的合成,为高频考点,把握有机物中官能团变化、有机反应为解答的关键,侧重分析与推断能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ③④⑤ | B. | ④⑤ | C. | ④⑤⑦ | D. | ③④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=12的Ba(OH)2 | B. | pH=12的氨水 | ||
| C. | 0.02mol•L-1的NaOH | D. | 0.01mol•L-1的BaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
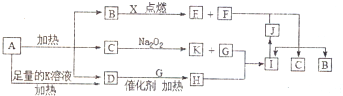
 ,写出F的一种同素异形体金刚石(C60、石墨等),D分子的空间构型为三角锥形.
,写出F的一种同素异形体金刚石(C60、石墨等),D分子的空间构型为三角锥形.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点得到小:HI>HBr>HCl>HF | |
| B. | 干冰升华克服的是分子间作用力 | |
| C. | HF稳定性很强,是因为分子间能形成氢键 | |
| D. | 冰、水和水蒸气中都存在氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 二者的pH仍然相等且均为5 | B. | 盐酸的pH大 | ||
| C. | 醋酸的pH大 | D. | 盐酸的pH为5,醋酸的pH在3~5之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
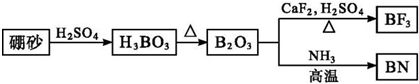
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com