
”¾ĢāÄæ”æĮņĖįŹŌ¼ĮĘæ±źĒ©ÉĻµÄÄŚČŻČēĶ¼ĖłŹ¾:

£Ø1£©øĆĮņĖįµÄĪļÖŹµÄĮæÅØ¶ČŹĒ____________mol/L£»
£Ø2£©Ä³»ÆѧŠĖȤŠ”×é½ųŠŠĮņĖįŠŌÖŹµÄŹµŃéĢ½¾æŹ±,ŠčŅŖ240mL 4.6mol£®L-1µÄĻ”ĮņĖį,ŌņÅäÖĘĻ”ĮņĖįŹ±ŠčŅŖČ”____mLµÄøĆĮņĖį;ÅäÖĘŹ±ŠčŃ”ÓƵÄŅĒĘ÷Ö÷ŅŖÓŠĮæĶ²”¢ÉÕ±”¢²£Į§°ō”¢_______”¢½ŗĶ·µĪ¹Ü£ØŌŚŗįĻßÉĻĢīŠ“ĖłČ±ŅĒĘ÷µÄĆū³Ę£©”£
£Ø3£©ÅäÖĘ¹ż³ĢÖŠ,ĻĀĮŠ²Ł×÷»įŹ¹ÅäÖʵÄĻ”ĮņĖįČÜŅŗÅضČĘ«øߵďĒ____£ØĢīŠņŗÅ£©”£
¢ŁĮæČ”ÅØĮņĖįµÄĮæĶ²ÓĆÕōĮóĖ®Ļ“µÓ2~3“Ī,²¢°ŃĻ“µÓŅŗ×ŖČėČŻĮæĘæ
¢ŚČŻĮæĘæŹ¹ÓĆŹ±Ī“øÉŌļ
¢ŪČܽāŗóĪ“¾ĄäČ“¾ĶŅĘŅŗ²¢¶ØČŻ
¢Ü¶ØČŻŹ±²»Š”ŠÄÓŠÉŁĮæÕōĮóĖ®µĪµ½ĘæĶā
¢Ż¶ØČŻŗó¾Õńµ“”¢Ņ”ŌČ”¢¾²ÖĆ,·¢ĻÖŅŗĆęµĶÓŚæĢ¶ČĻߣ¬ŌŁ¼ÓÕōĮóĖ®²¹ÖĮæĢ¶ČĻß
”¾“š°ø”æ18£®462£®5250 mLČŻĮæĘæ¢Ł¢Ū
”¾½āĪö”æ
(1).øĆĮņĖįµÄĪļÖŹµÄĮæÅØ¶ČŹĒ£ŗc(H2SO4)=![]() =18.4mol/L£¬¹Ź“š°øĪŖ£ŗ18.4£»
=18.4mol/L£¬¹Ź“š°øĪŖ£ŗ18.4£»
(2).ŹµŃéŹŅĪŽ240mL¹ęøńµÄČŻĮæĘ棬ĖłŅŌӦєÓĆ250mL¹ęøńµÄČŻĮæĘæ½ųŠŠÅäÖĘ£¬ÉčŠčŅŖÅØĮņĖįµÄĢå»żĪŖa mL£¬øł¾ŻĻ”ŹĶ¶ØĀÉÓŠ£ŗa ”Į10£3L”Į18.4mol/L=0.25L”Į4.6mol/L£¬½āµĆa=62.5mL£»ÅäÖĘøĆĮņĖįČÜŅŗŹ±ŠčŅŖµÄŅĒĘ÷Ö÷ŅŖÓŠĮæĶ²”¢ÉÕ±”¢²£Į§°ō”¢250mLČŻĮæĘ攢½ŗĶ·µĪ¹ÜµČ£¬¹Ź“š°øĪŖ£ŗ62.5£»250mLČŻĮæĘ棻
(3). ¢Ł. ĮæČ”ÅØĮņĖįµÄĮæĶ²ÓĆÕōĮóĖ®Ļ“µÓ2~3“Ī£¬²¢°ŃĻ“µÓŅŗ×ŖČėČŻĮæĘæÖŠ£¬»įŹ¹ČÜÖŹĘ«¶ą£¬ÅäÖʵÄČÜŅŗÅضČĘ«øߣ»
¢Ś.Ņņ¶ØČŻŹ±ŅŖ¼ÓĖ®£¬ĖłŅŌČŻĮæĘæŹ¹ÓĆŹ±Ī“øÉŌļ¶ŌÅäÖʵÄČÜŅŗÅضČĪŽÓ°Ļģ£»
¢Ū.ÅØĮņĖįĻ”ŹĶ·ÅČČ£¬ČܽāŗóĪ“¾ĄäČ“¾ĶŅĘŅŗ²¢¶ØČŻ£¬»įŹ¹ČÜŅŗµÄĢå»żĘ«Š”£¬ÅäÖʵÄČÜŅŗÅضČĘ«øߣ»
¢Ü.¶ØČŻŹ±²»Š”ŠÄÓŠÉŁĮæÕōĮóĖ®µĪµ½ĘæĶā£¬¶ŌÅäÖʵÄČÜŅŗÅضČĪŽÓ°Ļģ£»
¢Ż.¶ØČŻŗó¾Õńµ“”¢Ņ”ŌČ”¢¾²ÖĆ£¬·¢ĻÖŅŗĆęµĶÓŚæĢ¶ČĻߣ¬ĪŖÕż³£Ēéæö£¬ČōŌŁ¼ÓÕōĮóĖ®²¹ÖĮæĢ¶ČĻß»įŹ¹ČÜŅŗĢå»żĘ«“ó£¬ÅäÖʵÄČÜŅŗÅضČĘ«µĶ£¬×ŪÉĻĖłŹö£¬»įŹ¹ÅäÖʵÄČÜŅŗÅضČĘ«øߵďĒ¢Ł¢Ū£¬¹Ź“š°øĪŖ£ŗ¢Ł¢Ū”£


 ÓŵČÉśĢāæāĻµĮŠ“š°ø
ÓŵČÉśĢāæāĻµĮŠ“š°ø 53ĢģĢģĮ·ĻµĮŠ“š°ø
53ĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓĆ0.1000 mol”¤L£1KMnO4ĖįŠŌČÜŅŗµĪ¶ØĪ“ÖŖÅØ¶ČµÄĪŽÉ«H2C2O4ČÜŅŗ£¬·“Ó¦Ąė×Ó·½³ĢŹ½ŹĒ£ŗ2MnO4££«5H2C2O4£«6H+ = 2Mn2+£«10CO2”ü£«8H2O
ĢīæÕĶź³ÉĪŹĢā£ŗ
£Ø1£©øƵĪ¶ØŹµŃéĖłŠčµÄ²£Į§ŅĒĘ÷ÓŠ______________”££ØĢī×ÖÄø£©
A£®ĖįŹ½µĪ¶Ø¹ÜB£®¼īŹ½µĪ¶Ø¹Ü C£®ĮæĶ² D£®×¶ŠĪĘæ E£®Ģś¼ÜĢØF£®µĪ¶Ø¹Ü¼ŠG£®ÉÕ±H£®°×Ö½ I£®Ā©¶·
£Ø2£©²»ÓĆ________(Ģī”°Ėį”±»ņ”°¼ī”±)Ź½µĪ¶Ø¹ÜŹ¢·ÅøßĆĢĖį¼ŲČÜŅŗ”£ŹŌ·ÖĪöŌŅņ___________________________________________”£
£Ø3£©µĪ¶ØÖÕµćµÄĻÖĻóĪŖ___________________________________”£
£Ø4£©ČōµĪ¶ØæŖŹ¼ŗĶ½įŹųŹ±£¬µĪ¶Ø¹ÜÖŠµÄŅŗĆęČēĶ¼ĖłŹ¾£¬ŌņĘšŹ¼¶ĮŹżĪŖ________mL£¬ÖÕµć¶ĮŹżĪŖ________mL”£
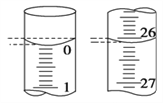
£Ø5£©Ä³Ń§Éśøł¾Ż3“ĪŹµŃé·Ö±š¼ĒĀ¼ÓŠ¹ŲŹż¾ŻČēĻĀ±ķ£ŗ
µĪ¶Ø “ĪŹż | “ż²āH2C2O4ČÜŅŗµÄĢå»ż/mL | 0.1000 mol/L KMnO4µÄĢå»ż£ØmL£© | ||
µĪ¶ØĒ°æĢ¶Č | µĪ¶ØŗóæĢ¶Č | ČÜŅŗĢå»ż/mL | ||
µŚŅ»“Ī | 25.00 | 0.00 | 26.11 | 26.11 |
µŚ¶ž“Ī | 25.00 | 1.56 | 30.30 | 28.74 |
µŚČż“Ī | 25.00 | 0.22 | 26.31 | 26.09 |
ŅĄ¾ŻÉĻ±ķŹż¾ŻĮŠŹ½¼ĘĖćøĆH2C2O4ČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ_______________”£
£Ø6£©ĻĀĮŠ²Ł×÷ÖŠæÉÄÜŹ¹²ā¶Ø½į¹ūĘ«µĶµÄŹĒ___________(Ģī×ÖÄø)”£
A£®ĖįŹ½µĪ¶Ø¹ÜĪ“ÓƱź×¼ŅŗČóĻ“¾ĶÖ±½Ó×¢ČėKMnO4±ź×¼Ņŗ
B£®µĪ¶ØĒ°Ź¢·Å²ŻĖįČÜŅŗµÄ׶ŠĪĘæÓĆÕōĮóĖ®Ļ“¾»ŗóƻӊøÉŌļ
C£®ĖįŹ½µĪ¶Ø¹Ü¼ā×ģ²æ·ÖŌŚµĪ¶ØĒ°Ć»ÓŠĘųÅŻ£¬µĪ¶ØŗóÓŠĘųÅŻ
D£®¶ĮČ”KMnO4±ź×¼ŅŗŹ±£¬æŖŹ¼ŃöŹÓ¶ĮŹż£¬µĪ¶Ø½įŹųŹ±ø©ŹÓ¶ĮŹż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
A.±ź×¼×“æöĻĀ£¬22.4LH2OĖłŗ¬µÄ·Ö×ÓŹżĪŖNA
B.14gµŖĘųĖłŗ¬µÄµŖŌ×ÓŹżĪŖNA
C.±ź×¼×“æöĻĀ£¬22.4LNH3Ėłŗ¬µÄµē×ÓŹżĪŖNA
D.1molNaÓėCl2·“Ó¦×ŖŅʵē×ÓŹżĪŖ2NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĢõ¼žĻĀ£¬ŌŚĢå»żĪŖV LµÄĆܱÕČŻĘ÷ÖŠ·¢Éś»Æѧ·“Ó¦CO(g)£«2H2(g) ![]() CH3OH(g)£¬æÉÅŠ¶ĻøĆæÉÄę·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ£Ø £©
CH3OH(g)£¬æÉÅŠ¶ĻøĆæÉÄę·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ£Ø £©
A. vÉś³É(CH3OH)£½vĻūŗÄ(CO) B. CO”¢H2”¢CH3OHµÄÅØ¶Č±ČĪŖ1:2:1
C. »ģŗĻĘųĢåµÄĆÜ¶Č²»ŌŁøıä D. »ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»ŌŁøıä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠ£¬²»ŹōÓŚ½šŹō²ÄĮĻµÄŹĒ( )
A.»ĘĶB.Ó²ĀĮC.²»ŠāøÖD.½šøÕŹÆ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗCO(g)£«H2O(g)![]() CO2(g)£«H2(g)””¦¤H£½£41 kJ”¤mol£1”£ĻąĶ¬ĪĀ¶ČĻĀ£¬ŌŚČŻ»żĻąĶ¬µÄĮ½øöŗćĪĀĆܱÕČŻĘ÷ÖŠ£¬¼ÓČėŅ»¶ØĮæµÄ·“Ó¦Īļ·¢Éś·“Ó¦”£Ļą¹ŲŹż¾ŻČēĻĀ£ŗ
CO2(g)£«H2(g)””¦¤H£½£41 kJ”¤mol£1”£ĻąĶ¬ĪĀ¶ČĻĀ£¬ŌŚČŻ»żĻąĶ¬µÄĮ½øöŗćĪĀĆܱÕČŻĘ÷ÖŠ£¬¼ÓČėŅ»¶ØĮæµÄ·“Ó¦Īļ·¢Éś·“Ó¦”£Ļą¹ŲŹż¾ŻČēĻĀ£ŗ
ČŻĘ÷±ąŗÅ | ĘšŹ¼Ź±ø÷ĪļÖŹĪļÖŹµÄĮæ/mol | “ļĘ½ŗā¹ż³ĢĢåĻµÄÜĮæµÄ±ä»Æ | |||
CO | H2O | CO2 | H2 | ||
¢Ł | 1 | 4 | 0 | 0 | ·Å³öČČĮæ£ŗ32.8 kJ |
¢Ś | 0 | 0 | 1 | 4 | ČČĮæ±ä»Æ£ŗQ kJ |
ĻĀĮŠĖµ·ØÖŠ£¬²»ÕżČ·µÄŹĒ(””””)
A. ČŻĘ÷¢ŁÖŠ·“Ó¦“ļĘ½ŗāŹ±£¬COµÄ×Ŗ»ÆĀŹĪŖ80%
B. ČŻĘ÷¢ŁÖŠCOµÄ×Ŗ»ÆĀŹµČÓŚČŻĘ÷¢ŚÖŠCO2µÄ×Ŗ»ÆĀŹ
C. Ę½ŗāŹ±£¬Į½ČŻĘ÷ÖŠCO2µÄÅضČĻąµČ
D. ČŻĘ÷¢ŁŹ±COµÄ·“Ó¦ĖŁĀŹµČÓŚH2OµÄ·“Ó¦ĖŁĀŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ100”ꏱ£¬½«0.100mol N2O4ĘųĢå³äČė1LŗćČŻ³éæÕµÄĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦£ŗN2O4£Øg£©![]() 2NO2£Øg£©”£øōŅ»¶ØŹ±¼ä¶ŌøĆČŻĘ÷ÄŚĪļÖŹµÄÅØ¶Č½ųŠŠ·ÖĪöµĆµ½Čē±ķŹż¾Ż”£»Ų“šÓŠ¹ŲĪŹĢā;
2NO2£Øg£©”£øōŅ»¶ØŹ±¼ä¶ŌøĆČŻĘ÷ÄŚĪļÖŹµÄÅØ¶Č½ųŠŠ·ÖĪöµĆµ½Čē±ķŹż¾Ż”£»Ų“šÓŠ¹ŲĪŹĢā;
Ź±¼ä(s) | 0 | 20 | 40 | 60 | 80 |
c(N2O4)/mol”¤L£1 | 0.100 | c1 | 0.050 | c3 | c4 |
c(NO2)/mol”¤L£1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
¢Łc3________c4(Ģī”°>”±”¢”°<”±»ņ”°£½”±)”£
¢ŚŌŚÉĻŹöĢõ¼žĻĀ£¬“Ó·“Ó¦æŖŹ¼Ö±ÖĮ“ļµ½»ÆŃ§Ę½ŗāŹ±£¬N2O4µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ_________mol”¤L£1”¤s£1”£
¢Ū“ļĘ½ŗāŗóĻĀĮŠĢõ¼žµÄøıäæÉŹ¹NO2ĘųĢåÅضČŌö“óµÄŹĒ_______(ĢīŠņŗÅ)”£
A£®Ą©“óČŻĘ÷µÄČŻ»ż B£®ŌŁ³äČėŅ»¶ØĮæµÄN2O4
C£®·ÖĄė³öŅ»¶ØĮæµÄNO2 D£®ŌŁ³äČėŅ»¶ØĮæµÄHe
¢ÜČōŌŚĻąĶ¬Ģõ¼žĻĀ£¬ĘšŹ¼Ź±Ö»³äČė0.200 mol NO2ĘųĢ壬Ōņ“ļµ½Ę½ŗāŹ±NO2ĘųĢåµÄ×Ŗ»ÆĀŹĪŖ_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøÖĢś·¢Éśµē»ÆøÆŹ“Ź±£¬øŗ¼«ÉĻ·¢ÉśµÄ·“Ó¦ŹĒ£Ø £©
A.2H++2e-=H2ӟB.2H2O+O2+4e-=4OH-
C.Fe-2e-=Fe2+D.4OH--4e-=O2ӟ+2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹé·ØĄė²»æŖĪÄ·æĖı¦(±Ź”¢Ä«”¢Ö½”¢Ńā)£¬×ö±ŹÓƵĥĒŗĮ£¬ŃŠÄ«ÓƵÄÄ«ĢõŅŌ¼°ŠūÖ½(¼“°×Ö½)ŗĶ×öŃāĢØÓƵÄŃāŹÆµÄÖ÷ŅŖ³É·ÖŅĄ“ĪŹĒ
A. ¶ąĢĒ”¢ĢæŗŚ”¢µ°°×ÖŹ”¢ĪŽ»śŃĪ
B. ĖÜĮĻ”¢ĆŗĢ攢¶ąĢĒ”¢ĪŽ»śŃĪ
C. µ°°×ÖŹ”¢ĢæŗŚ”¢¶ąĢĒ”¢ĪŽ»śŃĪ
D. µ°°×ÖŹ”¢ĆŗĢ攢¶ąĢĒ”¢ÓŠ»ś²£Į§
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com