
【题目】已知氨气、氯化氢极易溶于水。实验室用下图所示装置干燥收集气体R,并吸收多余尾气,则R是( )

A.CH4B.HClC.COD.NH3
科目:高中化学 来源: 题型:
【题目】将HI(g)置于密闭容器中,某温度下发生下列变化:2HI(g)H2(g)+I2(g) △H<0
(1)该反应平衡常数的表达式为K=___。
(2)当反应达到平衡时c(I2)=0.5mol/L,c(HI)=4mol/L,则c(H2)为____,HI的分解率为____。
(3)若该反应800℃时达到平衡状态,且平衡常数为1.0,某时刻,测得容器内各物质的溶度分别为c(HI)=2.0mol/L,c(I2)=1.0mol/L,c(H2)=1.0mol/L,则该时刻,反应向____(填“正向”或“逆向”,下同)进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16 g白色沉淀,在所得的悬浊液中逐滴加入1 mol·L-1 HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示,试回答:
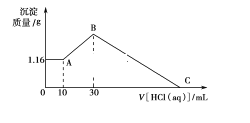
(1)A点→B点反应的离子方程式为____________________________________。
(2)原混合物中AlCl3的物质的量为________________,NaOH的物质的量为___________________。
(3)HCl溶液在C点的加入量是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】厌氧性硫酸盐还原菌(SRB)是导致金属微生物腐蚀最为普遍的菌种,铸铁管的一种腐蚀图解如图所示。下列说法正确的是
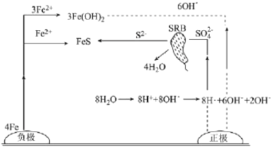
A.生成1molFeS,负极质量增加32g
B.正极区溶液的pH变小
C.正极电极反应式为:8H++8e-=8H·(吸附)、SO42-+8H·(吸附)+8e-![]() S2-+4H2O
S2-+4H2O
D.总反应:4Fe+4H2O+SO42-![]() FeS+3Fe(OH)2+2OH-
FeS+3Fe(OH)2+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环氧乙烷常用于一次性口罩生产过程中灭菌和新冠病毒的消杀,工业上常利用乙烯直接氧化法生产环氧乙烷(![]() ),发生的反应如下。
),发生的反应如下。
主反应Ⅰ:2CH2=CH2(g)+O2(g)![]() 2
2![]() (g)
(g) ![]() =-210kJ·mol-1
=-210kJ·mol-1
副反应Ⅱ:CH2=CH2(g)+3O2(g)![]() 2CO2(g)+2H2O)(l)
2CO2(g)+2H2O)(l)![]() =-1324kJ·mol-1
=-1324kJ·mol-1
Ⅲ.2![]() (g)+5O2(g)
(g)+5O2(g)![]() 4CO2(g)+4H2O(g)
4CO2(g)+4H2O(g)![]()
已知:环氧乙烷选择性是指乙烯进行反应Ⅰ生成环氧乙烷的优势。
(1)![]() =_________kJ·mol-1。
=_________kJ·mol-1。
(2)①图1是乙烯转化率、环氧乙烷选择性与流速关系的图象,图中随进料气的流速加快,乙烯的转化率下降,其可能原因是_________________。

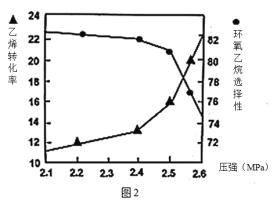
②图2是乙烯转化率、环氧乙烷选择性与压强关系的图象,图中当反应体系的压强高于2.4MPa,环氧乙烷选择性下降,其可能原因是__________________。
(3)实验测得反应Ⅰ中,v正=K正·x2(CH2=CH2)·x(O2),v逆=K逆·x2(![]() ),(式中x为物质的量分数;K正、K逆为速率常数,只与温度有关)。
),(式中x为物质的量分数;K正、K逆为速率常数,只与温度有关)。
①若在1L的密闭容器中充2molCH2=CH2(g)和1molO2(g),在一定温度下只发生反应,达到平衡时CH2=CH2的转化率为75%,则该反应平衡常数的值为___________。
②若平衡后仅升高温度,则下列说法正确的是___________。
a.x(CH2=CH2)增大,x(![]() )减小
)减小
b.K正与K逆的比值增大
c.v正减小,v逆增大
d.K正与K逆的比值减小
(4)将乙烯与饱和食盐水的电解产物反应,转化为氯乙醇[CH2(OH)CH2C],氯乙醇进一步反应生成环氧乙烷,其电解简易装置如右图所示。
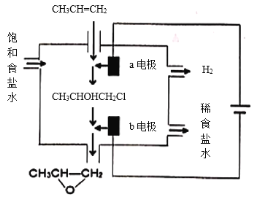
已知:CH2=CH2+H2O+Cl2→CH2(OH)CH2Cl+HCl
①a电极为___________(选填“阴极”或“阳极”)。
②b电极区域生成环氧乙烷的化学方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A.实验室常用排饱和食盐水的方法收集氯气
B.合成氨反应中,为提高氢气的转化率,理论上应采取加压的措施
C.对于2HI(g) ![]() H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
D.反应CO(g)+NO2(g) ![]() CO2(g)+NO(g) △H<0,达平衡后,升高温度体系颜色变深
CO2(g)+NO(g) △H<0,达平衡后,升高温度体系颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇是一种重要的化工原料和燃料,常见合成乙醇的途径如下:
(1)乙烯气相直接水合法:C2H4(g)+H2O(g)=C2H5OH(g) ΔH1=akJ·mol-1
已知:C2H4(g)+3O2(g)=2CO2(g)+2H2O(g) ΔH2=-1323.0kJ·mol-1
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) ΔH3=-1278.5kJ·mol-1,则a=__。
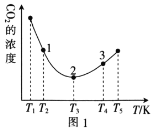
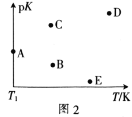
(2)工业上常采用CO2和H2为原料合成乙醇,某实验小组将CO2(g)和H2(g)按1:3的比例置于一恒容密闭容器中发生反应:2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g) ΔH=bkJ·mol-1。在相同的时间内,容器中CO2的浓度随温度T的变化如图1所示,上述反应的pK(pK=-lgK,K表示反应平衡常数)随温度T的变化如图2所示。
C2H5OH(g)+3H2O(g) ΔH=bkJ·mol-1。在相同的时间内,容器中CO2的浓度随温度T的变化如图1所示,上述反应的pK(pK=-lgK,K表示反应平衡常数)随温度T的变化如图2所示。
①由图1可知,b=__(填“![]() ”“
”“![]() ”或“<”)0。
”或“<”)0。
②在T1~T2及T4~T5两个温度区间内,容器中CO2(g)的浓度呈现如图1所示的变化趋势,其原因是___。
③图1中点1、2、3对应的逆反应速率v1、v2、v3中最大的是___(填“v1”“v2”或“v3”);要进一步提高H2(g)的转化率,可采取的措施有___(任答一条)。
④图2中当温度为T1时,pK的值对应A点,则B、C、D、E四点中表示错误的是__。
⑤乙烯气相直接水合法过程中会发生乙醇的异构化反应:C2H5OH(g)![]() CH3OCH3(g) ΔH=+50.7kJ·mol-1,该反应的速率方程可表示为v正=k正c(C2H5OH)和v逆=k逆c(CH3OCH3),k正和k逆只与温度有关。该反应的活化能Ea(正)__(填“
CH3OCH3(g) ΔH=+50.7kJ·mol-1,该反应的速率方程可表示为v正=k正c(C2H5OH)和v逆=k逆c(CH3OCH3),k正和k逆只与温度有关。该反应的活化能Ea(正)__(填“![]() ”“
”“![]() ”或“<”) Ea(逆),已知:T℃时,k正=0.006s-1,k逆=0.002s-1,该温度下向某恒容密闭容器中充入1.5mol乙醇和4mol甲醚,此时反应__(填“正向”或“逆向”)进行。
”或“<”) Ea(逆),已知:T℃时,k正=0.006s-1,k逆=0.002s-1,该温度下向某恒容密闭容器中充入1.5mol乙醇和4mol甲醚,此时反应__(填“正向”或“逆向”)进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积为2L且固定的密闭容器中充入2 molSO2和1 molO2,测得起始容器压强为p,一定条件下发生反应:2SO2(g)+O2(g) ![]() 2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,第一次反应达到平衡时共放出热量176.4kJ,此时再向容器中充入2 molSO2和1 molO2,达到新平衡,则下列说法正确的是
2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,第一次反应达到平衡时共放出热量176.4kJ,此时再向容器中充入2 molSO2和1 molO2,达到新平衡,则下列说法正确的是
A.该温度下,此反应的平衡常数为810
B.若使用高效催化剂,第一次达到平衡时放出热量大于176.4kJ
C.第一次反应达到平衡时,容器内压强为0.7p
D.若降低容器的温度可使新平衡时各物质的体积分数与第一次平衡时相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用某冶金行业产生的废渣(主要含![]() ,还有少量
,还有少量![]() 、
、![]() 等杂质)可以制备
等杂质)可以制备![]() ,生产流程如下:
,生产流程如下:
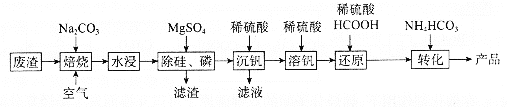
已知:![]() 微溶于水、溶于碱生成
微溶于水、溶于碱生成![]() (加热生成
(加热生成![]() ),具有强氧化性。向
),具有强氧化性。向![]() 溶液中加酸,不同
溶液中加酸,不同![]() 对应的主要存在形式如表:
对应的主要存在形式如表:
|
| 10.6~12 | 约8.4 | 3~8 | 约2 | <1 |
存在形式 |
|
|
|
|
|
|
回答下列问题:
(1)“焙烧”后V元素转化为![]() ,
,![]() 元素转化为________(写化学式)。
元素转化为________(写化学式)。
(2)欲除尽磷元素(即![]() ),最终溶液中
),最终溶液中![]() 的浓度至少为________
的浓度至少为________![]() (已知
(已知![]() )。
)。
(3)“沉钒”过程中,![]() 由8.5到5.0发生反应的离子方程式为________;最终需要控制
由8.5到5.0发生反应的离子方程式为________;最终需要控制![]() 约为________;“沉钒”最终得到的主要含钒物质是________(写化学式)。
约为________;“沉钒”最终得到的主要含钒物质是________(写化学式)。
(4)“还原”和“转化”过程中主要反应的离子方程式分为________、________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com