
分析 氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,结合反应的方程式分析解答.
解答 解:(1)向FeCl2溶液中滴加氯水,发生反应2Fe2++Cl2=2Fe3++2Cl-,氧化性:Cl2>Fe3+;(2)再滴加KSCN溶液,溶液变红,证明(1)发生了氧化还原反应.(3)加入铜粉,振荡,溶液红色消失,发生的反应为:2Fe3++Cu=2Fe2++Cu2+,氧化性:Fe3+>Cu2+;所以Fe3+、Cu2+、Cl2的氧化性顺序为:Cl2>Fe3+>Cu2+;
故答案为:Cl2、Fe3+、Cu2+;2Fe2++Cl2=2Fe3++2Cl-;2Fe3++Cu=2Fe2++Cu2+.
点评 本题考查了亚铁离子和铁离子的检验、氧化还原反应,题目难度不大,注意把握常见离子的检验方法和氧化性强弱的比较方法.


科目:高中化学 来源: 题型:解答题
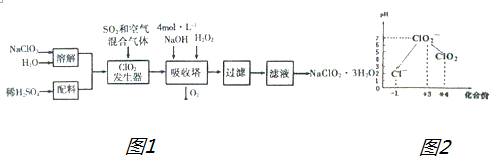
| 弱酸 | HClO2 | HF | HCN | H2S |
| Ka/mol•L-1 | 1×10-2 | 6.3×10-4 | 4.9×10-10 | K1=9.1×10-8 K2=1.1×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| B. | 在一定条件下,1.0 mol的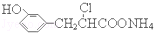 ,最多能与含2.0 mol NaOH的溶液完全反应 ,最多能与含2.0 mol NaOH的溶液完全反应 | |
| C. | 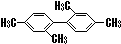 分子中至少有11个碳原子处于同一平面上 分子中至少有11个碳原子处于同一平面上 | |
| D. | 1mol有机物 一定条件下能和7molNaOH反应 一定条件下能和7molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
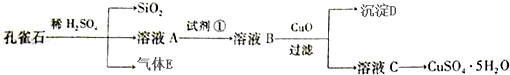
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1=△H2 | B. | △H1>△H2 | C. | △H2>△H1 | D. | 无法比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 澄清透明的溶液中:Cu2+、Fe3+、NO3-、Cl- | |
| B. | 使红色石蕊试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl- | |
| C. | 含有大量ClO-的溶液中:K+、OH-、I-、SO32- | |
| D. | c(Fe3+)=0.1 mol•L-1的溶液中:K+、ClO-、SO42-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2 SO3.某化学兴趣小组进行该实验时,却检测到生成的盐中含有SO42-.
资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2 SO3.某化学兴趣小组进行该实验时,却检测到生成的盐中含有SO42-.| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| T/℃ | 50 | 60 | 70 | 80 | 90 |
| c/mol.L-1 | 1.0 | 3.0 |
| 实验方案(不要求写出具体操作过程) | 预期实验现象和结论 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com