
【题目】(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH= +49.0kJ/mol
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g) ΔH= -192.9kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH= -192.9kJ/mol
由上述方程式可知:CH3OH的燃烧热____(填“大于”“等于”或“小于”)192.9kJ/mol。已知水的气化热为44kJ/mol。则表示氢气燃烧热的热化学方程式为___。
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH= -159.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5kJ/mol
③H2O(l)=H2O(g) ΔH= +44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式___。
(3)已知:①Fe(s)+![]() O2(g)=FeO(s) ΔH1= -272.0kJ/mol
O2(g)=FeO(s) ΔH1= -272.0kJ/mol
②2Al(s)+![]() O2(g)=Al2O3(s) ΔH2= -1675.7kJ/mol
O2(g)=Al2O3(s) ΔH2= -1675.7kJ/mol
Al和FeO发生铝热反应的热化学方程式是___。铝热反应的反应类型___,某同学认为,铝热反应可用于工业炼铁,你的判断是____(填“能”或“不能”),你的理由____。
(4)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。已知:25℃、101KPa下:
①H2(g)+![]() O2(g)=H2O(g) ΔH1= -242kJ/mol
O2(g)=H2O(g) ΔH1= -242kJ/mol
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g) ΔH2= -676kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH2= -676kJ/mol
写出CO2和H2生成气态甲醇等产物的热化学方程式____。
【答案】大于 H2(g)+![]() O2(g)=H2O(l) ΔH= -124.6kJ/mol 2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) ΔH= -87.0kJ/mol 3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s) ΔH= -859.7kJ/mol 置换反应 不能 该反应的引发,需消耗大量能量,成本较高 CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH= -50kJ/mol
O2(g)=H2O(l) ΔH= -124.6kJ/mol 2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) ΔH= -87.0kJ/mol 3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s) ΔH= -859.7kJ/mol 置换反应 不能 该反应的引发,需消耗大量能量,成本较高 CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH= -50kJ/mol
【解析】
(1)根据盖斯定律得到所需热化学反应方程式;
(2)由已知热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式;
(3)根据盖斯定律书写目标热化学方程式;利用铝热反应大量制取金属时考虑经济效益;
(4)根据盖斯定律,①×3-②可得目标热化学方程式。
(1)反应②,燃烧热中生成的水必须是液态水,气态水变为液态水放出热量,故甲醇完全燃烧释放的热量应大于192.9kJmol-1,
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H= +49.0kJ/mol
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g) △H= -192.9kJ/mol
O2(g)=CO2(g)+2H2O(g) △H= -192.9kJ/mol
③H2O(g)=H2O(l) △H= -44kJmol-1
根据盖斯定律计算,[③×3-②-①]×![]() ,热化学反应方程式为:H2(g)+
,热化学反应方程式为:H2(g)+![]() O2(g)=H2O(l) ΔH= -124.6kJ/mol;
O2(g)=H2O(l) ΔH= -124.6kJ/mol;
(2)①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH= -159.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5kJ/mol
③H2O(l)=H2O(g) ΔH= +44.0kJ/mol
依据热化学方程式和盖斯定律计算①+②③得到CO2与NH3合成尿素和液态水的热化学反应方程式为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) ΔH= -87.0kJ/mol;
(3)依据盖斯定律②-①×3得到热化学方程式为:3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s) ΔH= -859.7kJ/mol;该反应类型属于置换反应;利用铝热反应在工业上大面积炼铁时,需要消耗冶炼成本更高的Al,冶炼Fe的成本就太高了;
(4)①H2(g)+![]() O2(g)=H2O(g) ΔH1= -242kJ/mol
O2(g)=H2O(g) ΔH1= -242kJ/mol
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g) ΔH2= -676kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH2= -676kJ/mol
则①×3-②可得CO2和H2生成气态甲醇等产物的热化学方程式为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH= -50kJ/mol。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】“花卉保鲜剂”是一种可以延长花期的试剂。如表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
成分 | 质量(g) | 摩尔质量(gmol1) |
蔗糖 | 25.00 | 342 |
硫酸钾 | 0.87 | 174 |
阿司匹林 | 0.17 | 180 |
高锰酸钾 | 0.316 | 158 |
硝酸银 | 0.0075 | 170 |
(1)下列“花卉保鲜剂”的成分中,属于非电解质的是______,可做杀菌剂的是____
A. 高锰酸钾B. 硫酸钾C. 蔗糖D. 硝酸银E. 水
(2) 配制1L上述“鲜花保鲜剂”需要高锰酸钾______mol。
(3)在溶液配制过程中,下列操作会使配制结果无影响的是______。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚配制完一定物质的量浓度的氯化钠溶液未洗涤
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为______mol/L。
(5)如果用高铁酸钾(K2FeO4)代替高锰酸钾效果会更好,湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O.碱性条件下,氧化剂与还原剂的物质的量的比为3:2发生反应,写出并配平湿法制备高铁酸钾的离子反应方程式___________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不属于四种基本反应类型,但属于氧化还原反应的是
A.Zn+CuSO4=ZnSO4+CuB.3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
C.AgNO3+KCl=AgCl↓+KNO3D.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中通入两种气体并使其发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )

A. 该反应的化学方程式为3B+4D![]() 6A+2C
6A+2C
B. 0~1 s内,v(A)=v(C)
C. 0~6 s内,B的平均反应速率为0.05 mol·L-1·s-1
D. 0~6 s内,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某温度时,在2 L容器中A、B两种物质间的转化反应中,A、B物质的量随时间变化的曲线如下图所示,由图中数据分析得:
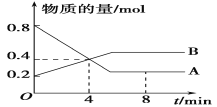
①该反应的化学方程式为____________________;
②反应开始至4 min时,B的平均反应速率为________ ,A的反应速率为_____ ,A的转化率为_____。
③4 min时,反应是否达到平衡状态?________(填“是”或“否”),8 min时,v(正)________v(逆)(填“>”、“<”或“=”)。
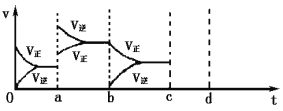
(2)下图表示在密闭容器中反应:2SO2(g) + O2(g)![]() 2SO3(g)△H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时改变的条件可能是______________;b时改变的条件可能是______________。
2SO3(g)△H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时改变的条件可能是______________;b时改变的条件可能是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.Na2O2与H2O反应:2O![]() +2H2O===O2↑+4OH-
+2H2O===O2↑+4OH-
B.向Fe2(SO4)3溶液中加入足量Cu粉:2Fe3++3Cu===2Fe+3Cu2+
C.向NaHSO4溶液中加入Ba(OH)2溶液至中性:2H++SO![]() +Ba2++2OH-===BaSO4↓+2H2O
+Ba2++2OH-===BaSO4↓+2H2O
D.向银氨溶液中加入足量盐酸:[Ag(NH3)2]++2H+===Ag++2NH![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断正确的是( )

A.图1可表示电解200 mL 0.1 mol·L-1 NaCl溶液过程中,产生氢气体积(标准状况)与转移电子物质的量的关系曲线
B.图2可表示常温下0.1 mol·L-1盐酸滴加到40 mL 0.1 mol·L-1 NaOH溶液的滴定曲线
C.高温下能自发进行的反应CO2(g)+H2(g)![]() CO(g)+H2O(g)的能量变化如图3所示,则该反应的ΔS>0
CO(g)+H2O(g)的能量变化如图3所示,则该反应的ΔS>0
D.图4可表示反应N2(g)+3H2(g)![]() 2NH3(g)在t1时刻扩大容器体积时,v逆随时间的变化曲线
2NH3(g)在t1时刻扩大容器体积时,v逆随时间的变化曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大。A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物是常用的食品调味剂。
回答下列问题:
(1)写出元素D在周期表中的位置____________________________________________。
(2)五种元素中,原子半径最大的是________(填元素符号),非金属最强的是________(填元素符号)。
(3)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是________(用化学式表示)。
(4)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为________,其中存在的化学键类型为_______________和________________。
(5)单质E与水反应的离子方程式为____________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物在生产生活中广泛存在。
(1)①氯胺(NH2Cl)的电子式为________。可通过反应NH3(g)+Cl2(g)=NH2Cl(g)+HCl(g)制备氯胺,已知部分化学键的键能如右表所示(假定不同物质中同种化学键的键能一样),则上述反应的ΔH=_________。
化学键 | 键能/(kJ·mol-1) |
N-H | 391.3 |
Cl-Cl | 243.0 |
N-Cl | 191.2 |
H-Cl | 431.8 |
②NH2Cl与水反应生成强氧化性的物质,可作长效缓释消毒剂,该反应的化学方程式为________。
(2)用焦炭还原NO的反应为:2NO(g)+C(s)![]() N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
t/min | 0 | 40 | 80 | 120 | 160 |
n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
n(NO)(乙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
n(NO)(丙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
①该反应为____________(填“放热”或“吸热”)反应。
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=_________。
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s) ![]() N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
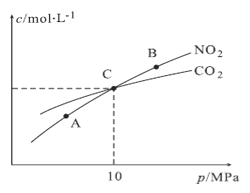
①A、B两点的浓度平衡常数关系:Kc(A)_____Kc(B)(填“<”或“>”或“=”)。
②A、B、C三点中NO2的转化率最高的是______(填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp(C)=______(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com