
【题目】氮及其化合物在人们的生活经常出现。
(1)汽车尾气中NO生成过程的能量变化示意图如图:
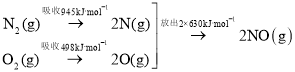
该条件下,![]() 和
和![]() 完全反应生成
完全反应生成![]() ,会___(填“吸收”或“放出”)__kJ能量。
,会___(填“吸收”或“放出”)__kJ能量。
(2)一定温度下,在体积为![]() 的恒容密闭容器中,氮的气态氧化物X和Y之间反应过程中各物质的物质的量与时间的关系如图所示。
的恒容密闭容器中,氮的气态氧化物X和Y之间反应过程中各物质的物质的量与时间的关系如图所示。
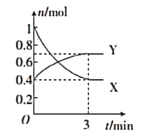
①写出该反应的化学反应方程式:____(用物质的化学式表示)
②在![]() 内,用Y表示的反应速率为____。
内,用Y表示的反应速率为____。
③下列叙述能说明该反应已达到化学平衡状态的是____(填字母)。
a.容器内压强不再发生变化
b.X的体积分数不再发生变化
c.容器内原子总数不再发生变化
d.相同时间内消耗![]() 的同时生成
的同时生成![]()
④反应达到平衡后,若降低温度,则v(正)____,v(逆)___。(填“增大“减小”或“不变”)。
(3)反应![]() 在四种不同情况下的反应速率分别为:
在四种不同情况下的反应速率分别为:
①![]() ②
②![]()
③![]() ④
④![]()
该反应在四种不同情况下速率由大到小的顺序为(用序号填空)_____。
【答案】吸收 91.5 ![]()
![]() ab 减小 减小 ②>③>①=④
ab 减小 减小 ②>③>①=④
【解析】
根据断键和成键过程中能量的变化计算反应热;根据反应物的浓度变化计算反应速率;根据化学平衡状态的特征分析反应是否达到平衡;根据反应速率与化学计量数间的关系比较反应的快慢。
(1)断键吸收能量为945kJ+498kJ=1443kJ/mol,成键放出能量为2×630kJ=1260kJ/mol,由于吸收的能量大于放出的能量,所该反应为吸热反应,生成1molNO吸收的热量为![]() (1443kJ/mol-1260kJ/mol)=91.5kJ/mol,故答案为:吸收;91.5;
(1443kJ/mol-1260kJ/mol)=91.5kJ/mol,故答案为:吸收;91.5;
(2)①根据图示可知反应物X消耗1mol-0.4mol=0.6mol时,生成Y0.7mol-0.4mol=0.3mol,则根据原子守恒可知该反应为![]() ;
;
②v(Y)=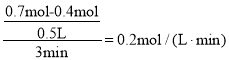 ;
;
③a.该反应为气体体积减小的反应,当容器内压强不再发生变化,说明反应已经达到平衡,故此项正确;
b.X的体积分数不再发生变化,说明反应物的浓度不再变化,说明反应已经达到平衡,故此项正确;
c.根据原子守恒,反应前后原子总数始终不变,所以容器内原子总数不再发生变化不能说明反应已经达到平衡,故此项错误;
d.消耗![]() 的同时生成
的同时生成![]() 都是逆反应的过程,不能说明正反应速率等于逆反应速率,故此项错误,故选ab;
都是逆反应的过程,不能说明正反应速率等于逆反应速率,故此项错误,故选ab;
④温度越高反应越快,所以减低温度时,正逆反应速率都减小,故答案为:减小;减小;
(3)根据反应速率之比等于化学计量数之比计算知:①![]() ②
②![]() ,则
,则![]() ;③
;③![]() ,则
,则![]() ,④
,④![]() ,则
,则![]() ,所以该反应在四种不同情况下速率由大到小的顺序为②>③>①=④。
,所以该反应在四种不同情况下速率由大到小的顺序为②>③>①=④。


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:
【题目】(1)用如图装置做以下两个实验:
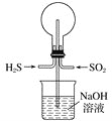
①常温下将H2S和SO2以物质的量之比为1∶1充满烧瓶,不久,烧瓶中能观察到的现象是_______。
②若用Cl2代替SO2,其他条件不变,观察到的现象与①相同之处为______,不同之处为_____;试用简要文字和化学方程式解释原因: ______。
③若想使②中反应后,烧瓶内产生“喷泉”现象,引发的操作为________。
(2)某课外活动小组利用如图所示装置进行实验:
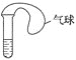
在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,因此溶液可能是_____溶液;加热时溶液由无色变为红色的原因是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B是中学化学常见的化合物,它们各由两种元素组成;乙为元素R组成的单质,它们之间存在如图所示关系。根据要求回答问题:
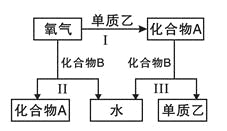
(1)上图三个反应中,属于氧化还原反应的有____个。
(2)若元素R与氧同主族,下列事实能说明R与氧的非金属性相对强弱的有____。
A.还原性:H2R>H2O B.酸性:H2R>H2O
C.稳定性:H2R<H2O D.沸点:H2R<H2O
(3)若化合物B常温下为气体,其水溶液呈碱性(答题必须用具体物质表示)。
①化合物B的电子式为______;其水溶液呈碱性的原因是______(用离子方程式表示)。
②化合物B可与O2组成燃料电池(氢氧化钾溶液为电解质溶液),其反应产物与反应Ⅲ相同。写出该电池负极的电极反应式______________________。
③当1mol的化合物B分别参与反应Ⅱ、Ⅲ时,热效应为△H1和△H2,则反应Ⅰ的热化学方程式为______________(注:反应条件相同、所有物质均为气体)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)是一种具有许多优良性能的金属,钛和钛合金被认为是21世纪的重要金属材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态电子排布式可表示为_____。
②与BH4-互为等电子体的阳离子的化学式为_____。
③H、B、Ti原子的第一电离能由小到大的顺序为_____。
(2)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米TiO2催化的一个实例如图所示。
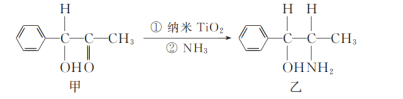
化合物乙的分子中采取sp3杂化方式的原子个数为_____。
(3)水溶液中并没有[Ti(H2O)6)]4+离子,而是[Ti(OH)2(H2O)4]2+离子,1mol[Ti(OH)2(H2O)4]2+中σ键的数目为____。
(4)氮化钛(TiN)具有典型的NaCl型结构,某碳氮化钛化合物,结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,则此碳氮化钛化合物的化学式是_____。
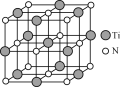
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在实验室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。
已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2
②氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O
5NaCl+NaClO3+3H2O
该兴趣小组设计了下列实验装置,进行实验。
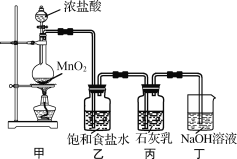
请回答下列问题:
(1)①甲装置用于制备氯气,乙装置的作用是__。
②实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法不正确的是_。(填字母)
A.若产物为NaClO3、NaCl,则参加反应的氧化剂和还原剂的物质的量之比为1∶5
B.若产物为NaClO、NaCl,则吸收后的溶液中n(NaClO)=n(NaCl)
C.若产物为NaClO、NaClO3、NaCl,则NaOH与Cl2相互反应的物质的量之比为2∶1
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。他们讨论后认为,其可能原因是部分氯气未与石灰乳反应而逸出,以及温度升高。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢匀速地通入足量氯气,得出了Ca(ClO)2、Ca(ClO3)2两种物质的物质的量(n)与反应时间(t)的关系曲线,粗略表示为如图(不考虑氯气和水的反应)。
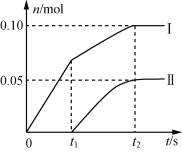
①图中曲线II表示__(填物质的化学式)的物质的量随反应时间变化的关系;
②所取石灰乳中含有Ca(OH)2的物质的量为__mol;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用足量的一氧化碳还原4.64 g某金属氧化物,把生成的二氧化碳全部通入到过量的澄清石灰水中,得到的沉淀干燥后质量为8.0 g,则此金属氧化物是下列中的( )
A. 氧化铜 B. 氧化铁 C. 四氧化三铁 D. 二氧化锰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组利用下列装置探究氯气与氨气的反应.其中A、B分别为氯气和氨气的发生装置,C为纯净干燥的氯气与氨气反应的装置.

(1)若Cl2从左向右流动,NH3从右向左流动,则上述实验装置中,依次连接的合理顺序为:A→________________→B;为使NH3与Cl2更充分混合,Cl2应从C装置的__口进入(填“x”或“y”).
(2)简述装置A中使用分液漏斗向圆底烧瓶中滴加浓盐酸的操作是__________________.
(3)装置A中发生反应的离子方程式为_______________________________.
(4)装置B中圆底烧瓶内的试剂为______________(填名称).
(5)装置D的作用是____________________________.
(6)反应开始后,装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气中的主要成分之一,该反应的化学方程式为________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,能达到实验目的的是
A. 实验室制取氨气
实验室制取氨气
B.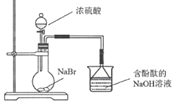 烧杯中红色褪去能证明生成HBr
烧杯中红色褪去能证明生成HBr
C. 实验室制取氧气
实验室制取氧气
D.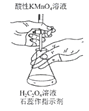 用酸性KMnO4溶液滴定HCO4溶液
用酸性KMnO4溶液滴定HCO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,50mL0.10 mol·L-1醋酸中存在电离平衡:CH3COOH![]() CH3COO-+H+
CH3COO-+H+
(1)加入少量醋酸钠,上述平衡向___移动(填“左”、“右”、“不”,下同)。
(2)加入少量0.1 mol·L-1盐酸,上述平衡向___移动,c(H+)___(填“增大”、“减小”、“不变”,下同)。
(3)加入碳酸钠固体,上述平衡向___移动,c(H+)___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com