
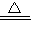 CaCl2+2NH3↑+2H2O,干燥管中的干燥剂,氨气不能与干燥剂反应,且干燥剂且能吸水,碱石灰是固体氢氧化钠和氧化钙的混合物,所以碱石灰能作干燥剂;
CaCl2+2NH3↑+2H2O,干燥管中的干燥剂,氨气不能与干燥剂反应,且干燥剂且能吸水,碱石灰是固体氢氧化钠和氧化钙的混合物,所以碱石灰能作干燥剂;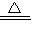 CaCl2+2NH3↑+2H2O;碱石灰;向下排空气;湿润的红色石蕊试纸变蓝 或用蘸有浓盐酸的玻璃棒放在瓶口,产生白烟.
CaCl2+2NH3↑+2H2O;碱石灰;向下排空气;湿润的红色石蕊试纸变蓝 或用蘸有浓盐酸的玻璃棒放在瓶口,产生白烟.

科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com