A
分析:在1L含0.1mol NaAlO
2和0.1mol Ba(OH)
2的混合溶液中n(NaAlO
2)=0.1mol,n[Ba(OH)
2]=0.1mol,向该混合溶液中加入H
2SO
4溶液,首先发生反应Ba(OH)
2+H
2SO
4=BaSO
4↓+2H
2O,Ba(OH)
2反应完毕,继续加入H
2SO
4溶液,再发生反应AlO
2-+H
++H
2O=Al(OH)
3↓,AlO
2-反应完毕,沉淀达最大,继续加入H
2SO
4溶液,发生反应Al(OH)
3+3H
+=Al
3++3H
2O,沉淀减少,Al(OH)
3反应完毕,最后为BaSO
4沉淀,继续加入H
2SO
4溶液,沉淀的量不变.
第一阶段:由发生反应Ba(OH)
2+H
2SO
4=BaSO
4↓+2H
2O可知,Ba(OH)
2反应完毕,需加入0.1molH
2SO
4,H
2SO
4溶液的体积为

=1L,生成沉淀n(BaSO
4)=0.1mol;
第二阶段:由发生反应AlO
2-+H
++H
2O=Al(OH)
3↓可知,0.1molAlO
2-反应完毕,该阶段需加入0.05molH
2SO
4,H
2SO
4溶液的体积为

=0.5L,该阶段生成沉淀n[Al(OH)
3]=0.1mol,但加入相同体积的硫酸,该阶段比第一阶段生成沉淀的多,为第一阶段的2倍;
第三阶段:由发生反应Al(OH)
3+3H
+=Al
3++3H
2O可知,沉淀减少,0.1molAl(OH)
3完全溶解,该阶段需加入

=0.15molH
2SO
4,H
2SO
4溶液的体积为

=1.5L,沉淀n(BaSO
4)=0.1mol;
据此作出图象进行判断.
解答:在1L含0.1mol NaAlO
2和0.1mol Ba(OH)
2的混合溶液中n(NaAlO
2)=0.1mol,n[Ba(OH)
2]=0.1mol,向该混合溶液中加入H
2SO
4溶液,首先发生反应Ba(OH)
2+H
2SO
4=BaSO
4↓+2H
2O,Ba(OH)
2反应完毕,继续加入H
2SO
4溶液,再发生反应AlO
2-+H
++H
2O=Al(OH)
3↓,AlO
2-反应完毕,沉淀达最大,继续加入H
2SO
4溶液,发生反应Al(OH)
3+3H
+=Al
3++3H
2O,沉淀减少,Al(OH)
3反应完毕,最后为BaSO
4沉淀,继续加入H
2SO
4溶液,沉淀的量不变.
第一阶段:由发生反应Ba(OH)
2+H
2SO
4=BaSO
4↓+2H
2O可知,Ba(OH)
2反应完毕,需加入0.1molH
2SO
4,H
2SO
4溶液的体积为

=1L,生成沉淀n(BaSO
4)=0.1mol;
第二阶段:由发生反应AlO
2-+H
++H
2O=Al(OH)
3↓可知,0.1molAlO
2-反应完毕,该阶段需加入0.05molH
2SO
4,H
2SO
4溶液的体积为

=0.5L,该阶段生成沉淀n[Al(OH)
3]=0.1mol,但加入相同体积的硫酸,该阶段比第一阶段生成沉淀的多,为第一阶段的2倍;
第三阶段:由发生反应Al(OH)
3+3H
+=Al
3++3H
2O可知,沉淀减少,0.1molAl(OH)
3完全溶解,该阶段需加入

=0.15molH
2SO
4,H
2SO
4溶液的体积为

=1.5L,沉淀n(BaSO
4)=0.1mol.
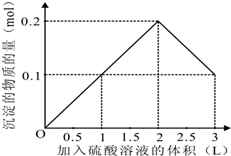
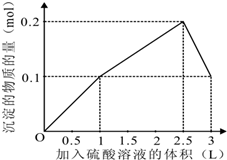
由上述分析可知:
第一阶段产生沉淀n(BaSO
4)=0.1mol,加入H
2SO
4溶液的体积为1L;
第二阶段又生成沉淀n[Al(OH)
3]=0.1mol,此时沉淀总量为0.2mol,该阶段加入H
2SO
4溶液的体积为0.1L,此时加入H
2SO
4溶液的总体积为1.5L;
第三阶段0.1molAl(OH)
3完全溶解,此时沉淀n(BaSO
4)=0.1mol,该阶段加入H
2SO
4溶液的体积为1.5L,此时加入H
2SO
4的总体积为3L.
故沉淀的量与H
2SO
4溶液体积关系图为:

,
故选A.
点评:本题考查离子反应、化学计算、图象分析等,难度较大,理清反应的过程,确定沉淀的量与H
2SO
4溶液体积关系是关键,是对学生综合能力的考查.





 =1L,生成沉淀n(BaSO4)=0.1mol;
=1L,生成沉淀n(BaSO4)=0.1mol; =0.5L,该阶段生成沉淀n[Al(OH)3]=0.1mol,但加入相同体积的硫酸,该阶段比第一阶段生成沉淀的多,为第一阶段的2倍;
=0.5L,该阶段生成沉淀n[Al(OH)3]=0.1mol,但加入相同体积的硫酸,该阶段比第一阶段生成沉淀的多,为第一阶段的2倍; =0.15molH2SO4,H2SO4溶液的体积为
=0.15molH2SO4,H2SO4溶液的体积为 =1.5L,沉淀n(BaSO4)=0.1mol;
=1.5L,沉淀n(BaSO4)=0.1mol; =1L,生成沉淀n(BaSO4)=0.1mol;
=1L,生成沉淀n(BaSO4)=0.1mol; =0.5L,该阶段生成沉淀n[Al(OH)3]=0.1mol,但加入相同体积的硫酸,该阶段比第一阶段生成沉淀的多,为第一阶段的2倍;
=0.5L,该阶段生成沉淀n[Al(OH)3]=0.1mol,但加入相同体积的硫酸,该阶段比第一阶段生成沉淀的多,为第一阶段的2倍; =0.15molH2SO4,H2SO4溶液的体积为
=0.15molH2SO4,H2SO4溶液的体积为 =1.5L,沉淀n(BaSO4)=0.1mol.
=1.5L,沉淀n(BaSO4)=0.1mol. ,
,

![]() 为阿伏加德罗常数,则下列叙述不正确的是
为阿伏加德罗常数,则下列叙述不正确的是![]() 所含分子数为
所含分子数为![]()
![]()
![]()
![]() 溶液中,所含
溶液中,所含![]() 的离子数与
的离子数与![]() 的分子数之和为
的分子数之和为![]()