
【题目】含氧有机物甲可用来制取多种有用的化工产品,合成路线如图:

已知:Ⅰ.RCHO
Ⅱ.RCOOH![]() RCOCl
RCOCl![]() RCOOR’(R、R’代表烃基)
RCOOR’(R、R’代表烃基)
(1)甲的含氧官能团的名称是___。写出检验该官能团常用的一种化学试剂的名称___。
(2)写出己和丁的结构简式:己__,丁__。
(3)乙有多种同分异构体,属于甲酸酯,含酚羟基,且酚羟基与酯的结构在苯环邻位的同分异构体共有___种。
(4)在NaOH溶液中发生水解反应时,丁与辛消耗NaOH的物质的量之比为__。
(5)庚与M合成高分子树脂的化学方程式为___。
【答案】醛基 银氨溶液(或新制氢氧化铜悬浊液) ![]()
![]() 5 1:2
5 1:2 
【解析】
甲能与银氨溶液反应,则甲含有-CHO,甲与HCN发生加成反应、酸化得到乙,可推知甲为![]() ,甲与氢气发生加成反应生成丙为
,甲与氢气发生加成反应生成丙为![]() ,乙与丙在浓硫酸、加热条件下发生酯化反应生成丁为
,乙与丙在浓硫酸、加热条件下发生酯化反应生成丁为![]() .甲与与银氨溶液发生氧化反应、酸化生成戊为
.甲与与银氨溶液发生氧化反应、酸化生成戊为![]() ,戊分子羧基中-OH被Cl原子取代生成己为
,戊分子羧基中-OH被Cl原子取代生成己为![]() ,庚与有机物M发生聚合反应生成高分子树脂,由高分子树脂的结构可知,应是
,庚与有机物M发生聚合反应生成高分子树脂,由高分子树脂的结构可知,应是![]() 与HCHO发生的加聚反应,而庚与己发生反应生成辛,由信息可知,庚应含有羟基,故庚为
与HCHO发生的加聚反应,而庚与己发生反应生成辛,由信息可知,庚应含有羟基,故庚为![]() ,M为HCHO,辛为
,M为HCHO,辛为![]() ,据此解答。
,据此解答。
(1)甲为![]() ,含氧官能团是:醛基,检验醛基常用的化学试剂为:银氨溶液(或新制氢氧化铜悬浊液),故答案为:醛基;银氨溶液(或新制氢氧化铜悬浊液);
,含氧官能团是:醛基,检验醛基常用的化学试剂为:银氨溶液(或新制氢氧化铜悬浊液),故答案为:醛基;银氨溶液(或新制氢氧化铜悬浊液);
(2)由上述分析可知,己的结构简式为![]() ,丁的结构简式为
,丁的结构简式为![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;
(3)乙有多种同分异构体.属于甲酸酯,含酚羟基,且酚羟基与酯的结构在苯环邻位的同分异构体:
若有2个侧链,侧链为-OH、-CH2OOCH,若有3个侧链,侧链为-OH、-OOCH、-CH3 ,-OH、-OOCH处于邻位,-CH3 有4种位置,故共有5种,故答案为:5;
(4)在NaOH溶液中发生水解反应时,1mol丁(![]() )水解消耗1molNaOH,1mol辛(
)水解消耗1molNaOH,1mol辛(![]() )消耗NaOH为2mol,二者消耗氢氧化钠的物质的量之比为1:2,故答案为:1:2;
)消耗NaOH为2mol,二者消耗氢氧化钠的物质的量之比为1:2,故答案为:1:2;
(5)庚与M合成高分子树脂的化学方程式为: ,
,
故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】在体积为1L的密闭容器中![]() 体积不变
体积不变![]() 充入
充入![]() 和
和![]() ,一定条件下发生反应:
,一定条件下发生反应:![]() ,测得
,测得![]() 和
和![]() 的浓度随时间变化如图所示。下列说法正确的是
的浓度随时间变化如图所示。下列说法正确的是
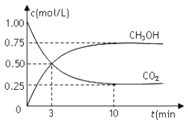
A.从反应开始到平衡,氢气的平均反应速率为![]()
B.进行到3min时,正反应速率和逆反应速率相等
C.10min后容器中各物质的量浓度不再改变
D.到达平衡状态时,反应放出![]() 的能量
的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:2N2O5(g )=2N2O4( g )+O2( g ) H1=-4.4kJ·mol-1
2NO2( g)=N2O4(g ) H2 =-55.3kJ·mol-1
则反应N2O5( g )=2NO2(g )+![]() O2(g )的H=_______ kJ·mol-1
O2(g )的H=_______ kJ·mol-1
(2)2molCH3OH(l)在O2(g)中完全燃烧,生成CO2(g)和H2O(l),放出887kJ热量:请写出CH3OH燃烧热的热化学方程式__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验淀粉水解的产物,设计如下实验方案:
![]()
请回答下列问题:
(1)试剂1为20%的H2SO4溶液,其作用是_________;
(2)试剂2为_________NaOH溶液,其作用是_________,使检验水解产物的实验得以顺利进行;发生反应的离子方程式为:_________;
(3)反应①的化学方程式为_________;
(4)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是_________;
(5)如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的_________(填”能”或”否”)否,若不能,其原因是_________硫酸能溶解Cu(OH)2而使实验失败,最简单的改正措施是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素A、B、C都是短周期元素,它们的原子序数大小为A<B<C。A元素原子的最外层电子数为次外层电子数的2倍;B元素原子的次外层电子数是最外层电子数的2倍。B与C可形成共价化合物BC4。请回答下列问题:
(1)这三种元素所对应的气态氢化物中最不稳定的是__________(填化学式),该氢化物在空气中燃烧的化学方程式为__________________________________________________________。
(2)它们的最高价氧化物对应的水化物中酸性最强的是__________,最弱的是__________(填酸的化学式)。
(3)BC4的化学式是__________。BC4不稳定,遇水易形成B的含氧酸及C的氢化物。近代海战中为了掩蔽军事目标,通常采用喷BC4和液氨的方法以形成烟幕,有关化学反应用方程式表示为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下述转化关系,回答问题:

已知:①+CH3Br![]() CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,直线交点处的圆圈为NaCl晶体中Na+或Cl-所处的位置。这两种离子在空间三个互相垂直的方向上都是等距离排列的。

(1)请将其中代表Na+的圆圈涂黑(不必考虑体积大小),以完成NaCl晶体结构示意图______________。
(2)晶体中,在每个Na+的周围与它最接近的且距离相等的Na+共有________个。
(3)在NaCl晶胞中正六面体的顶角上、面上、棱上的Na+或Cl-为该晶胞与其相邻的晶胞所共有,一个晶胞中Cl-的个数等于________,即________(填计算式);Na+的个数等于________,即________(填计算式)。
(4)设NaCl的摩尔质量为Mrg·mol-1,食盐晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA。食盐晶体中两个距离最近的钠离子间的距离为____________________________________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界的矿物、岩石的成因和变化受到许多条件的影响。地壳内每加深1km,压强增大约25000~30000 kPa。在地壳内SiO2和HF存在以下平衡:SiO2(s) +4HF(g)![]() SiF4(g)+ 2H2O(g) ΔH =-148.9kJ/mol。
SiF4(g)+ 2H2O(g) ΔH =-148.9kJ/mol。
(1)在地壳深处容易有_____气体逸出,在地壳浅处容易有_____沉积。
(2)如果上述反应的平衡常数K值变大,该反应_____(选填编号)。
a.一定向正反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(3)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,___。
a.2v正(HF)=v逆(H2O) b.v(H2O)=2v(SiF4)
c.SiO2的质量保持不变 d.反应物不再转化为生成物
(4)若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为某化学小组设计的一个用于探究电解原理的实验装置,其中X为阳离子交换膜。下列有关说法正确的是
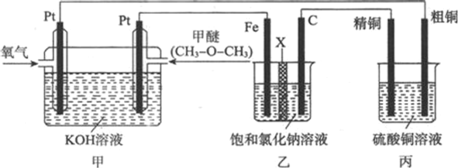
A.通入甲醚的电扳上发生的电极反应式为![]()
B.乙装置中C电极上生成氢气
C.反应一段时间后,向乙中加入几滴酚酞试液,铁电极附近溶液变红色
D.反应一段时间后,丙装置中两个电极上的质量变化量相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com