
| A. | 铁与硫酸铜溶液反应:Fe+Cu2+═Fe2++Cu | |
| B. | 氧化镁与稀盐酸混合:MgO+H+═Mg2++H2O | |
| C. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ |
分析 A.Fe和铜离子发生置换反应生成Cu和亚铁离子;
B.MgO和稀盐酸反应生成可溶性氯化镁和水,原子不守恒;
C.难溶物碳酸钙要写化学式;
D.漏写生成水的离子方程式.
解答 解:A.Fe和铜离子发生置换反应生成Cu和亚铁离子,离子方程式为Fe+Cu2+═Fe2++Cu,故A正确;
B.MgO和稀盐酸反应生成可溶性氯化镁和水,原子不守恒,离子方程式为MgO+2H+═Mg2++H2O,故B错误;
C.难溶物碳酸钙要写化学式,离子方程式为CaCO3+2H+═Ca2++CO2↑+H2O,故C错误;
D.漏写生成水的离子方程式,离子方程式为2H++2OH-+Ba2++SO42-═BaSO4↓+2H2O,故D错误;
故选A.
点评 本题考查离子方程式书写正误判断,为高频考点,明确离子方程式书写规则及反应实质是解本题关键,注意要遵循客观事实、原子守恒、电荷守恒及转移电子守恒,易错选项是D.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 漂白粉的有效成分是Ca(ClO)2和CaCl2 | |
| B. | 漂白粉在空气中久置后会变质 | |
| C. | 漂白粉是由Cl2与烧碱制得的 | |
| D. | 在使用漂白粉时应用浓盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
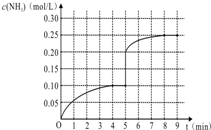 在一容积为1L的密闭容器内加入0.1mol的N2和0.3mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0,反应中NH3的物质的量浓度的变化情况如图:
在一容积为1L的密闭容器内加入0.1mol的N2和0.3mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0,反应中NH3的物质的量浓度的变化情况如图:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{{20M×{{10}^{-3}}}}{127}$g | B. | 20M g | C. | $\frac{{20×{{10}^{-3}}}}{M}$g | D. | $\frac{20}{M}$g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的化学方程式为CO+H2O$?_{高温高压}^{催化剂}$CO2+H2 | |
| B. | 该反应的焓变为正值 | |
| C. | 恒温恒容下,增大压强,H2浓度一定减小 | |
| D. | 升高温度,平衡右移,逆反应速率减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2可用作呼吸面具的供氧剂 | |
| B. | 侯德榜“联合制碱法”制取的是碳酸钠 | |
| C. | 钠与乙醇反应,钠块沉入试管底部 | |
| D. | NaHCO3的热稳定性大于Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15N中含有7个中子 | |
| B. | N2和N70属于同位素 | |
| C. | N5+中含有36个电子 | |
| D. | 若NH5为离子化合物,则其既含有离子键,又含有共价 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com