
【题目】常温下用NaOH溶液滴定H2C2O4溶液溶液中﹣lg![]() 和﹣lgc(HC2O4-)[或-lg
和﹣lgc(HC2O4-)[或-lg![]() 和﹣lgc(C2O42-)]的关系如图所示。下列说法正确的是( )
和﹣lgc(C2O42-)]的关系如图所示。下列说法正确的是( )

A. 曲线N表示-lg![]() 和﹣lgc(C2O42-)的关系
和﹣lgc(C2O42-)的关系
B. Ka1(H2C2O4)的数量级为10﹣1
C. 向NaHC2O4溶液中加少量NaOH至c(HC2O4﹣)和c(C2O42﹣)相等,此时溶液pH约为4
D. 在Na2C2O4和NaHC2O4物质的量为1:1的混合溶液中c(Na+)>c(C2O42﹣)>c(HC2O4﹣)>c(H2C2O4)>c(OH-)>c(H+)
【答案】A
【解析】
A.H2C2O4溶液存在H2C2O4HC2O4-+H+,HC2O4-C2O42-+H+,且Ka1(H2C2O4)=![]() ,Ka2=
,Ka2=![]() ,可知[-lg
,可知[-lg![]() +[-lg
+[-lg![]() ]=-lg(Ka1),[-lg
]=-lg(Ka1),[-lg![]() +[-lg
+[-lg![]() ]=-lg(Ka2),因Ka1>Ka2,则-lg(Ka1)< -lg(Ka2),可知曲线M表示-lg
]=-lg(Ka2),因Ka1>Ka2,则-lg(Ka1)< -lg(Ka2),可知曲线M表示-lg![]() 和-lg
和-lg![]() 的关系,曲线N表示-lg
的关系,曲线N表示-lg![]() 和-lg
和-lg![]() 的关系,A正确;
的关系,A正确;
B.当lg![]() =
=![]() ,[-lg
,[-lg![]() +[-lg
+[-lg![]() ]=-lg(Ka1)=2,Ka1(H2C2O4)=
]=-lg(Ka1)=2,Ka1(H2C2O4)=![]() =c(H+)=10-2,B错误;
=c(H+)=10-2,B错误;
C.向NaHC2O4溶液中加少量NaOH至c(HC2O4-)和c(C2O42-)相等,Ka2(H2C2O4)=![]() c(H+)=10-5,C错误;
c(H+)=10-5,C错误;
D.溶液的体积相等,由于二者的物质的量相等,所以c(NaHC2O4)、c(Na2C2O4)相等,Ka2=![]() = c(H+)=10-5,pH<5,溶液显酸性,c(H+)>c(OH-),D错误;
= c(H+)=10-5,pH<5,溶液显酸性,c(H+)>c(OH-),D错误;
故合理选项是A。


 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案科目:高中化学 来源: 题型:
【题目】对于反应N2O4(g)![]() 2NO2(g)在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点)
2NO2(g)在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点)

(1)B、C两点的反应速率的关系为B_________C(填“>”“<”或“=”)。
(2)当反应处于A状态时,V正_____V逆(填“>”“<”或“=”)
(3)由D状态转变为C状态后,混合气体的总物质的量会______(填“增大”、“减小”)。
(4)若在注射器中盛有一定量NO2,向内推活塞至原有体积的3/4,达到平衡时其中气体颜色较初始颜色如何变化_______,其原理为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 钠和钾的合金在常温下是液体,可用于快中子反应堆的热交换剂
B. 氯化铁、硫酸铁是优良的净水剂
C. 碳酸钡可作为检查肠胃的内服药剂,俗称“钡餐”
D. 乙醇可以直接作为燃料,也可以和汽油混合后作发动机燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需精确配制480mL0.100mol/L的CuSO4溶液,以下操作正确的是
A.称取7.68gCuSO4,配成500mL溶液
B.称取12.0g胆矾,配成500mL溶液
C.称取8.0gCuSO4,加入500mL水
D.称取12.5g胆矾,配成500mL溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应N2(g)+3H2(g) ![]() 2NH3(g )在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内NH3的反应速率为
2NH3(g )在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内NH3的反应速率为
A.1.2mol/(L·min)B.1.8mol/(L·min)
C.0.6mol/(L·min)D.0.4mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用作食品添加剂(抗结剂),我国卫生部规定实验中黄血盐的最大使用量为10mg/kg。一种制备黄雪盐的工艺如下:

回答下列问题:
(1)步骤Ⅰ反应的化学方程式为__________________________。
(2)步骤Ⅳ过滤所得的废液中含量较多的溶质为____________(填化学式)。
(3)步骤Ⅴ所用的试剂X是___________。(填化学式)
(4)工艺中用到剧毒的HCN溶液,含CN- 的废水必须处理后才能排放。
已知: HCN是一种具有苦杏仁味的无色剧毒液体,易挥发,25℃时Ka(HCN)=6.25×10-10;溶液中H2CO3、HCO3-、CO32-的存在与溶液pH的关系如图所示:
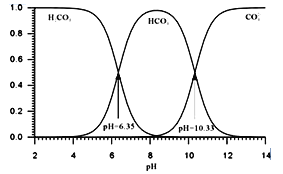
①NaCN的电子式为___________。
②处理含CN-废水的方法:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN-;第二步控制pH为7.5~8.5,用NaClO溶液完全氧化OCN-生成N2和两种盐。第一步控制强碱性的主要目的是_______,第二步反应的离子方程式为____________。
(5)已知蓝色染料普鲁士蓝的合成方法如下:

用硫酸亚铁碱性试纸可以检验食品中是否含有CN-,方案如下:

若试纸变蓝则证明食品中含有CN-,基于普鲁士蓝的合成原理,请解释检测时试纸变蓝的原因:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化硼(BCl3)是一种重要的化工原料。实验室制备BCl3的原理B2O3+3C+3Cl2 =2BCl3+3CO,某实验小组利用干燥的氯气和下列装置(装置可重复使用)制备BCl3并验证反应中有CO生成。已知:BCl3的熔点为-107.3℃,沸点为12.5℃,遇水水解生成H3BO3和HCl,请回答下列问题:
(实验Ⅰ)制备BCl3并验证产物CO

(1)该实验装置中合理的连接顺序为G→_____→_____→_____→____→F→D→I。其中装置E的作用是___________________________。
(2)装置J中反应的化学方程式为____________________________________。
(实验Ⅱ)产品中氯含量的测定
①准确称取少许m克产品,置于蒸馏水中完全水解,并配成100mL溶液。
②取10.00mL溶液于锥形瓶中
③加入V1mL浓度为C1 mol/LAgNO3溶液使氯离子完全沉淀;向其中加入少许硝基苯用力摇动。
④以硝酸铁为指示剂,用C2 mol/L KSCN标准溶液滴定过量的AgNO3溶液。发生反应:Ag+ +SCN- =AgSCN↓。
⑤重复步骤②~④二次,达到滴定终点时用去KSCN溶液的平均体积为V2 mL。
已知: Ksp(AgCl)>Ksp(AgSCN) 。
(3)步骤④中达到滴定终点的现象为__________________。
(4)实验过程中加入硝基苯的目的是___________________。
(5)产品中氯元素的质量分数为_________________%。
(6)下列操作,可能引起测得产品中氯含量偏高是__________。
A.步骤③中未加硝基苯
B.步骤①中配制100mL溶液时,定容时俯视刻度线
C.用KSCN溶液滴定剩余AgNO3溶液时,滴定前有气泡,滴定后无气泡
D.滴定剩余AgNO3溶液时,KSCN溶液滴到锥形瓶外面一滴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中,A为空气中常见的气体单质,B、C、E是金属单质,D为非金属单质。已知:①I是一种常见的温室气体,E原子核内有12个质子;②反应![]() 能放出大量的热,该反应曾应用于铁轨的焊接。回答下列问题:
能放出大量的热,该反应曾应用于铁轨的焊接。回答下列问题:

(1)分别写出A、F的化学式
A________;F ________。
(2)写出下列反应的化学方程式
C+G![]() B+H______________
B+H______________
2E+I![]() 2F+D_____________
2F+D_____________
(3)C与NaOH溶液反应的离子方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分短周期(即原子序数为1~18号)元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | M层上的电子数等于其内层电子数的差值 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下其单质为双原子分子,且占空气中的含量最大 |
Z | 该元素的某种含氧酸具有漂白性 |
(1)按要求用有关的化学用语填充:
T元素的离子符号:______;Y离子的电子式__________;Z离子的结构示意图_______________;
(2)元素Y与氢元素能形成一种10电子的阳离子,该微粒符号是____________;
(3)写出元素T的最高价含氧酸与X的最高价含氧酸对应的钠盐反应的化学方程式____
(4)元素Z与某一活泼金属元素组成的盐是重要的化工原料,写出其作为该原料在化工生产上电解的一个重要反应:______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com