
【题目】卤代烃在碱性醇溶液中能发生消去反应。
例如,![]()
该反应式也可表示为
下面是几种有机化合物的转化关系:

(1)根据系统命名法,化合物A的名称是_____________。
(2)反应①的反应类型_________,反应③的反应类型___________
(3)化合物E是重要的工业原料,写出由D生成E的化学方程式:_______。
(4)C2的结构简式是______________,F1的结构简式是______________,F1与F2互为__________。
【答案】2,3-二甲基丁烷 取代反应 加成反应 CH3CBr(CH3)CBr(CH3)2+2NaOH![]() CH2=C(CH3)C(CH3)=CH2+2NaBr+2H2O (CH3)2C=C(CH3)2 BrCH2C(CH3)=C(CH3)CH2Br 同分异构体
CH2=C(CH3)C(CH3)=CH2+2NaBr+2H2O (CH3)2C=C(CH3)2 BrCH2C(CH3)=C(CH3)CH2Br 同分异构体
【解析】
A在光照条件下与氯气发生取代反应生成B,B在氢氧化钠醇溶液、加热条件下发生消去反应生成C1、C2,C2与溴发生加成反应生成D,D在氢氧化钠醇溶液、加热条件下发生消去反应生成E,E与溴可以发生1,2-加成反应生成F2,发生1,4-加成反应生成F1,则E为CH2=C(CH3)C(CH3)=CH2、F2为CH2=C(CH3)CBr(CH3)CH2Br,F1为BrCH2C(CH3)=C(CH3)CH2Br.逆推可得D为CH3CBr(CH3)CBr(CH3)2,C2为(CH3)2C=C(CH3)2,C1为(CH3)2CHC(CH3)=CH2。据此分析解答。
(1)由化合物A的结构简式,名称是:2,3-二甲基丁烷,故答案为:2,3-二甲基丁烷;
(2)上述框图中,反应①属于取代反应,反应③属于加成反应,故答案为:取代反应;加成反应;
(3)根据以上分析,D生成E的化学方程式:CH3CBr(CH3)CBr(CH3)2+2NaOH![]() CH2=C(CH3)C(CH3)=CH2+2NaBr+2H2O,故答案为:CH3CBr(CH3)CBr(CH3)2+2NaOH
CH2=C(CH3)C(CH3)=CH2+2NaBr+2H2O,故答案为:CH3CBr(CH3)CBr(CH3)2+2NaOH![]() CH2=C(CH3)C(CH3)=CH2+2NaBr+2H2O;
CH2=C(CH3)C(CH3)=CH2+2NaBr+2H2O;
(4)根据以上分析,C2的结构简式是:(CH3)2C=C(CH3)2,F1的结构简式是:BrCH2C(CH3)=C(CH3)CH2Br,F2的结构简式是:CH2=C(CH3)CBr(CH3)CH2Br,F1与F2互为同分异构体,故答案为:(CH3)2C=C(CH3)2;BrCH2C(CH3)=C(CH3)CH2Br;同分异构体。


科目:高中化学 来源: 题型:
【题目】下列反应中,离子方程式书写正确的是( )
A. 氢氧化钡与盐酸反应: OH—+H+=H2O
B. Fe和盐酸反应:2Fe+6H+=2Fe3++3H2↑
C. Cu和AgNO3溶液反应:Cu+Ag+=Cu2++Ag
D. 石灰石和盐酸反应:CO32—+2H+=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
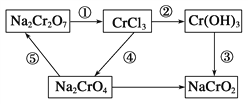
【题目】(1)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:在如图有编号的步骤中,发生氧化反应的是_________(填编号,下同),发生还原反应的是___________ 。(提示:铬元素化合价有+6、+3价)
(2)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10A1+6NaNO3+4NaOH==10NaA1O2+3N2↑+2H2O。请回答下列问题:
①其中被还原的元素是________ ,氧化剂是__________ ,还原剂是_________ ,氧化产物是__________ ,还原产物是__________。
②表示反应中电子转移的方向和数目:__________。
10 A1 + 6 NaNO3 + 4 NaOH == 10 NaA1O2 + 3 N2↑ + 2 H2O
(3)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2Fe3++Cu═2Fe2++Cu2+的拆写结果是:氧化反应为:Cu-2e-═Cu2+;还原反应为:2Fe3++2e-═2Fe2+。
请据此将反应:Fe+2H+===Fe2++H2↑拆写成两个“半反应式”:氧化反应为____________________;还原反应为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】处理高浓度乙醛废水的新方法一隔膜电解法,让乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸。实验室以一定浓度的乙醛一Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。下列说法正确的是
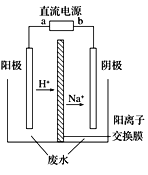
A. 若以CH4一空气燃料电池为直流电源,燃料电池的a极应通入甲烷
B. 电解过程中,阴极区Na2SO4的物质的量增大
C. 阳极反应为CH3CHO-2e-+H2O=CH3COOH+2H+
D. 阴极还原产物H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体是一种常见的分散系,回答下列问题。
(1)向煮沸的蒸馏水中逐滴加入____________溶液,继续煮沸至__________________,停止加热,可制得Fe(OH)3胶体。
(2)向Fe(OH)3胶体中加入Na2SO4饱和溶液,主要由于________(填离子符号)的作用,使胶体形成了沉淀,这个过程叫作________________。
(3)区分胶体和溶液常用的方法叫作______________,这是因为胶体粒子对光线的________作用而形成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
①标准状况下,0.2 mol任何物质的体积均为4.48 L ②若1 mol气体的体积为22.4 L,则它一定处于标准状况下 ③标准状况下,1 L HCl和1 L H2O的物质的量相同 ④标准状况下,1 g H2和14 g N2的体积相同 ⑤28 g CO的体积为22.4 L ⑥两种物质的物质的量相同,则它们在标准状况下的体积也相同 ⑦在同温同体积时,气体物质的物质的量越大,则压强越大 ⑧同温同压下,气体的密度与气体的相对分子质量成正比
A. ①②③④ B. ②③⑥⑦⑧ C. ⑤⑥⑦⑧ D. ④⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源与人类的生活和社会发展密切相关,下列有关说法不正确的是( )
A.用植物秸秆生产酒精代替汽油作汽车燃料
B.实行垃圾分类回收,将垃圾中的生物质能转化为热能
C.在农村提倡利用沼气作生活燃料
D.人类利用的能源都是通过化学反应获得的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常状况下,CO是一种无色、无味、有毒的气体,难溶于水,与酸、碱、盐溶液均不反应。已知乙二酸晶体加热分解的方程式为:H2C2O4·2H2O![]() 3H2O+CO2↑+CO↑,不考虑其他因素干扰,如何利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。酒精喷灯可作高温热源。请回答下列问题:
3H2O+CO2↑+CO↑,不考虑其他因素干扰,如何利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。酒精喷灯可作高温热源。请回答下列问题:

(1)检验装置A气密性的方法是
(2)按气流方向连接各仪器,用数字表示接口的连接顺序:
①→
(3)证明CO存在的实验现象是
(4)本实验尾气处理的方法是
(5)根据题给的数据,假设各反应均充分发生且产生的气体全部排出,并与吸收液充分反应(提示:B、C中澄清石灰水均先变浑浊,后又变澄清),D中溶质及对应的物质的量是: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com