
【题目】按要求完成下列问题:
(1)下列各化合物中,属于同系物的是_____,属于同分异构体的是___填入编号

![]()
F.戊烯和环戊烷
(2)反—2-丁烯的结构简式_________________________;
(3)2,6–二甲基–4–乙基辛烷的结构简式:_______;1mol该有机物完全燃烧耗氧气_______________mol。
(4) CH3-CH(C2H5) – C(C2H5)=CH-CH3的系统命名的名称为___________________;
(5)某烷烃分子里含有9个碳原子,且其一氯代物只有2种,则该烷烃的系统命名的名称是______。
(6)  单体的结构简式________________。
单体的结构简式________________。
【答案】BE AF 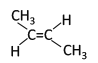
![]() 18.5mol 4-甲基-3-乙基-2-己烯 2,2,4,4-四甲基戊烷(或3,3—二乙基戊烷)
18.5mol 4-甲基-3-乙基-2-己烯 2,2,4,4-四甲基戊烷(或3,3—二乙基戊烷) ![]() CH2=CH-CH=CH2
CH2=CH-CH=CH2
【解析】
(1)同系物是指结构相似,分子组成相差1个或若干个-CH2基团的有机物的互称。同分异构体是分子式相同结构不同的有机物的互称。(2)反—2-丁烯中只有一个碳碳双键, 且碳碳双键在第二个碳原子和第三个碳原子之间, 反式结构两个甲基不在双键的同一侧;(3)根据烷烃的命名原则写出该有机物的结构简式;根据该有机物的结构简式写出分子式,然后计算出完全燃烧消耗的氧气的物质的量。(4)根据烯烃的命名原则对该有机物进行命名;(5)烷烃的一个分子里含有9个碳原子,该烷烃的分子式为C9H20,其一氯代物只有两种,则结构对称,只有2种位置的H原子,结构简式为:(CH3)3CCH2C(CH3)3或C(CH2CH3)4;(6)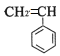 与CH2=CH-CH=CH2能发生加聚反应生成
与CH2=CH-CH=CH2能发生加聚反应生成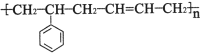 。
。
(1)![]() 与
与![]() 分子式都是
分子式都是![]() ,结构不同;
,结构不同;![]() 与
与![]() 结构相似,分子组成相差1个-CH2基团;
结构相似,分子组成相差1个-CH2基团;![]() 属于酚,
属于酚,![]() 属于醇,
属于醇,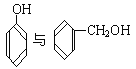 结构不同;
结构不同;![]() 有2个羟基,
有2个羟基,![]() 含有3个羟基,
含有3个羟基,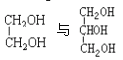 结构不同;
结构不同;![]() 都含有2个羧基,分子组成相差2个-CH2基团;戊烯和环戊烷结构不同、分子式都是
都含有2个羧基,分子组成相差2个-CH2基团;戊烯和环戊烷结构不同、分子式都是![]() 。同系物是指结构相似,分子组成相差1个或若干个-CH2基团的有机物的互称,所以BE属于同系物。同分异构体是分子式相同结构不同的有机物的互称,所以AF属于同分异构体。 (2)反—2-丁烯中只有一个碳碳双键, 且碳碳双键在第二个碳原子和第三个碳原子之间, 反式结构两个甲基不在双键的同一侧,结构简式是
。同系物是指结构相似,分子组成相差1个或若干个-CH2基团的有机物的互称,所以BE属于同系物。同分异构体是分子式相同结构不同的有机物的互称,所以AF属于同分异构体。 (2)反—2-丁烯中只有一个碳碳双键, 且碳碳双键在第二个碳原子和第三个碳原子之间, 反式结构两个甲基不在双键的同一侧,结构简式是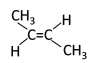 ;(3)2,6-二甲基-4-乙基辛烷,主链为辛烷,在2、6号C各含有1个甲基,在4号C含有1个乙基,该有机物结构简式为:
;(3)2,6-二甲基-4-乙基辛烷,主链为辛烷,在2、6号C各含有1个甲基,在4号C含有1个乙基,该有机物结构简式为:![]() ;根据其结构简式可知该有机物分子式为:C12H26,1mol该有机物完全燃烧消耗的氧气的物质的量为:(12+
;根据其结构简式可知该有机物分子式为:C12H26,1mol该有机物完全燃烧消耗的氧气的物质的量为:(12+![]() )mol=18.5mol;(3)CH3-CH(C2H5) – C(C2H5)=CH-CH3含有碳碳双键为烯烃,含有双键的最长链上有6个碳为己烯,从离双键近的一端给碳原子编号,2、3号碳原子之间有双键,3号碳原子连有乙基、4号碳原子连有甲基,所以该烯烃的名称是:4-甲基-3-乙基-2-己烯;(5)烷烃的一个分子里含有9个碳原子,该烷烃的分子式为C9H20,其一氯代物只有两种,则结构对称,只有2种位置的H原子,结构简式为:(CH3)3CCH2C(CH3)3或C(CH2CH3)4,名称是2,2,4,4-四甲基戊烷或3,3—二乙基戊烷;(6)
)mol=18.5mol;(3)CH3-CH(C2H5) – C(C2H5)=CH-CH3含有碳碳双键为烯烃,含有双键的最长链上有6个碳为己烯,从离双键近的一端给碳原子编号,2、3号碳原子之间有双键,3号碳原子连有乙基、4号碳原子连有甲基,所以该烯烃的名称是:4-甲基-3-乙基-2-己烯;(5)烷烃的一个分子里含有9个碳原子,该烷烃的分子式为C9H20,其一氯代物只有两种,则结构对称,只有2种位置的H原子,结构简式为:(CH3)3CCH2C(CH3)3或C(CH2CH3)4,名称是2,2,4,4-四甲基戊烷或3,3—二乙基戊烷;(6) 与CH2=CH—CH=CH2能发生加聚反应生成
与CH2=CH—CH=CH2能发生加聚反应生成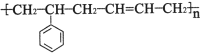 ,所以
,所以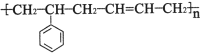 的单体是
的单体是![]() 和CH2=CH-CH=CH2。
和CH2=CH-CH=CH2。


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
【题目】常温下,向1L0.1mol·L-1NH4Cl溶液中不断加入固体NaOH后,NH4+与NH3·H2O的变化趋势如右图所示(不考虑体积变化和氨的挥发),下列说法不正确的是( )

A. M点溶液中水的电离程度比原溶液小
B. 在M点时,n(OH-)-n(H+)=(a-0.05)mol
C. 随着NaOH的加入,![]() 不断增大
不断增大
D. 当n(NaOH)=0.05mo1时,溶液中有:c(Cl-)> c(NH4+)>c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5,表示,咸水中的主要溶质为NaCl。下列有关说法正确的是

A. a为原电池的负极
B. b电极附近溶液的pH减小
C. a电极反应式为![]()
D. 中间室:Na+移向左室,Cl-移向右室
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生课外活动小组的同学设计下图所示实验装置,用来验证一氧化碳具有还原性,回答下列问题:

(1)写出装置A中所发生反应的离子方程式:__________。
(2)装置B中最适宜的试剂是_________________。
(3)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是_______。
(4)根据实验中的___________________现象,可证明CO具有还原性。
(5)若要根据装置F中澄清石灰水变浑浊的现象确认一氧化碳具有还原性,应在上图装置________与______之间连接下图中的________装置(填序号)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四个反应
①2Na+2H2O=2NaOH+H2↑ ②2F2+2H2O=4HF+O2
③Cl2+H2O=HCl+HClO ④C+H2O(g)![]() CO+H2
CO+H2
试从氧化还原的角度,回答下列问题:
(1)水只作还原剂的是__________________(填序号)
(2)二氧化氯(ClO2)是一种在水处理方面有广泛应用的高效安全消毒剂,而且不会产生对人体有潜在危害的物质。工业上可以用如下方法制备ClO2:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O。反应中氧化剂是____________,生成1.25mol氧化产物共转移电子_________mol。写出该反应的离子方程式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四种粒子中,半径按由大到小排列顺序正确的是
①基态X的原子结构示意图
②基态Y的价电子排布式:3s23p5
③基态Z2-的电子排布图![]()
④W基态原子有2个能层,电子式为![]()
A. ①>②>③>④ B. ③>④>①>②
C. ③>①>②>④ D. ①>②>④>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢材在社会发展中应用广泛。为研究某种碳索钢(含少量碳和硫)的成分,科研小组进行了如下探究活动。
称取碳素钢(已除表面氧化物)24.0g放入耐高温反应管中与O2反应,除去未反应的O2,收集到干燥混合气体X 1.12L(已折算成标准状况下的体积)。
(1)科研小组用下图所示实验装置检验混合气体X的组成。

①装置B中的试剂是___________,装置C的作用是_________。
②若观察到________(填实验现象),证明X中含有CO。
(2)反应后,耐高温反应管内固体中除含有Fe3+之外,还可能含有Fe2+。要确定其中的Fe2+,可选用_______(填序号)。
a.KSCN溶液和氯水 b.KSCN溶液和铁粉
c.稀盐酸和K3[Fe(CN)6]溶液 d.稀H2SO4和KMnO4溶液
(3)科研小组用下图所示装置(部分)测定SO2的体积分数,并计算碳素钢的含碳量。将气体X缓慢通过实验装置,当观察到_____(填实验现象)时,停止通气,此时气体流量仪显示的流量为112mL(已换算成标准状况)。则气体X中SO2的体积分数为_____,碳素钢中碳元素的质量分数为_________(保留1位小数)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiAlH4是金属储氢材料,遇水剧烈反应释放出H2,LiAlH4在125℃时分解为LiH、H2和Al。下列说法正确的是( )
A.LiAlH4中Al的化合价为-5价
B.LiAlH4与水反应时,LiAlH4作还原剂
C.LiAlH4在125℃时完全分解,每生成2mol H2,转移电子数2NA个
D.LiH是反应的还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铅蓄电池的工作原理为Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。

(1)A是铅蓄电池的___________极,铅蓄电池正极反应式为___________,放电过程中电解液的密度___________ (填“减小”、“增大”或“不变”)。
(2)Ag电极的电极反应式是___________,该电极的电极产物共____________g。
(3)Cu电极的电极反应式是____________,CuSO4溶液的浓度____________(填“减小”、“增大”或“不变”)
(4)如图表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示___________。

a.各U形管中产生的气体的体积
b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com