
| ||
| A、②③⑤ | B、①④⑤ |
| C、①③⑤ | D、②④⑤ |
| ||


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
| A、降温 |
| B、加入CaSO4 |
| C、加入BaCl2 |
| D、加水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2SO4 |
| B、CH3COOH |
| C、NaOH |
| D、CH3COOK |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢管与电源正极连接,钢管可被保护 |
| B、铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀 |
| C、钢管与铜管露天堆放在一起时,钢管不易被腐蚀 |
| D、钢铁发生析氢腐蚀时,负极反应是2H++2e-═H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、只有③ | C、②④ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
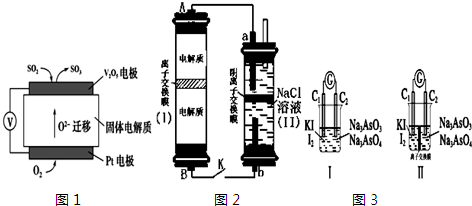
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由于水中存在氢键,所以稳定性:H2O>H2S |
| B、由于磷化氢的相对分子质量比氨气的大,所以沸点:PH3>NH3 |
| C、若A2+2D-═2A-+D2,则氧化性D2>A2 |
| D、若R2-和M+的电子层结构相同,则离子半径R2->M+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
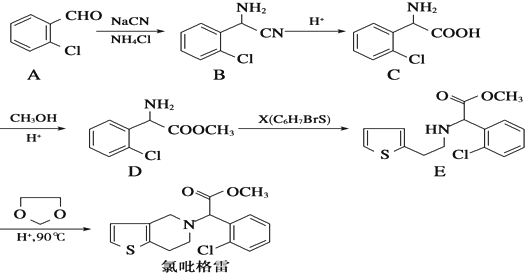
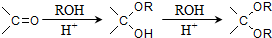
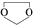 ,需要经历的反应类型有
,需要经历的反应类型有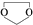 的最后一步反应
的最后一步反应查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com