
 ĄūÓĆ·ĻĀĮ²£ØÖ÷ŅŖ³É·ÖĪŖAl”¢ÉŁĮæµÄFe”¢SiµČ£©¼ČæÉÖĘȔӊ»śŗĻ³É“߻ƼĮAlBr3ÓÖæÉÖĘČ”¾»Ė®¼ĮĮņĖįĀĮ¾§Ģå[A12£ØSO4£©3•18H2O]£®
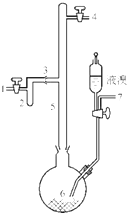
ĄūÓĆ·ĻĀĮ²£ØÖ÷ŅŖ³É·ÖĪŖAl”¢ÉŁĮæµÄFe”¢SiµČ£©¼ČæÉÖĘȔӊ»śŗĻ³É“߻ƼĮAlBr3ÓÖæÉÖĘČ”¾»Ė®¼ĮĮņĖįĀĮ¾§Ģå[A12£ØSO4£©3•18H2O]£®·ÖĪö £Ø1£©ĀĮ²±ķĆę»įÓŠÓĶĪŪ£¬øł¾ŻĻąĖĘĻąČÜŌĄķÖŖ£¬ÓŠ»śČÜÖŹŅ×ČÜÓŚÓŠ»śČܼĮ£»
£Ø2£©äå»ÆĀĮŅ×Ė®½āÉś³ÉĒāŃõ»ÆĀĮŗĶHBr£»
£Ø3£©ŹµŃéĄūÓĆÕōĮó·½·ØµĆµ½äå»ÆĀĮ£¬Čē¹ūäå¹żĮ棬äåŅ×»ģČėäå»ÆĀĮÖŠ£»
£Ø4£©äåĶźČ«·“Ó¦ŗó£¬5µÄ¹ÜÖŠ»ŲĮ÷Ņŗ³ŹĪŽÉ«»ņÉÕĘæ6ÖŠĪļÖŹ³ŹĪŽÉ«£»
£Ø5£©½«äå»ÆĀĮÕōĘūµ¼Čė×°ÖĆ2ÖŠ²¢ĄäÄżµĆµ½äå»ÆĀĮ£®
½ā“š ½ā£ŗ£Ø1£©ĀĮ²±ķĆęŅ×Õ“ÓŠÓĶÖ¬£¬øł¾ŻĻąĖĘĻąČÜŌĄķÖŖ£¬ÓŠ»śČÜÖŹŅ×ČÜÓŚÓŠ»śČܼĮ£¬ĖłŅŌÓĆĖÄĀČ»ÆĢ¼³żČ„ĀĮ²±ķĆęµÄÓĶÖ¬£¬
¹Ź“š°øĪŖ£ŗ³żČ„ĀĮ²±ķĆęµÄÓĶÖ¬µČÓŠ»śĪļ£»
£Ø2£©äå»ÆĀĮŅ×Ė®½āÉś³ÉĒāŃõ»ÆĀĮŗĶHBr£¬ĪŖ·ĄÖ¹äå»ÆĪļŌŚæÕĘųÖŠµÄĖ®ÕōĘųÖŠĖ®½ā£¬ÓƵŖĘų½«Ė®ÕōĘųÅųö£¬
¹Ź“š°øĪŖ£ŗÅųö×°ÖĆÖŠŗ¬ÓŠĖ®ÕōĘųµÄæÕĘų£»
£Ø3£©ŹµŃéĄūÓĆÕōĮó·½·ØµĆµ½äå»ÆĀĮ£¬Čē¹ūäå¹żĮ棬äåŅ×»ģČėäå»ÆĀĮÖŠ£¬ĖłŅŌĪŖ±£Ö¤ŅŗäåĶźČ«·“Ó¦£¬øĆŹµŃéŅŖ±£Ö¤ÉÕĘæÖŠĀĮ²¹żŹ££¬
¹Ź“š°øĪŖ£ŗ±£Ö¤äåĶźČ«·“Ó¦£¬·ĄÖ¹äå¹żĮæ»ģČėäå»ÆĀĮÖŠ£»
£Ø4£©µ±5µÄ¹ÜÖŠ»ŲĮ÷Ņŗ³ŹĪŽÉ«»ņÉÕĘæ6ÖŠĪļÖŹ³ŹĪŽÉ«£¬ĖµĆ÷äåĒ”ŗĆĶźČ«·“Ó¦£¬ŌņæÉŅŌĶ£Ö¹»ŲĮ÷£¬
¹Ź“š°øĪŖ£ŗµ±5µÄ¹ÜÖŠ»ŲĮ÷Ņŗ³ŹĪŽÉ«»ņÉÕĘæ6ÖŠĪļÖŹ³ŹĪŽÉ«£»
£Ø5£©²½Öč5Šč“ņæŖµ¼¹ÜæŚlŗĶ4£¬ĄūÓĆŃ¹Ēæ²ī½«äå»ÆĀĮÕōĘūµ¼Čė×°ÖĆ2²¢ĄäÄżµĆµ½äå»ÆĀĮ£¬
¹Ź“š°øĪŖ£ŗ½«äå»ÆĀĮÕōĘūµ¼Čė×°ÖĆ2ÖŠ²¢ĄäÄżµĆµ½äå»ÆĀĮ£®
µćĘĄ ±¾Ģāæ¼²éÖʱøŹµŃé·½°øÉč¼Ę£¬²ąÖŲæ¼²éѧɜ¶ŌŹµŃé²Ł×÷µÄ·ÖĪöĘĄ¼Ū£¬ŹĒ¶Ōѧɜ×ŪŗĻÄÜĮ¦µÄ漲飬ÄѶČÖŠµČ£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2.24L | B£® | 4.48L | C£® | 6.72L | D£® | 7.84 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4+ | B£® | Mg2+ | C£® | Cu2+ | D£® | Fe3+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 4ÖÖ | B£® | 5ÖÖ | C£® | 6ÖÖ | D£® | 7ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌĖÓĆĖ®²£Į§¶ĀČū¹ÜµĄ£¬ŹĒŅņĪŖĖ®²£Į§ĻŌ¼īŠŌ | |
| B£® | ÅäÖʵāĖ®Ź±£¬³£¼ÓČėÉŁĮæµÄKI£¬ÄæµÄŹĒ·ĄÖ¹I2±»»¹Ō | |
| C£® | ÓĆĖį»ÆµÄøßĆĢĖį¼ŲÓėH2O2æÉÖĘȔɣĮæŃõĘų£¬KMnO4×÷“߻ƼĮ | |
| D£® | Ć÷·Æ[KAl£ØSO4£©2•12H2O]¾»Ė®ŗĶŅŗĀČ£ØCl2£©¾»Ė®µÄŌĄķ²»ĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
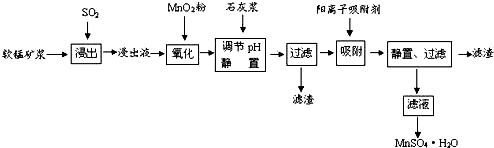

| Ąė×Ó | Ąė×Ó°ė¾¶£Øpm£© | æŖŹ¼³ĮµķŹ±µÄpH | ĶźČ«³ĮµķŹ±µÄpH |
| Fe2+ | 74 | 7.6 | 9.7 |
| Fe3+ | 64 | 2.7 | 3.7 |
| Al3+ | 50 | 3.8 | 4.7 |
| Mn2+ | 80 | 8.3 | 9.8 |
| Pb2+ | 121 | 8.0 | 8.8 |
| Ca2+ | 99 | - | - |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | »ģŗĻĘųĢåÖŠŅ»¶ØÓŠ¼×Ķé | B£® | »ģŗĻĘųĢåÖŠŅ»¶ØŹĒ¼×ĶéŗĶŅŅĻ© | ||
| C£® | »ģŗĻĘųĢåÖŠŅ»¶ØƻӊŅŅĶé | D£® | »ģŗĻĘųĢåÖŠŅ»¶ØÓŠŅŅČ² |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com