
 元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.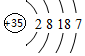 ,碘是紫黑色(填颜色)固体物质.(2)牙齿的损坏实际上是牙釉质羟基磷灰石[Ca5(PO4)3OH]溶解的结果,糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿.使用含氟牙膏会保护牙齿,因为氟离子会跟羟基磷灰石[Ca5(PO4)3OH]发生反应生成氟磷灰石,氟磷灰石比羟基磷灰石更能抵抗酸的侵蚀氟,用离子方程式表示这一过程Ca5(PO4)3OH(S)+F- (aq)?Ca5(PO4)3 F(S)+OH-(aq).此外氟离子还能抑制口腔细菌产生酸,含氟牙膏已经普遍使用.
,碘是紫黑色(填颜色)固体物质.(2)牙齿的损坏实际上是牙釉质羟基磷灰石[Ca5(PO4)3OH]溶解的结果,糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿.使用含氟牙膏会保护牙齿,因为氟离子会跟羟基磷灰石[Ca5(PO4)3OH]发生反应生成氟磷灰石,氟磷灰石比羟基磷灰石更能抵抗酸的侵蚀氟,用离子方程式表示这一过程Ca5(PO4)3OH(S)+F- (aq)?Ca5(PO4)3 F(S)+OH-(aq).此外氟离子还能抑制口腔细菌产生酸,含氟牙膏已经普遍使用.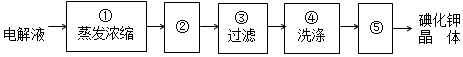
分析 (1)氯元素同族的下一周期元素的原子为溴原子,原子序数为35,核外电子分四层排布,据此画出原子结构示意图;碘单质为紫黑色固体;
(2)Ca5(PO4)3(OH)生成Ca5(PO4)3F,反应后同时生成OH-;
(3)在酸性条件碘酸根离子和碘离子发生氧化反应生成碘单质;
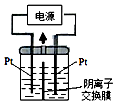
(4)①左侧溶液变蓝色,生成I2,左侧电极为阳极,电极反应为:2I--2e-=I2,右侧电极为阴极,电极反应式为:2H2O+2e-=H2↑+2OH-,右侧放出氢气,右侧I-、OH-通过阴离子交换膜向左侧移动,发生反应3I2+6OH-=IO3-+5I-+3H2O,一段时间后,蓝色变浅,保证两边溶液呈电中性,左侧的IO3-通过阴离子交换膜向右侧移动,如果用阳离子交换膜代替阴离子交换膜,左侧多余K+通过阳离子交换膜迁移至阴极,保证两边溶液呈电中性;
②从热溶液中析出晶体的方法是冷却结晶;洗涤后的晶体要进行干燥;洗涤晶体的目的:洗去吸附在碘酸钾晶体上的氢氧化钾等杂质;
(5)①淀粉遇到碘变蓝,依据I2+2S2O32-═S4O62-+2I-可知,当Na2S2O3标准溶液刚好将碘全部反应,淀粉由蓝色变成无色,据此解答;
②CuCl2溶液与KI反应实质铜离子氧化碘离子生成生成碘化亚铜沉淀和单质碘;
③依据碘单质被Na2S2O3标准溶液滴定到终点,发生反应离子方程式得到 2Na2S2O3~2Cu2+计算.
解答 解:(1)氯元素同族的下一周期元素的原子为溴原子,原子序数为35,原子结构示意图为 ,碘单质为紫黑色固体,
,碘单质为紫黑色固体,
故答案为: ; 紫黑色;
; 紫黑色;
(2)由题意氟离子会跟羟基磷灰石[Ca5(PO4)3OH]发生反应生成氟磷灰石可知,反应离子方程式为Ca5(PO4)3OH(S)+F- (aq)?Ca5(PO4)3 F(S)+OH-(aq),
故答案为:Ca5(PO4)3OH(S)+F- (aq)?Ca5(PO4)3 F(S)+OH-(aq);
(3)在酸性条件碘酸根离子和碘离子发生氧化反应生成碘单质,离子方程式为:IO3-+5I-+6H+=3I2+3H2O,
故答案为:IO3-+5I-+6H+═3H2O+3I2;
(4)①A.左侧溶液变蓝色,生成I2,左侧电极为阳极,右侧电极为阴极,电极反应式为:2H2O+2e-=H2↑+2OH-,故A正确;
B.一段时间后,蓝色变浅,发生反应3I2+6OH-=IO3-+5I-+3H2O,中间为阴离子交换膜,右侧I-、OH-通过阴离子交换膜向左侧移动,保证两边溶液呈电中性,左侧的IO3-通过阴离子交换膜向右侧移动,故右侧溶液中含有IO3-,故B正确;
C.左侧电极为阳极,电极反应为:2I--2e-=I2,同时发生反应3I2+6OH-=IO3-+5I-+3H2O,右侧电极为阴极,电极反应式为:2H2O+2e-=H2↑+2OH-,故总的电极反应式为:KI+3H2O$\frac{\underline{\;电解\;}}{\;}$KIO3+3H2↑,故C正确;
D.用阴离子交换膜,电解槽内发生的总化学方程式为:KI+3H2O$\frac{\underline{\;电解\;}}{\;}$KIO3+3H2↑,如果用阳离子交换膜代替阴离子交换膜,左侧电极为阳极,电极反应为:2I--2e-=I2,右侧电极为阴极,电极反应式为:2H2O+2e-=H2↑+2OH-,保证两边溶液呈电中性,左侧多余K+通过阳离子交换膜迁移至阴极,左侧生成I2,右侧溶液中有KOH生成,碘单质与KOH不能反应,总反应相当于:2KI+2H2O$\frac{\underline{\;电解\;}}{\;}$2KOH+I2+H2↑,故D正确;
故答案为:ABCD;
②从热溶液中析出晶体的方法是:冷却结晶;洗涤后的晶体有水分,所以要进行干燥;过滤后得到的晶体上吸附部分氢氧化钾等杂质,为得到较纯净的碘酸钾晶体,所以要进行洗涤,据此可知步骤⑤的操作名称为干燥,
故答案为:干燥;
(5)①淀粉遇到碘变蓝,依据I2+2S2O32-═S4O62-+2I-可知,当Na2S2O3标准溶液刚好将碘全部反应,淀粉由蓝色变成无色,所以可以淀粉做指示剂,当淀粉由蓝色变成无色且半分钟不变化滴定达到终点;
故答案为:淀粉溶液; 滴最后一滴硫代硫酸钠时,溶液蓝色褪去,半分钟内不恢复;
②CuCl2溶液与KI反应实质铜离子氧化碘离子生成生成碘化亚铜沉淀和单质碘,离子方程式:2Cu2++4I-=2CuI↓+I2;
故答案为:2Cu2++4I-=2CuI↓+I2;
③依据2Na2S2O3+I2═Na2S4O6+2NaI,2Cu2++4I-=2CuI↓+I2;
得到 2Na2S2O3~2Cu2+
2 2
试样中CuCl2•2H2O的物质的量为b mL×c mol/L,
试样中CuCl2•2H2O的质量百分数=$\frac{171bc×1{0}^{-3}}{a}$×100%,
故答案为:$\frac{171bc×1{0}^{-3}}{a}$×100%.
点评 本题考查了碘的物理性质、电解原理、碘离子的检验等性质,为高频考点,题目难度中等,涉及物质分离和提纯、基本实验操作计算等知识点,侧重分析与实验能力的考查.


科目:高中化学 来源: 题型:解答题
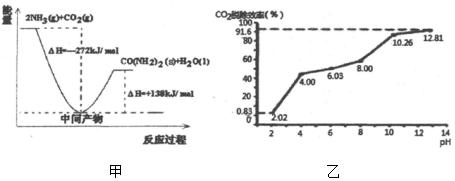
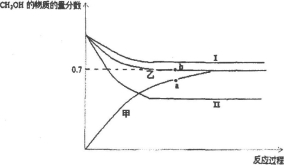
| 容器 | 甲 | 乙 | 丙 |
| 起始反应物投入量 | 2molH2、1molCO | 1molCH3OH | 2mol CH3OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3Cl | B. | CHCl3 | C. | CCl4 | D. | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丁烷有3种同分异构体 | |
| B. | 己烷共有5种同分异构体,它们的熔、沸点各不相同 | |
| C. | “可燃冰”的主要成分是甲烷和水 | |
| D. | 多氯代甲烷常为有机溶剂,其中分子结构为正四面体的是四氯化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
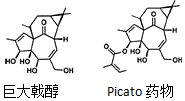 2016 年化学领域重要成果之一是丹麦制药公司LEO Pharma与美国斯克里普斯研究所(The Scripps Research Institute)的Phil S.Baran课题组合作,成功地将合成巨大戟醇(一个分子中含有20个碳原子)的步骤由37步缩短至14步.巨大戟醇是合成治疗日光性角化病药物(Picato)的原料.下列说法错误的是( )
2016 年化学领域重要成果之一是丹麦制药公司LEO Pharma与美国斯克里普斯研究所(The Scripps Research Institute)的Phil S.Baran课题组合作,成功地将合成巨大戟醇(一个分子中含有20个碳原子)的步骤由37步缩短至14步.巨大戟醇是合成治疗日光性角化病药物(Picato)的原料.下列说法错误的是( )| A. | 由巨大戟醇制备Picato药物的另一种反应物是(CH3)2C=CHCOOH | |
| B. | 巨大戟醇能发生取代反应、氧化反应、加成反应 | |
| C. | 巨大戟醇和Picato药物都不属于芳香族化合物 | |
| D. | 0.1mol巨大戟醇完全燃烧消耗2.45molO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
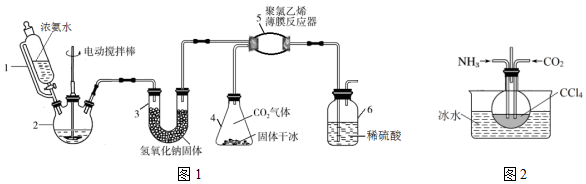
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 1mol苹果酸与足量金属Na反应生成生成lmolH2 | |
| B. | 1mol苹果酸可与3molNaOH发生中和反应 | |
| C. | 苹果酸中能发生酯化反应的官能团有2种 | |
| D. |  与苹果酸互为同分异构体 与苹果酸互为同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com