
(12·Ö)ŅŃÖŖ25”ꏱ²æ·ÖČõµē½āÖŹµÄµēĄėĘ½ŗā³£ŹżŹż¾ŻČēĻĀ±ķ£ŗ
|
»ÆѧŹ½ |
CH3COOH |
H2CO3 |
HClO |
|
Ę½ŗā³£Źż |
Ka=1.8”Į10-5 |
Ka1=4.3”Į10-7
Ka2=5.6”Į10-11 |
Ka=3.0”Į10-8 |
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ĪļÖŹµÄĮæÅØ¶Č¾łĪŖ0.1mol•L-1µÄĖÄÖÖČÜŅŗ£ŗ
A”¢CH3COOH B”¢Na2CO3 C”¢NaClO D”¢NaHCO3£»
pHÓÉŠ”µ½“óµÄÅÅĮŠĖ³ŠņŹĒ ;£ØÓĆ×ÖÄø±ķŹ¾£©
£Ø2£©³£ĪĀĻĀ£¬0.1mol•L-1µÄCH3COOHČÜŅŗ¼ÓĖ®Ļ”ŹĶ¹ż³ĢÖŠ£¬ĻĀĮŠ±ķ“ļŹ½µÄŹż¾Ż±ä“óµÄŹĒ( )
A”¢c£ØH+£© B”¢c£ØH+£©/c£ØCH3COOH£©
C”¢c£ØH+£©•c£ØOH-£© D”¢c£ØOH-£©/c£ØH+£©
E”¢c£ØH+£©•c( CH3COO-)/£ØCH3COOH£©
£Ø3£©Ģå»ż¾łĪŖ100mL pH=2µÄCH3COOHÓėŅ»ŌŖĖįHX£¬¼ÓĖ®Ļ”ŹĶ¹ż³ĢÖŠpHÓėČÜŅŗĢå»żµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņHXµÄµēĄėĘ½ŗā³£Źż CH3COOHµÄµēĄėĘ½ŗā³£Źż£ØĢī“óÓŚ”¢Š”ÓŚ»ņµČÓŚ£©£¬ĄķÓÉŹĒ .

£Ø4£©25”ꏱ£¬CH3COOHÓėCH3COONaµÄ»ģŗĻČÜŅŗ£¬Čō²āµĆpH=6£¬ŌņČÜŅŗÖŠ
c£ØCH3COO-£©”Ŗc£ØNa+£©= £ØĢī¾«Č·Öµ£©£¬c£ØCH3COO-£©/c£ØCH3COOH£©= ”£
(1)ADCB (2)BD
(3)“óÓŚ£¬Ļ”ŹĶĻąĶ¬±¶Źż£¬Ņ»ŌŖĖįHXµÄpH±ä»Æ±Č“×Ėį“󣬹ŹĖįŠŌĒ棬µēĮ¦Ę½ŗā³£Źż“ó”£
(4)9.9”Į10-7 18
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©øł¾ŻŌ½ČõŌ½Ė®½āŗĶĖįµÄµēĄėĘ½ŗā³£ŹżæÉÖŖHCO3-µÄµēĄė³£Źż×īŠ”£¬ŌņNa2CO3µÄ¼īŠŌ×īĒ棬Ę䏵“ĪNaClO£¬NaHCO3£¬×īŗóŹĒCH3COOH”£ŌņpHÓÉŠ”µ½“óµÄĖ³ŠņŹĒADCB”£
£Ø2£©Ļ”ŹĶ¹ż³ĢÖŠc(H+)¼õŠ”£¬K=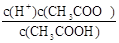 ŌŚĻ”ŹĶ¹ż³ĢÖŠ²»±ä£¬c(CH3COO-)¼õŠ”£¬ĖłŅŌ
ŌŚĻ”ŹĶ¹ż³ĢÖŠ²»±ä£¬c(CH3COO-)¼õŠ”£¬ĖłŅŌ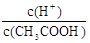 Ōö“ó£¬c(H+)•c(OH-)²»±ä£¬
Ōö“ó£¬c(H+)•c(OH-)²»±ä£¬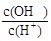 Ōö“ó£¬ĖłŅŌŌö“óµÄŹĒBD”£
Ōö“ó£¬ĖłŅŌŌö“óµÄŹĒBD”£
£Ø3£©øł¾ŻĶ¼ĻńæÉÖŖHXĻ”ŹĶŗópH±ä»Æ“ó£¬ĖłŅŌHXµÄĖįŠŌĒæÓŚCH3COOH£¬HXµÄµēĄėĘ½ŗā³£Źż“óÓŚCH3COOHµÄµēĄėĘ½ŗā³£Źż”£
£Ø4£©øł¾ŻµēŗÉŹŲŗćc(H+)+c(Na+)=c(OH-)+c(CH3COO-)£¬Ōņc(CH3COO-)-c(Na+)=c(H+)-c(OH-)£¬ČÜŅŗµÄpH=6£¬Ōņc(H+)=10-6mol/L£¬c(OH-)=10-8mol/L£¬ĖłŅŌc(CH3COO-)-c(Na+)=9.9”Į10-7”£K=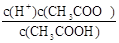 £¬Ōņ
£¬Ōņ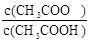 =
= =18ӣ
=18ӣ
æ¼µć£ŗµēĄėĘ½ŗā
µćĘĄ£ŗ±¾Ģā×ŪŗĻŠŌ½ĻĒ棬ÄŃ¶Č½Ļ“ó£¬Ö÷ŅŖŅŖŌĖÓĆŗĆĘ½ŗā³£Źż”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£Ø12 ·Ö£©£ØĆææÕ2·Ö£©CH3COOHŹĒ֊ѧ»Æѧ֊³£ÓƵÄŅ»ŌŖČõĖį£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Čō·Ö±š½«pH=2µÄŃĪĖįŗĶ“×ĖįĻ”ŹĶ100±¶£¬ŌņĻ”ŹĶŗóČÜŅŗµÄpH£ŗŃĪĖį “×Ėį£ØĢī”°£¾”±”¢”°£½”±»ņ”°£¼”±£©”£
£Ø2£©½«100mL0.1mol”¤L-1µÄCH3COOHČÜŅŗÓė50mL 0.2mol”¤L-1µÄNaOHČÜŅŗ»ģŗĻ£¬ĖłµĆČÜŅŗ³Ź ŠŌ£¬ŌŅņ £ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£©”£
£Ø3£©ŅŃÖŖij»ģŗĻČÜŅŗÖŠÖ»ŗ¬ÓŠCH3COO-”¢H+”¢Na+”¢OH-ĖÄÖÖĄė×Ó£¬ĒŅĄė×ÓÅØ¶Č“óŠ”¹ŲĻµĪŖ£ŗc(CH3COO-)>c(H+)> c(Na+)> c(OH-)£¬ŌņøĆČÜŅŗÖŠŗ¬ÓŠµÄČÜÖŹĪŖ ”£
£Ø4£©ŅŃÖŖKa(CH3COOH)= 1.76”Į10-5£¬Ka(HNO2)= 4.6”Į10-4£¬ČōÓĆĶ¬ÅØ¶ČµÄNaOHČÜŅŗ·Ö±šÖŠŗĶµČĢå»żĒŅpHĻąµČµÄCH3COOHŗĶHNO2£¬ŌņĻūŗÄNaOHČÜŅŗµÄĢå»ż¹ŲĻµĪŖ£ŗ
Ē°Õß ŗóÕߣØĢī”°>£¬<»ņ=”±£©
£Ø5£©ŅŃÖŖ25”ꏱ£¬0.1mol”¤L-1“×ĖįČÜŅŗµÄpHŌ¼ĪŖ3£¬ĻņĘäÖŠ¼ÓČėÉŁĮæ“×ĖįÄĘ¾§Ģ壬·¢ĻÖČÜŅŗµÄpHŌö“󔣶ŌÉĻŹöĻÖĻóÓŠĮ½ÖÖ²»Ķ¬µÄ½āŹĶ£ŗ¼×Ķ¬Ń§ČĻĪŖ“×ĖįÄĘ³Ź¼īŠŌ£¬ĖłŅŌČÜŅŗµÄpHŌö“ó£»ŅŅĶ¬Ń§øų³öĮķĶāŅ»ÖÖ²»Ķ¬ÓŚ¼×Ķ¬Ń§µÄ½āŹĶ£¬ĒėÄ抓³öŅŅĶ¬Ń§æÉÄܵĥķÓÉ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ÄźŗžÄĻÖźÖŽŹŠÄĻ·½ÖŠŃ§ø߶žÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌĄķæĘ»ÆѧŹŌ¾ķ£Ø“ų½āĪö£© ĢāŠĶ£ŗĢīæÕĢā
£Ø12 ·Ö£©£ØĆææÕ2·Ö£©CH3COOHŹĒ֊ѧ»Æѧ֊³£ÓƵÄŅ»ŌŖČõĖį£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Čō·Ö±š½«pH=2µÄŃĪĖįŗĶ“×ĖįĻ”ŹĶ100±¶£¬ŌņĻ”ŹĶŗóČÜŅŗµÄpH£ŗŃĪĖį “×Ėį£ØĢī”°£¾”±”¢”°£½”±»ņ”°£¼”±£©”£
£Ø2£©½«100mL 0.1mol”¤L-1µÄCH3COOHČÜŅŗÓė50mL 0.2mol”¤L-1µÄNaOHČÜŅŗ»ģŗĻ£¬ĖłµĆČÜŅŗ³Ź ŠŌ£¬ŌŅņ £ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£©”£
£Ø3£©ŅŃÖŖij»ģŗĻČÜŅŗÖŠÖ»ŗ¬ÓŠCH3COO-”¢H+”¢Na+”¢OH-ĖÄÖÖĄė×Ó£¬ĒŅĄė×ÓÅØ¶Č“óŠ”¹ŲĻµĪŖ£ŗc(CH3COO-)> c(H+)> c(Na+)> c(OH-)£¬ŌņøĆČÜŅŗÖŠŗ¬ÓŠµÄČÜÖŹĪŖ ”£
£Ø4£©ŅŃÖŖKa(CH3COOH)= 1.76”Į10-5£¬Ka(HNO2)= 4.6”Į10-4£¬ČōÓĆĶ¬ÅØ¶ČµÄNaOHČÜŅŗ·Ö±šÖŠŗĶµČĢå»żĒŅpHĻąµČµÄCH3COOHŗĶHNO2£¬ŌņĻūŗÄNaOHČÜŅŗµÄĢå»ż¹ŲĻµĪŖ£ŗ
Ē°Õß ŗóÕߣØĢī”°>£¬<»ņ=”±£©
£Ø5£©ŅŃÖŖ25”ꏱ£¬0.1mol”¤L-1“×ĖįČÜŅŗµÄpHŌ¼ĪŖ3£¬ĻņĘäÖŠ¼ÓČėÉŁĮæ“×ĖįÄĘ¾§Ģ壬·¢ĻÖČÜŅŗµÄpHŌö“󔣶ŌÉĻŹöĻÖĻóÓŠĮ½ÖÖ²»Ķ¬µÄ½āŹĶ£ŗ¼×Ķ¬Ń§ČĻĪŖ“×ĖįÄĘ³Ź¼īŠŌ£¬ĖłŅŌČÜŅŗµÄpHŌö“ó£»ŅŅĶ¬Ń§øų³öĮķĶāŅ»ÖÖ²»Ķ¬ÓŚ¼×Ķ¬Ń§µÄ½āŹĶ£¬ĒėÄ抓³öŅŅĶ¬Ń§æÉÄܵĥķÓÉ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012-2013ѧğ¼ŖĮÖŹ”³¤“ŗ¶žÖŠø߶žÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø“ų½āĪö£© ĢāŠĶ£ŗĢīæÕĢā
(12·Ö)ŅŃÖŖ25”ꏱ²æ·ÖČõµē½āÖŹµÄµēĄėĘ½ŗā³£ŹżŹż¾ŻČēĻĀ±ķ£ŗ
| »ÆѧŹ½ | CH3COOH | H2CO3 | HClO |
| Ę½ŗā³£Źż | Ka=1.8”Į10-5 | Ka1=4.3”Į10-7 Ka2=5.6”Į10-11 | Ka=3.0”Į10-8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ÄźŗŚĮś½Ė«Ń¼É½Ņ»ÖŠø߶žÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
(14·Ö)
£Ø1£©25 ”ꏱ£¬½«pH=11µÄNaOHČÜŅŗÓėpH=4µÄĮņĖįČÜŅŗ»ģŗĻ£¬ČōĖłµĆ»ģŗĻČÜŅŗpH=9£¬ŌņNaOHČÜŅŗÓėĮņĖįČÜŅŗµÄĢå»ż±ČĪŖ
ŅŃÖŖ25 ”ꏱ£¬0.1 L 0.1 mol”¤L-1µÄNaAČÜŅŗµÄpH=10,ČÜŅŗÖŠø÷Ąė×ÓµÄĪļÖŹµÄĮæÅضČÓɓ󵽊”µÄĖ³ŠņĪŖ ”£
£Ø2£©£©Čō100 ”ꏱ£¬KW=10-12£¬Ōņ100 ”ꏱpH=11µÄBa(OH)2ČÜŅŗÓėpH=2µÄĮņĖį°“Ģå»ż±Č1:9»ģŗĻ³ä·Ö·“Ó¦ŗópH= £»ČōøĆĪĀ¶ČĻĀ10Ģå»żµÄpH=aµÄijĒæĖįČÜŅŗÓė1Ģå»żpH=bµÄijĒæ¼īČÜŅŗ»ģŗĻŗóČÜŅŗ³ŹÖŠŠŌ£¬Ōņ»ģŗĻÖ®Ē°,aÓėbÖ®¼äÓ¦Āś×ćµÄ¹ŲĻµĪŖ  ”£
ӣ
£Ø3£©Ä³ĪĀ¶ČĻĀµÄĖ®ČÜŅŗÖŠ£¬c£ØH+£©=10x mol/L£¬c£ØOH-£©=10y mol/L”£xÓėyµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£
øĆĪĀ¶ČĻĀĖ®µÄĄė×Ó»żĪŖ ”£øĆĪĀ¶ČĻĀĀČ»ÆÄĘČÜŅŗµÄpHĪŖ
øĆĪĀ¶ČĻĀ0.01 mol/L NaOHČÜŅŗµÄpHĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com