
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
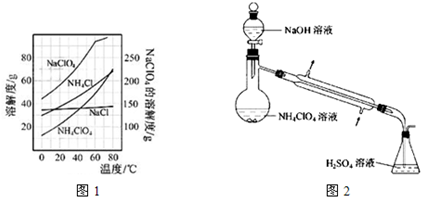
查看答案和解析>>
科目:高中化学 来源:101网校同步练习 高二化学 山东科学技术出版社 鲁教版 题型:022
混合溶液中NaCl和K2CrO4的浓度均为0.010 mol·L-1,向其中逐滴加入AgNO3溶液时,先与Ag+生成沉淀的离子是________.
[已知:Ksp(AgCl)=1.8×10-10 mol2·L-2
Ksp(Ag2CrO4)=2.0×10-12 mol3·L-3]
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(气体体积已换算成标准状况下的体积),根据图中信息回答下列问题。

(1)通过计算推测:
①原混合溶液中NaCl和CuSO4的物质的量浓度。
②t2时所得溶液的pH。
(2)实验中发现,阳极产生的气体的体积与阴极相比,明显小于对应时间段的理论值。试简要分析其可能的原因。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com