
ij�о���ѧϰС��̽��FeSO4�Ļ�ѧ���ʺ���;���ش��������⣺
��һ�� ̽��FeSO4��Һ������ԣ�
38.ȡ����FeSO4���壬����ʯ����Һ����FeSO4��Һ������ԣ�����ѡ�õ������н�ͷ�ιܡ�ҩ�� ��
������A����������������B���Թܡ���������C����ƽ��������D����Ͳ
������������ͼװ��̽��FeSO4���ȶ���
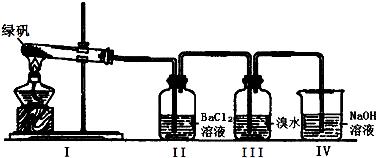
39. II���а�ɫ�������ɣ�С���Ա������۷�������Ϊ���зֽ���ﲻ���ܵ��� ��
A��Fe2O3��SO3��H2O �� ��B��Fe2O3��SO2��SO3��H2O ��
C��FeO��Fe2O3��SO2��SO3��H2O
40. III����ˮ�����������Ƿ���SO2�������ɣ�����SO2���ɣ���ˮ����ɫ��ʵ���У��۲쵽��ˮ��ɫ���ݴ��Ʋ�FeSO4�ֽ����п��ܱ�������Ԫ���� ��
41. NaOH������������SO2���壬��д�����������SO2����ķ�Ӧ��ѧ����ʽ�� ��
������̽��FeSO4��Fe2+��ԭ�ԣ�
42. ֤��FeSO4�н�ǿ�Ļ�ԭ�ԣ�����±���
| ʵ�鲽�� | ʵ��Ԥ�������� |
| ����һ��ȡ������FeSO4�������Թ��У�����һ����ˮ�ܽ⡣ | �� |
| ������� | �� |
���ģ�����������;̽��
43. ȱ����ƶѪ�����ڷ������������������������Ƴ�ҩƬʱ���������һ����������£��������� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й��̲��漰������ԭ��Ӧ����
A����������������ȴ����ɫ��dz B��þ���ڶ�����̼������ȼ��
C���˹��̵� D�����õ�Ũ�����Ի�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
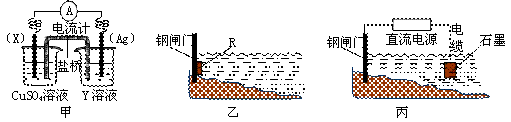
��1�����ݷ�Ӧ��2Ag��(aq)��Cu(s)��Cu2��(aq)��2Ag(s)��Ƶ�ԭ�������ͼ����ʾ��
�� �缫X�IJ����� ��
�� ���·�еĵ����Ǵ� �缫���� �缫����缫�������ƻ���ţ���
�� �ڵ�طŵ�����У�ʢ�б���KCl��֬�ܽ��������У���CuSO4��Һһ����ɢ�������� �������ӷ��ţ���
��2���� ������ʴһ��ɷ�Ϊ��ѧ��ʴ�͵绯ѧ��ʴ�������˵�����δ��ʱ��ϴ�������绯ѧ��ʴ�����⡣��д������������̵�������Ӧʽ�� ��
�� Ϊ�˼���ijˮ����բ�ű���ʴ�����ʣ����Բ�����ͼ����ʾ�ķ��������к�������բ���ϵĹ������R���Բ��� ����д��ĸ��ţ���
A��ͭ������ B���ơ����� C��п������ D��ʯī
�� ͼ����ʾ����Ҳ���Լ�����բ�ŵĸ�ʴ���ʣ�����բ��Ӧ����ֱ����� ����
��3��������һ�ֿ��Է�����硢�ŵ��װ�á���һ�������ڳ��ͷŵ�ʱ�����ķ�Ӧ�ǣ�NiO2 + Fe + 2H2O Fe(OH)2 + Ni(OH)2��
Fe(OH)2 + Ni(OH)2��
�� �������طŵ�ʱ���õ��ijһ�缫������ԭ��Ӧ�������� ������ţ���
A��NiO2 B��Fe C��Fe(OH)2 D��Ni(OH)2
�� �õ�طŵ�ʱ������������Һ��PH ��������С�����䣩
�� ���ʱ�õ�������ĵ缫��Ӧʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��Ӧ�٣�CO(g)��CuO(s)  CO2(g)��Cu(s)�ͷ�Ӧ�ڣ�H2(g)��CuO(s)
CO2(g)��Cu(s)�ͷ�Ӧ�ڣ�H2(g)��CuO(s)  Cu(s)��H2O(g)����ͬ��ij�¶��µ�ƽ�ⳣ���ֱ�ΪK1��K2�����¶��·�Ӧ�ۣ�
Cu(s)��H2O(g)����ͬ��ij�¶��µ�ƽ�ⳣ���ֱ�ΪK1��K2�����¶��·�Ӧ�ۣ�
CO(g)��H2O(g)  CO2(g)��H2(g)��ƽ�ⳣ��ΪK��������˵����ȷ����(�� ��)
CO2(g)��H2(g)��ƽ�ⳣ��ΪK��������˵����ȷ����(�� ��)
A����Ӧ�ٵ�ƽ�ⳣ��K1��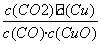
B����Ӧ�۵�ƽ�ⳣ��K��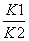
C�����ڷ�Ӧ�ۣ�����ʱ���¶����ߣ�H2Ũ�ȼ�С����÷�ӦΪ���ȷ�Ӧ
D�����ڷ�Ӧ�ۣ����º����£�����ѹǿ��H2Ũ��һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������ĵ���ƽ�ⳣ�����±���
| ���� | HCOOH | HCN | H2CO3 |
| ����ƽ�ⳣ�� ��25�棩 | Ki=1.77��10-4 | Ki=4.9��10-10 | Ki1=4.3��10-7 Ki2=5.6��10-11 |
����ѡ����ȷ����( )
A. 2CN��+H2O+CO2��2HCN+CO32-
B. �к͵��������pH��HCOOH��HCN����NaOH����ǰ��С�ں���
C. ���ʵ���Ũ����ȵ�HCOONa��KCN��Һ�У�c(Na��)��c(HCOO��) < c(K��)��c(CN��)
D. c(NH4+) ��ȵ�HCOONH4��Һ��NH4CN��Һ��NH4HCO3��Һ�У�
c(NH4HCO3)>c(NH4CN) >c(HCOONH4)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ����(����)
A���ܶȻ���Ļ������ܽ�ȿ϶���
B������AgCl�������Һ�м���������ˮʹAgCl�ܽ��ִﵽƽ��ʱ��AgCl���ܶȻ����䣬���ܽ��Ҳ����
C�������ܵ���ʷ��봿ˮ�У��ܽ�ﵽƽ��ʱ����������ӵ�Ũ�ȵij˻����Ǹ����ʵ��ܶȻ�
D��AgClˮ��Һ�ĵ����Ժ���������AgClΪ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һ���¶����У�a.���ᡡb�����ᡡc�����������ᡣ
(1)�������ʵ���Ũ����ͬʱ��[H��]�ɴ�С��˳����______________��
(2)ͬ�����ͬ���ʵ���Ũ�ȵ������ᣬ�к�NaOH������˳����____________��
(3)����[H��]��ͬʱ�����ʵ���Ũ���ɴ�С��˳��Ϊ______________��
(4)����[H��]��ͬ�������ͬʱ���ֱ��������п����ͬ״���²������������ɴ�С��˳��Ϊ_________________________________________________________________��
(5)��[H��]��ͬ�������ͬʱ��ͬʱ����п����������ͬ�����H2(��ͬ״��)����ʼʱ�ķ�Ӧ����________����Ӧ����ʱ��__________��
(6)��[H��]��ͬ���������ϡ��10����[H��]�ɴ�С��˳����______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�Ҷ����׳Ʋ��ᣬΪ��Ԫ�ᣨ�ṹ��ʽΪHOOC﹣COOH���ɼ�дΪH2C2O4����25��ʱ������ĵ���ƽ�ⳣ��K1=5.0��10﹣2��K2=5.4��10﹣5��̼��ĵ���ƽ�ⳣ��K1=4.5��10﹣7��K2=4.7��10﹣11������Ƶ�Ksp=4.0��10﹣8��̼��Ƶ�Ksp=2.5��10﹣9���ش��������⣺
��1��д��ˮ��Һ�в���ĵ��뷽��ʽ��������
��2��25�棬���ʵ���Ũ�ȶ�Ϊ0.1mol/L��Na2C2O4��Һ��pH��Na2CO3��ҺpH���������С������ȡ�����
��3�������½�0.2mol/L��KOH��Һ10mL��0.2mol/L�IJ�����Һ10mL��ϣ��������Һ�����ԣ������Һ����������Ũ���ɴ�С��˳��������
��4��25��ʱ��20mL̼��Ƶı�����Һ����μ���1.0��10﹣3 mol/L�IJ������Һ20mL���ܷ������������������ܡ�����
��5����ȥ��¯ˮ���е�CaSO4������̼������Һ�����������������ܽ⣬�䷴Ӧ�����ӷ���ʽ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ͼ����Լ�������ΪӦ�ܷⲢ�������������������________�������ʦ�����װ�ƾ�����ô����Ϊ���ĸ�ͼ�������________��ʢװŨ������Լ�ƿ���ĸ�ͼ�������________��

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com