
����Ŀ����ͼ��ʾ������Na2CO3��Һ�е���ϡ����ʱ����CO2�Ĺ��̡�

��1��д��a����ǰ������Ӧ�Ļ�ѧ����ʽ��___________________________________________________________________________________________��
��2��д��a��b�㷢����Ӧ�Ļ�ѧ����ʽ��____________________________________________________________________________________________��
��3����ijNa2CO3��Һ�к�mmol Na2CO3�������е���һ������ϡ���ᣬǡ��ʹ��Һ��Cl-��HCO3-�����ʵ���Ũ��֮��Ϊ2��1��������ϡ�����е�HCl�����ʵ�������____mol(�ú���ĸm�Ĵ���ʽ��ʾ)��
���𰸡�Na2CO3+HCl=NaHCO3+NaCl NaHCO3+HCl====NaCl+CO2��+H2O 4m/3
��������
��1��a��ǰ��CO2������˵������ֻ��Na2CO3ת����NaHCO3������ʽΪNa2CO3+HCl=NaHCO3+NaCl��
��2��b�㿪ʼ���ټ�������Ҳ�������CO2���壬˵��NaHCO3��ȫ��ת����NaCl��CO2��H2O������ʽΪNaHCO3+HCl=NaCl+CO2��+H2O��
��3��������˵������NaHCO3ת��ΪNaCl��CO2��H2O������ڶ�����Ӧ���ĵ�HCl�����ʵ���Ϊn����
Na2CO3+HCl====NaCl+NaHCO3
m m m m
NaHCO3+HCl====NaCl+CO2��+H2O
n n n
��ʱ����Һ�е�HCO3-�����ʵ���Ϊ(m-n)mol��Cl-�����ʵ���Ϊ(m+n)mol��������ã�(m+n)��(m-n)=2��1�����
n=m/3 mol����n(HCl)=n(Cl-)= (m+n)mol=(m+m/3)mol=4m/3 mol��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ��ͬѹ�£��������һ��������(N2O)�Ͷ�����̼����������Ƚϣ���������ȡ�������̼ԭ�����뵪ԭ������ȡ���������������ȡ�������������ȷ����(����)
A. �٢ڢ� B. �ڢ� C. �٢� D. �٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������500mL 0.100 mol��L��1��NaCl��Һ������ʵ�����ʾ��ͼ���£�
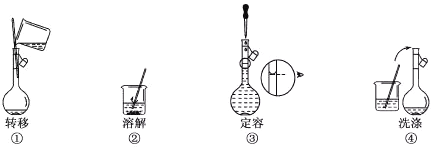
����˵����ȷ����
A. ʵ�������õ������У���ƽ��250mL����ƿ���ձ�������������ͷ�ιܵ�
B. ����ʵ������������ȷ˳��Ϊ�٢ڢܢ�
C. ����ƿ��Ҫ������ˮ������ˮϴ�ӣ������ſ���
D. ����ʱ����������ƿ�Ŀ̶��ߣ�ʹ��õ�NaCl��ҺŨ��ƫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£��ڹ̶��ݻ����ܱ������У����淴Ӧ A(g)+3B(g) ![]() 2C(g)�ﵽƽ��ʱ�������ʵ����ʵ���֮���� n(A)��n(B) ��n(C)=1��3��2�������¶Ȳ��䣬�� 1��3��2 �����ʵ���֮���ٳ��� A��B��C����
2C(g)�ﵽƽ��ʱ�������ʵ����ʵ���֮���� n(A)��n(B) ��n(C)=1��3��2�������¶Ȳ��䣬�� 1��3��2 �����ʵ���֮���ٳ��� A��B��C����
A. ƽ�����������ƶ� B. ƽ�ⲻ�ƶ�
C. C �����������С D. ��ѧ��Ӧ���ʼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��W��X��Y��Z���ֶ�����Ԫ����Ԫ�����ڱ��е����λ����ͼ��ʾ��W����̬�⻯���������ۺ����ᷴӦ�������ӻ�����ɴ˿�֪

A. X��Y��Z������⻯���ȶ�����������Y
B. ZԪ���������Ӧˮ���������һ��ǿ��Y
C. XԪ���γɵĵ��������ӻ�ԭ�Դ���Y
D. ZԪ�ص����ڻ�ѧ��Ӧ��ֻ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����amol���ۼ��뵽��bmol������Һ�У���ַ�Ӧ��������ȫ�ܽ⣬���ռ���c L���������NO��NO2������塣�����й�˵������ȷ����
A. ����Ӧ�������ֻ��Fe2+���ɣ���![]() < a<
< a<![]()
B. ����Ӧ�������ֻ��Fe3+���ɣ���b=3a +![]()
C. ����Ӧ���������Fe2+��Fe3+���ɣ���![]() <b<6a
<b<6a
D. ����Ӧ����Һ����dmol H+����b=3a+d+![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.Ħ���ǹ��ʵ�λ���е�7������������֮һ
B.�����Ħ��������98 g
C.0.5molH2 Լ����3.01��1023 ����ԭ��
D.NA���������ӵ�������32g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�У�һ�������ڻ�ѧ���������ת������( )��
A. ���ȷ�ӦB. ������ȼC. �ɱ�����D. ȼ�ű���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I��25��ʱ�������ΪVa��pH��a��ijһԪǿ����Һ�����ΪVb��pH��b��ijһԪǿ����Һ��ϣ�ǡ���к͡���ش�
����a��b��12����Va��Vb��________��
����Va��Vb��a��0.5b����a��ȡֵ��Χ��_________________��
II�����ӹ�ҵ�У�����FeCl3��Һ��Ϊӡˢ��·ͭ��ʴ��Һ��ij̽��С�����������·������Һ����Դ���գ�
��ش�

(1)��������FeCl3��Һʴ��ͭ���ķ�Һ�к��еĽ�����������_____________��
(2)������м���H2O2��Һ��Ŀ����________________________________________��
(3)��֪�������������������pH
Cu(OH) 2 | Fe(OH) 2 | Fe(OH) 3 | |
��ʼ����ʱ | 4.7 | 7.0 | 1.9 |
������ȫʱ | 6.7 | 9.0 | 3.2 |
���ݱ��������Ʋ����pH�ķ�Χ��_____________��
(4)��Ҫ��ȥ����MgCl2��Һ�е�FeCl3������Լ�����Լ���_____________��(����ĸ)
A��NaOH B��Mg(OH)2 C��MgCO3 D�� NH3H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com