
我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业作出了突出贡献。以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3+CO2+H2O=NH4HCO3; NH4HCO3+NaCl=NaHCO3↓+NH4Cl;  2NaHCO3 =Na2CO3+CO2↑+H2O。
2NaHCO3 =Na2CO3+CO2↑+H2O。
Ⅰ.原理分析
碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是 。
a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,在溶液中首先结晶析出
Ⅱ.实验探究
(1)一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
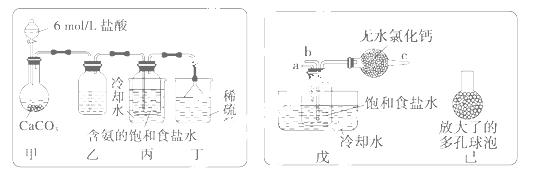
回答下列有关问题:
a.乙装置中的试剂是 ;
b.丁装置中稀硫酸的作用是 ;
c.实验结束后,分离出NaHCO3晶体的操作是 (填分离操作的名称)。
(2)另一位同学用图中戊装置(其他装置未画出)进行实验。
a.实验时,须先从 管通入 气体,再从 管中通入 气体。
b.有同学建议在戊装置的b导管下端连接己装置,理由是 。
(3)请再写出一种实验室制取少量碳酸氢钠的方法: 。
科目:高中化学 来源: 题型:
在一定条件下,Na2CO3溶液存在水解平衡:CO +H2O
+H2O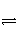
 HCO
HCO +OH-。下列说法正确的是( )
+OH-。下列说法正确的是( )
A.稀释溶液,水解平衡常数增大
B.通入CO2,平衡朝正反应方向移动
C.升高温度,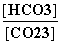 减小
减小
D.加入NaOH固体,溶液pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组的学生从网上查得如下信息:①钠能在CO2中燃烧。②常温下CO能与PdCl2溶液反应得到黑色的Pd。经过分析讨论,他们认为钠在CO2中燃烧时,还原产物可能是碳,也可能是CO,氧化产物可能是Na2CO3。为验证上述推断,他们设计如下方案进行实验,请回答下列问题。
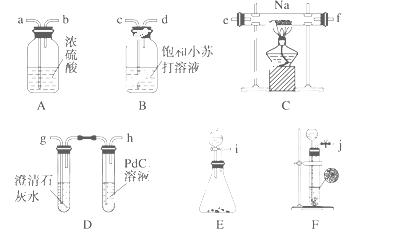
(1)他们欲用上述装置组装一套新装置:用石灰石与盐酸反应制取CO2(能随意控制反应的进行)来证明钠能在CO2中燃烧并检验其还原产物,所用装置接口连接顺序为__________________,制取CO2反应的离子方程式为______________________。
(2)装置连接好后,首先要进行的实验操作是__________,点燃酒精灯前,应进行的操作是__________,等装置__________(填写装置字母代号及现象)时,再点燃酒精灯,这步操作的目的是______________
(3)若装置D的PdCl2溶液中有黑色沉淀,C中有残留固体(只有一种物质),则C中 反应的化学方程式为________________________________________________;若装置D的PdCl2溶液中无黑色沉淀,C中有残留固体(有两种物质),则C中反应的化学方程式为_________________________。
(4)后来有一位同学提出,钠的氧化产物也可能是Na2O,因此要最终确定钠的氧化产物是何种物质,还 需要检验C中残留的固体是否含有Na2O,为此,他认为应较长时间通入CO2以确保钠反应完,然后按照如下方案进行实验,可确定残留固体中是否含有Na2O,他的实验方案是________________。
需要检验C中残留的固体是否含有Na2O,为此,他认为应较长时间通入CO2以确保钠反应完,然后按照如下方案进行实验,可确定残留固体中是否含有Na2O,他的实验方案是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
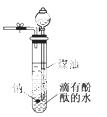 某同学设计出一种隔绝空气让钠与水
某同学设计出一种隔绝空气让钠与水 反应的方法,使同学们能仔细观察到各种实验现象.该方法简便、安全、现象明显、有趣味性,实验装置如图所示.实验时,往100 mL的大试管中先加入40 mL煤油,取绿豆粒大小的金属钠放入大试管后,塞上橡皮塞(这时止水夹处于关闭状态),通过漏斗加入约40 mL滴有酚酞的水。
反应的方法,使同学们能仔细观察到各种实验现象.该方法简便、安全、现象明显、有趣味性,实验装置如图所示.实验时,往100 mL的大试管中先加入40 mL煤油,取绿豆粒大小的金属钠放入大试管后,塞上橡皮塞(这时止水夹处于关闭状态),通过漏斗加入约40 mL滴有酚酞的水。
根据反应中观察到的现象,回答下列问题。
(1)实验前怎样检验该装置的气密性?_________________________________
______________________ __________
__________ __________________________________.
__________________________________.
(2)金属钠投入煤油后的现象是____________。
(3)加入水后的现象及原因是_________________________________________________。
(4)大试管中溶液颜色的变化是__________________________________________。
(5)简述检验产生气体是否是氢气的方法:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
往甲、乙、丙、丁四个烧杯内分别放入0.1 mol的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100 mL水,搅拌,使固体完全溶解,则甲、乙、丙、丁溶液中溶质的质量分数大小顺序是( )
A.甲<乙<丙<丁 B.丁<甲<乙=丙
C.甲=丁<乙=丙 D.丁<甲<乙<丙
查看答案和解析>>
科目:高中化学 来源: 题型:
欲除去下列物质中的少量杂质,请填写所用方法及反应的化学方程式。
| 欲除去的少量 | 方法 | 反应的化学方程式 |
| (1)Na2CO3固体中的NaHCO3 | ||
| (2)NaCl溶液中的Na2CO3 | ||
| (3)NaOH溶液中的Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于钠的描述正确的是( )
①钠在自然界既有游离态又有化合态存在
②金属钠着火不可以用泡沫灭火器救火
③钠的密度比煤油大
④钠比铜活泼,因而钠可以从CuCl2溶液中置换出铜
⑤钠在空气中燃烧,主要产物是Na2O2
A.①③④⑤ B.③④⑤ C.①③⑤ D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
糕点包装中常见的脱氧剂组成为还原性铁粉、氯
化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
A.脱氧过程是吸热反应,脱氧的同时可降低温度,延长糕点保质期
B.脱氧过程中铁做原电池正极,电极反应为:Fe—2e— = Fe2+
C.脱氧过程中碳做原电池负极,电极反应为:2H2O + O2 + 4e— = 4OH—
D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com