
| A. | 脱氧过程是吸热反应,可降低温度,延长食品保质期 | |
| B. | 脱氧过程中炭作原电池正极,电极反应为4H++O2+4e-═2H2O | |
| C. | 含有0.56g铁粉的脱氧剂,理论上最多能吸收氧气168mL (标准状况) | |
| D. | 该过程实现了电能到化学能的转化 |
分析 Fe、C和NaCl溶液构成原电池,发生吸氧腐蚀,Fe易失电子作负极,C作正极,负极反应式为Fe-2e-=Fe2+、正极反应式为2H2O+O2+4e-=4OH-,生成的亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁被氧化生成氢氧化铁,据此解答.
解答 解:A.该装置构成原电池,原电池反应为放热反应,所以去脱氧过程为放热反应,故A错误;
B.炭作正极,氧气在正极上得电子发生还原反应,电极反应为:2H2O+O2+4e-=4OH-,故B错误;
C.负极反应式为Fe-2e-=Fe2+、正极反应式为2H2O+O2+4e-=4OH-,生成的亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁被氧化生成氢氧化铁,所以Fe单质最终转化为+3价铁元素,0.56gFe的物质的量=$\frac{0.56g}{56g/mol}$=0.01mol,完全转化为+3价铁元素时,转移电子的物质的量为0.03mol,根据转移电子守恒消耗氧气体积$\frac{0.03mol}{4}$×22.4L/mol=168mL,故C正确;
D.原电池将化学能转化为电能,故D错误;
故选C.
点评 本题考查金属腐蚀与防护,明确铁腐蚀过程中发生的反应是解本题关键,易错选项是C,注意铁单质最终被氧化生成物质的成分是解本题关键,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径:A<B<D | |
| B. | A与B形成的化合物溶于水后溶液呈碱性 | |
| C. | 氧化物的水化物的酸性一定是D>C | |
| D. | 气态氢化物沸点A大于C是因为H-A键比H-C键稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | X难溶于乙醇 | |
| B. | 酒中的少量丁酸能抑制X的水解 | |
| C. | X完全燃烧后生成CO2和H2O的物质的量比为1:1 | |
| D. | 分子式为 C5H10O2且能与NaHCO3溶液反应生成气体的物质有5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 的合成路线:
的合成路线: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 测定常温时的饱和HCOONa溶液、CH3COONa溶液的pH | HCOONa的pH<CH3COONa的pH | 弱酸的酸性:HCOOH>CH3COOH |
| B | 向5ml 2mol•L-1NaOH溶液中加入1ml 1mol•L-1CuSO4溶液,振荡后加入0.5ml有机物X,加热 | 未出现砖红色沉淀 | 说明X中不含有醛基 |
| C | KBrO3溶液中加入少量苯,然后通入少量Cl2 | 有机相呈橙红色 | 氧化性:Cl2>Br2 |
| D | NaAlO2溶液与NaHCO3溶液混合 | 有白色絮状沉淀生成 | 二者水解相互促进生成氧化铝沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.5 mol•L-l•min-l | B. | v(B)=0.6 mol•L-l•min-l | ||
| C. | v(C)=0.35 mol•L-l•min-l | D. | v(D)=0.4 mol•L-l•min-l |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
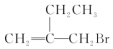
| A. | 该物质可以发生水解反应 | |
| B. | 该物质能和AgNO3溶液反应产生AgBr沉淀 | |
| C. | 该物质可以发生消去反应 | |
| D. | 该物质不能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 步骤①、③的操作分别是过滤、萃取 | |
| B. | 步骤②的反应是非氧化还原反应 | |
| C. | 步骤③中加入的有机溶剂是裂化汽油或四氯化碳 | |
| D. | 步骤④的操作是过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com