
下列图像均为实验过程中产生沉淀的物质的量(Y)与加入试剂的量(X)之间的关系图,则其中正确的是( )
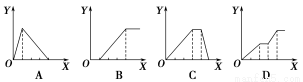
A.向AlCl3溶液中逐滴加入NaOH溶液至过量且边滴边振荡
B.向NaAlO2溶液中逐滴滴加稀盐酸至过量且边滴边振荡
C.向NH4Al(SO4)2溶液中逐滴加入氢氧化钠溶液直至过量
D.向NaOH、Ba(OH)2、NaAlO2的混合溶液中逐渐通入二氧化碳至过量
 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源:2017届河北省高三上学期摸底考试化学试卷(解析版) 题型:选择题
在FeCl3、CuCl2混合溶液中,加入一定量的铁屑,反应完全后将固体滤出,下列说法中正确的是( )
A.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+
B.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,可能含Cu2+和Fe3+
C.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe3+和Fe2+,一定不含Cu2+
D.若滤出的固体中含有铁和铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+和Fe3+
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期第一次月考化学试卷(解析版) 题型:填空题
磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)已知磷酸(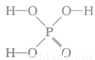 )分子中的三个氢原子都可以与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2) 却不能与D2O发生氢交换。则H3PO2是(填“一元”“二元”或“三元”)酸,其分子的结构式为________(填字母)。
)分子中的三个氢原子都可以与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2) 却不能与D2O发生氢交换。则H3PO2是(填“一元”“二元”或“三元”)酸,其分子的结构式为________(填字母)。
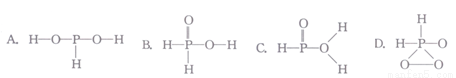
(2)H3PO2具有较强的还原性,可以通过电解的方法制备。“四室电渗析法”工作原理如图所示(阳离子交换膜和阴离子交换膜分别只允许阳离子、阴离子通过)。

①阳极的电极反应式为_________。
②II 膜为___________(填“阴离子交换膜”或“阳离子交换膜”)。
③早期采用“三室电渗析法”制备H3PO2,将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的交换膜,从而合并阳极室与产品室,其缺点是产品中混有______杂质。
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高新部高三上学期一轮复习第一次测试化学试卷(解析版) 题型:填空题
请回答:
(1)H2O2的电子式________________,Na2O2的电子式________________
(2)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式_________________。
(3)完成以下氧化还原反应的离子方程式:
( )MnO4-+( )C2O42-+________===( )Mn2++( )CO2↑+________
(4)向30 mL 1 mol·L-1的AlCl3溶液中逐渐加入浓度为4 mol·L-1的NaOH溶液,若产生0.78 g白色沉淀,则加入的NaOH溶液的体积可能为____________
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高新部高三上学期一轮复习第一次测试化学试卷(解析版) 题型:选择题
某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是( )
A.FeCl2 B.Na2O C.SiO2 D. AlCl3
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高新部高三上学期一轮复习第一次测试化学试卷(解析版) 题型:选择题
下列事实及其解释不正确的是( )
A.钠保存在煤油中,是因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水蒸气
B.用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应
C.滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3
D.钠长期暴露在空气中的产物是Na2CO3,原因是钠与氧气生成的Na2O与水和二氧化碳反应
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省葫芦岛市六校协作体高三上期初考试化学试卷(解析版) 题型:填空题
甲醇是结构最为简单的饱和一元醇,又称“木醇”或“木精”。甲醇是一碳化学基础的原料和优质的燃料,主要应用于精细化工、塑料、能源等领域。已知甲醇制备的有关化学反应如下:
反应①:CO(g)+2H2(g)  CH3OH(g) △H1=-90.77kJ/mol
CH3OH(g) △H1=-90.77kJ/mol
反应②:CO2(g)+H2(g)  CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应③:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H3=-49.58kJ/mol
CH3OH(g)+H2O(g) △H3=-49.58kJ/mol
(1)反应②的△H2=__________________
(2)若500℃时三个反应的平衡常数依次为K1、K2与K3,已知500℃时K1、K2的值分别为2.5、1.0,并测得该温度下反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,则此时V正________V逆(填“>”、“=”或“<”)
(3)在3L容积可变的密闭容器中发生反应②,c(CO)随反应时间t变化如图中曲线I所示。若在t0时刻分别改变一个条件,曲线I变为曲线II和曲线III。当曲线I变为曲线II时,改变的条件是 。当通过改变压强使曲线I变为曲线III时,曲线III达到平衡时容器的体积为_____________。

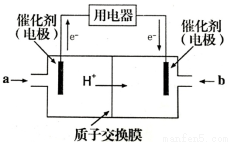
(4)甲醇燃料电池可能成为未来便携电子产品应用的主流。某种甲醇燃料电池工作原理如图所示,则通入a气体的电极电极反应式为 。
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。常温条件下,将a mol/L的CH3COOH与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为________________。
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省葫芦岛市六校协作体高三上期初考试化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.使甲基橙变红的溶液中:Na+、Cl-、CH3 COO-、Fez+
B.水电离的OH-浓度为10-12mol/L的溶液中:Mg2+、NH4+、AlO2-、SO32-
C.无色溶液中:Al3+、NO3-、Cl-、SO42-
D.c(K2C2O4)=0.5mol/L溶液中:Na+、K+、MnO4-、Cl-
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上学期期初热身测试化学试卷(解析版) 题型:选择题
X、Y、Z、W是原子序数依次增大的短周期元素。X、W同主族,Z、W同周期,X原子核内质子数是Y原子核内质子数的3/4,W原子最外层电子数是Z原子最外层电子数的4倍。下列说法中正确的是( )
A. 原子半径:r(X)>r(Y)>r(W)>r(Z)
B. 元素W的气态氢化物的热稳定性比元素X的强
C. X、Y、Z三种元素形成的化合物中存在离子键和共价键
D. Y和W形成的化合物的熔点肯定比Y和Z形成的化合物的熔点低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com