
【题目】已知某铁盐含三种元素,为了探究其组成并将之转化为硫酸铁,设计了如下实验:

请回答:
(1)铁盐X的化学式为________________,气体乙的化学式为________________。
(2)写出溶液A中加入H2O2后发生反应的离子方程式______________________。
(3)由溶液B制备纯净硫酸铁的一系列操作为:蒸发浓缩、______、过滤、洗涤、干燥。
(4)为确保溶液A到B反应完全,需要检验B溶液中有无Fe2+残留,请设计简单的实验:__________________________。
【答案】FeC2O4 CO 2Fe2++H2O2+2H+=2Fe3++2H2O 冷却结晶或冷却热饱和溶液 取少量B溶液,滴入KMnO4溶液,若紫色变浅褪去,说明仍有Fe2+,反之则无
【解析】
由转化关系可知X在隔绝空气下加热生成FeO,且生成气体甲可使澄清石灰水变浑浊,应为CO2,则X含有Fe、C、O三种元素,则生成的乙为CO,且n(CO)=c(CO2)=n(CaCO3)=![]() =0.05mol,满足m(FeO)+m(CO)+m(CO2)= 0.05mol×72g/mol+0.05mol×28g/mol +0.05mol×44g/mol =7.20g,因此n(Fe):n(C):n(O)=0.05∶0.1∶(0.05+2×0.05+0.05)=1∶2∶4,则X的化学式为FeC2O4,以此解答该题。
=0.05mol,满足m(FeO)+m(CO)+m(CO2)= 0.05mol×72g/mol+0.05mol×28g/mol +0.05mol×44g/mol =7.20g,因此n(Fe):n(C):n(O)=0.05∶0.1∶(0.05+2×0.05+0.05)=1∶2∶4,则X的化学式为FeC2O4,以此解答该题。
(1)由以上分析可知X为FeC2O4,气体乙为CO,故答案为:FeC2O4;CO;
(2)溶液A含有硫酸亚铁,具有还原性,加入H2O2后发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(3)B为硫酸铁,由溶液B制备纯净硫酸铁的一系列操作为:蒸发浓缩、冷却结晶、过滤、洗涤、干燥,故答案为:冷却结晶;
(4)为确保溶液A到B反应完全,需要检验B溶液中有无Fe2+残留,可利用亚铁离子的还原性,可取少量B溶液,滴入KMnO4溶液,若紫色变浅甚至褪去,说明仍有Fe2+,反之则没有亚铁离子,故答案为:取少量B溶液,滴入KMnO4溶液,若紫色变浅褪去,说明仍有Fe2+,反之则无。


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】某元素的原子最外层只有一个电子,其原子与卤素原子结合时,所形成的化学键( )
A.一定是离子键
B.一定是共价键
C.可能是离子键也可能是共价键
D.以上说法都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】180℃时将0.5 mol H2和1 mol CO2通入1 L的恒容密闭容器中,反应生成甲醇蒸汽(CH3OH)和某无机副产物,测得各物质的物质的量随时间的部分变化如图所示,下列说法中正确的是

A. 该反应的化学方程式:2CO2+4H2![]() 2CH3OH+O2
2CH3OH+O2
B. 在0~3 min内H2的平均化学反应速率为0.1 mol·L-1·min-1
C. 当容器内混合气体密度不再变化时,表明反应已经达到平衡状态
D. 在3~10 min内,反应仍未达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素R的最高价氧化物的水化物分子式是HnRO2n﹣2 , 则在气态氢化物中R元素的化合价是( )
A.3n﹣10
B.12﹣3n
C.3n﹣4
D.3n﹣12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修5有机化合物】甲苯是有机化工生产的基本原料之一。利用乙醇和甲苯为原料,可按下列路线合成分子式均为C9H10O2的有机化工产品E和J。

已知:
请回答:
(1)写出下列反应方程式
①B+D→E______________________________________。
②G→H________________________________________。
(2)①的反应类型为__________;②的反应类型为__________;F的结构简式为__________。
(3)E、J有多种同分异构体,写出符合下列条件的4种同分异构体的结构简式。要求:①与E、J属同类物质②苯环上有两个取代基且苯环上的一氯代物只有两种。
__________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO2是大气的主要污染物之一,某研究小组设计如图所示的装置对NO2 进行回收利用装置中a、b均为多孔石墨电极。下列说法正确的是

A. b为电池的负极,发生还原反应
B. 电子流向:a电极→溶液→b电极
C. 一段时间后,b极附近HNO3浓度增大
D. a极的电极反应为NO2+e-+H2O=NO3-+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 铅蓄电池放电时的负极和正极的质量均增加
B. MgO(s)+C(s)![]() Mg(s)+CO(g)在室温下不能自发进行,说明该反应的△H <0
Mg(s)+CO(g)在室温下不能自发进行,说明该反应的△H <0
C. 对于发应2H2O2![]() 2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率
2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率
D. H2O与金属Na反应生成1molH2,反应中转移的电子数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应方程式,书写正确的是
A. 碳酸钠溶液中加入盐酸 CO32-+2H+=H2O+CO2↑
B. 稀硫酸中加入铁粉 2Fe+6H+=2Fe3++3H2↑
C. 碳酸钙中加入盐酸 CO32-+2H+=H2O+CO2↑
D. 氢氧化钡溶液中加入硫酸 H++OH-=H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近浙江大学成功研制出具有较高能量密度的新型铝一石墨烯(Cn)电池(如图)。该电池分别以铝、石墨烯为电极,放电时电池中导电离子的种类不变。已知能量密度=电池容量(J)÷负极质量(g)。下列分析正确的是
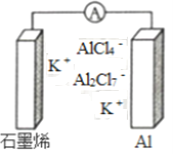
A. 放电时,Cn(石墨烯)为负极
B. 放电时,Al2Cl7-在负极转化为AlCl4-
C. 充电时,阳极反应为4 Al2Cl7-+3e-=A1+7AlCl4-
D. 以轻金属为负极有利于提高电池的能量密度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com