
【题目】向100mL的FeBr2溶液中通入标准状况下的C12 3.36 L后,C12全部被还原,并且测得溶液中c(Br–)=c(Cl–),则原FeBr2溶液的物质的量浓度是
A.3mol/LB.2mol/ LC.1.5 mol/ LD.0.75mol/L
【答案】B
【解析】
标准状况下的3.36 L C12的物质的量为0.15mol,C12全部被还原,可知转移电子的物质的量为0.3mol,溶液中的Cl–的物质的量为0.3mol。由于还原性:Fe2+>Br–,所以通入氯气后,Fe2+先被氯气氧化。若只有Fe2+被氧化,由于溶液中c(Br–)=c(Cl–),所以n(Br–)=2n(Cl2)=0.3mol,n(FeBr2)=![]() n(Br–)=0.15mol,n(Fe2+)=0.15mol,0.15moLFe2+被氧化为Fe3+,只转移0.15mol电子,所以应该还有部分Br–被氧化,则氧化后的溶液中有Fe3+、Br–和Cl–,Br–和Cl–的物质的量均为0.3mol,根据电荷守恒,Fe3+的物质的量为
n(Br–)=0.15mol,n(Fe2+)=0.15mol,0.15moLFe2+被氧化为Fe3+,只转移0.15mol电子,所以应该还有部分Br–被氧化,则氧化后的溶液中有Fe3+、Br–和Cl–,Br–和Cl–的物质的量均为0.3mol,根据电荷守恒,Fe3+的物质的量为![]() =0.2mol,所以原FeBr2溶液中FeBr2的物质的量即为0.2mol,物质的量浓度为
=0.2mol,所以原FeBr2溶液中FeBr2的物质的量即为0.2mol,物质的量浓度为![]() =2mol/L,故选B。
=2mol/L,故选B。


科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,Na、NaOH、NaHCO3分别与等物质的量的该物质恰好反应时,Na、NaOH、NaHCO3的物质的量之比为( )
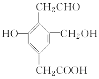
A. 3∶3∶2B. 3∶2∶1
C. 1∶1∶1D. 3∶2∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组拟合成除草剂苯达松和染料中间体X。

已知信息:

(1)下列说法正确的是___。
A.化合物B到C的转变涉及到取代反应 B.化合物C具有两性
C.试剂D可以是甲醇 D.苯达松的分子式是C10H10N2O3S
(2)化合物F的结构简式是________。
(3) 写出E+G→H的化学方程式______。
(4)写出分子式为C6H13NO2,同时符合下列条件的同分异构体的结构简式,写出2个即可_____。
①分子中有一个六元环,且成环原子中最多含2个非碳原子;
②1H﹣NMR谱和IR谱检测表明分子中有4种化学环境不同的氢原子。有N﹣O键,没有过氧键(﹣O﹣O﹣)。
(5)设计以CH3CH2OH和 为原料制备X(
为原料制备X( )的合成路线(无机试剂任选,合成中须用到上述①②两条已知信息,用流程图表示)。_____
)的合成路线(无机试剂任选,合成中须用到上述①②两条已知信息,用流程图表示)。_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴(Co)的氧化物是一种重要的化工原料,工业上利用反应CoCO3+O2![]() CoxOy+CO2来生产相应的钴的氧化物。实验室中可以用下列装置来制取钴的氧化物并测定其分子组成。
CoxOy+CO2来生产相应的钴的氧化物。实验室中可以用下列装置来制取钴的氧化物并测定其分子组成。
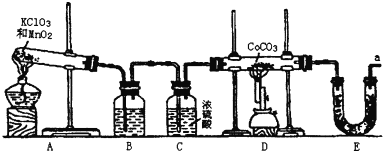
请填写下列空白:
(1)写出A装置的大试管里发生反应的化学方程式___;
(2)E装置的U形管里盛放的物质是___;
A.P2O5 B.无水CaCl2 C.碱石灰 D.无水CuSO4
(3)O3的氧化性比O2强。已知制得的O2中含有少量的Cl2和O3,则B装置中所盛放的物质是___;
A.NaOH溶液 B.饱和NaHCO3溶液 C.饱和NaCl溶液 D.KI溶液
(4)实验结束时,若先撤去A装置中的酒精灯,会引起___;
(5)在CoCO3完全转化为CoxOy后,若称得E管增重4.40g,D管内残留物质的质量是8.30g,则生成CoxOy的化学式为___;请写出详细的计算过程。
(6)此实验装置存在一个比较大的缺陷,如何完善___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是( )
图 1 图 2
图 2  图 3
图 3  图 4
图 4
A.由图1可知反应②的第I步比第Ⅱ步反应速率快
B.若图2为1 mL pH=2某一元酸溶液加水稀释时pH随溶液总体积的变化曲线,则说明该酸是强酸
C.由图3知反应3A(g)+2B(g) 2C(g) 的 ΔH>0,且a=1.5
D.若图4表示常温下用0.1000mo1/L NaOH溶液滴定25.00mL CH3COOH溶液的滴定曲线,则c(CH3COOH)=0.1000mo1/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:p(Ba2+) ═ -lgc(Ba2+),p(X2-) ═ -lgc(X2-) ,Ksp(BaSO4)<Ksp(BaCO3),常温下BaSO4、BaCO3的溶解平衡曲线如图所示,下列叙述中正确的是( )

A.M线为BaCO3的溶解平衡曲线B.b点对应的溶液中Ba2+、SO42-不能形成BaSO4沉淀
C.Ksp(BaSO4) > 10-(1+a)D.BaSO4(s)+CO32-(aq) ![]() BaCO3(s)+SO42-(aq)的K=0.1
BaCO3(s)+SO42-(aq)的K=0.1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在催化条件下发生反应:N2O(g)+CO(g) ![]() CO2(g)+N2(g)可使环境污染性气体转化为无害气体。反应进程中的能量变化如图所示。下列说法正确的是
CO2(g)+N2(g)可使环境污染性气体转化为无害气体。反应进程中的能量变化如图所示。下列说法正确的是

A. 加入催化剂使反应的△H变小
B. 该反应的热化学方程式为:N2O(g)+CO(g) ![]() CO2(g)+N2(g) △H﹦ - 226 kJ/mol
CO2(g)+N2(g) △H﹦ - 226 kJ/mol
C. 反应物的总能量小于生成物的总能量
D. 该反应正反应的活化能大于逆反应的活化能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:

下列说法正确的是 ( )
A. 自然界中存在大量的单质硅
B. 步骤电弧炉中的化学方程式为SiO2+C![]() Si+CO2↑
Si+CO2↑
C. 二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应
D. SiHCl3(沸点33.0 ℃)中含有少量的SiCl4(沸点67.6 ℃),通过蒸馏(或分馏)可提纯SiHCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一酸性溶液可能含有Br-、SO42-、H2SO3、NH4+ 等微粒,对该酸性溶液分别进行实验:
(1)加热,放出的气体可以使品红溶液褪色;
(2)取原溶液加碱,调至溶液呈碱性,加热,放出的气体能使湿润的红色石蕊试纸变蓝;
(3)取原溶液加氯水,溶液略显黄色,再加入BaCl2溶液,产生的白色沉淀不溶于稀硝酸。
对于下列微粒不能确认其在原溶液中是否存在的是![]()
![]()
![]()
A.SO42-B.Br-C.H2SO3D.NH4+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com