
【题目】光气(COCl2)常作有机合成、农药、药物、燃料及其他化工制品的中间体。
(1)COCl2结构与甲醛相似,写出COCl2电子式_____;解释COCl2的沸点比甲醛高的原因是_____。
(2)密闭容器中吸热反应COCl2(g)![]() Cl2(g)+CO(g)达到平衡后,改变一个条件,各物质的浓度变化如图所示(10~14min时有一物质浓度变化未标出)。
Cl2(g)+CO(g)达到平衡后,改变一个条件,各物质的浓度变化如图所示(10~14min时有一物质浓度变化未标出)。
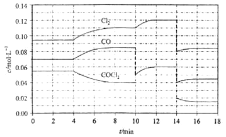
①说明该反应已达到平衡状态的是_____。
a.C(COCl2)=C(Cl2)
b.正(COCl2)=逆(CO)
c.容器内温度保持不变
d.容器内气体密度保持不变
②4~10min平均反应速率v(COCl2)为_____;10min时改变的反应条件是_____。
③0~4min、8~10min和16~18min三个平衡常数依次为K1、K2、K3,比较其大小____;说明理由____。
【答案】![]() 均为分子晶体,COCl2式量较大,范德华力较强,沸点较高 bc 0.0025mol/(L·min) 分离出CO K1<K2=K3 4min时改变条件为升温,吸热反应升温K变大
均为分子晶体,COCl2式量较大,范德华力较强,沸点较高 bc 0.0025mol/(L·min) 分离出CO K1<K2=K3 4min时改变条件为升温,吸热反应升温K变大
【解析】
(1)甲醛的结构式是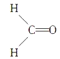 ;COCl2的相对分子质量大于甲醛;
;COCl2的相对分子质量大于甲醛;
(2)①根据平衡标志分析;
②根据![]() 计算4~10min平均反应速率v(COCl2);由图象可知10min时CO的浓度突然减小,后逐渐增大,10min时Cl2的浓度逐渐增大;
计算4~10min平均反应速率v(COCl2);由图象可知10min时CO的浓度突然减小,后逐渐增大,10min时Cl2的浓度逐渐增大;
③根据图象可知,4min时改变的条件是升高温度、14min时,各物质浓度均减小,改变的条件是减小压强。
(1)甲醛的结构式是 ,COCl2结构与甲醛相似,COCl2电子式是
,COCl2结构与甲醛相似,COCl2电子式是![]() ;甲醛、COCl2均为分子晶体,COCl2式量较大,范德华力较强,沸点较高;
;甲醛、COCl2均为分子晶体,COCl2式量较大,范德华力较强,沸点较高;
(2)①a.c(COCl2)=c(Cl2)时,浓度不一定不再改变,反应不一定平衡,故不选a;
b.反应达到平衡状态时,正逆反应速率比等于系数比, 正(COCl2)=逆(CO),一定平衡,故选b;
c.正反应吸热,密闭容器内温度是变量,容器内温度保持不变,反应一定平衡,故选c;
d.气体质量不变、容器体积不变,根据![]() ,密度是恒量,容器内气体密度保持不变,不一定平衡,故不选d;
,密度是恒量,容器内气体密度保持不变,不一定平衡,故不选d;
选bc;
②根据图象,4~10min内COCl2浓度变化是0.055mol/L-0.04mol/L=0.015mol/L, ![]() 0.0025mol/(L·min);由图象可知10min时CO的浓度突然减小,后逐渐增大,10min时Cl2的浓度逐渐增大,可知10min时改变的条件是分离出CO,平衡正向移动,氯气浓度增大;
0.0025mol/(L·min);由图象可知10min时CO的浓度突然减小,后逐渐增大,10min时Cl2的浓度逐渐增大,可知10min时改变的条件是分离出CO,平衡正向移动,氯气浓度增大;
③根据图象可知,4min时改变的条件是升高温度,正反应吸热,升高温度平衡正向移动,平衡常数增大,所以K1<K2,14min时改变的条件是减小压强,平衡常数只与温度有关,所以K2=K3,故K1、K2、K3的大小关系是K1<K2=K3;


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】某温度时,浓度均为1mol·L-1的两种气体X2和Y2,在恒容密闭容器中发生可逆反应生成气体Z,充分反应后X2的浓度为0.4mol·L-1,Y2的浓度为0.8mol·L-1,生成的Z的浓度为0.4mol·L-1,则该反应的化学方程式(Z用X、Y表示)是
A.X2+2Y2![]() 2XY2B.2X2+Y2
2XY2B.2X2+Y2![]() 2X2Y
2X2Y
C.X2+3Y2![]() 2XY3D.3X2+Y2
2XY3D.3X2+Y2![]() 2X3Y
2X3Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通水泥在固化过程中自由水分子减少并产生Ca(OH)2,溶液呈碱性。根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间。此方法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的

A.Cu为正极,Ag2O为负极
B.电池工作时,OH—向正极移动
C.正极的电极反应为:2Cu+2OH——2e—=Cu2O+H2O
D.外电路中每通过2mol电子,正极质量减少16g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2(g)+2ICl(g)→2HCl(g)+I2(g)能量曲线如图。描述正确的是
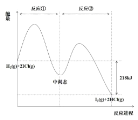
A.反应①为吸热反应
B.若加入催化剂可降低反应热
C.I2(g)+2HCl(g)的能量高于 I2(s)+2HCl(g)的总能量
D.热化学方程式为 H2(g)+2ICl(g)→2HCl(g)+I2(g)-218kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铬和氢气在工业上都有重要的用途。已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4)。铜铬构成原电池如图所示,盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是

A.盐桥的作用是使整个装置构成通路、保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以用饱和KCl琼脂溶液
B.理论上1molCr溶解,盐桥中将有2molCl-进入左池,2molK+进入右池
C.此过程中H+得电子,发生氧化反应
D.电子从铬极通过导线到铜极,又通过盐桥到转移到左烧杯中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,相同条件下,两个容积相同的试管分别装满NO2和NO气体,分别倒置于水槽中,然后通过导管缓慢通入氧气,边通边慢慢摇动试管,直到两个试管内充满液体。假设试管内的溶质不向水槽中扩散,则两个试管内溶液物质的量浓度之比为
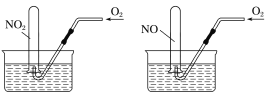
A.1∶1B.5∶7C.7∶5D.4∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校课外活动小组为了探究铜与稀硝酸反应产生的是NO气体,设计了如下实验。实验装置如图所示(已知NO、NO2能与NaOH溶液反应):
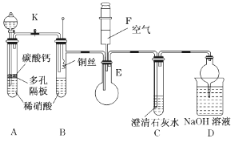
(1)设计装置A的目的是_____________________________________,为达此目的应进行的操作______________________________________________________。
(2)在(1)中的操作后将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是____________________________________________________________;B中反应的离子方程式是_____________________________________________________。
(3)将注射器F中的空气推入E中,E中的气体变为红棕色,该实验的目的是____________。
(4)D装置的作用是_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】线型 PAA( ![]() )具有高吸水性,网状 PAA 在抗压性、吸水性等方面优于线型 PAA。网状 PAA 的制备方法是:将丙烯酸用 NaOH 中和,加入少量交联剂 a,再引发聚合。其部分结构片段 如图所示,列说法错误的是
)具有高吸水性,网状 PAA 在抗压性、吸水性等方面优于线型 PAA。网状 PAA 的制备方法是:将丙烯酸用 NaOH 中和,加入少量交联剂 a,再引发聚合。其部分结构片段 如图所示,列说法错误的是
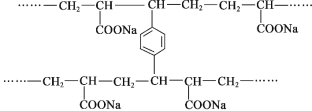
A.线型 PAA 的单体不存在顺反异构现象
B.形成网状结构的过程发生了加聚反应
C.交联剂 a 的结构简式是![]()
D.PAA 的高吸水性与—COONa 有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用98%的浓硫酸(密度为1.84g·cm-3)配制成浓度为0.5mol·L-1的稀硫酸500毫升.
(1)选用的主要仪器除了烧杯、玻璃棒、胶头滴管外还有:_______________(写两个)
(2)请将下列各操作,按正确的序号填在横线上。
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至刻度线
D.稀释浓H2SO4
E.将溶液转入容量瓶
其操作正确的顺序依次为____________________________。
(3)简要回答下列问题:
①98%的浓硫酸的物质的量浓度为_____________mol·L-1
②配制成浓度为0.5mol·L-1的稀硫酸500毫升.所需98%的浓硫酸的体积为____________mL;(保留小数点后一位)
③将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并用玻璃棒不断搅拌的目的是_____;
④定容时必须使溶液凹液面与刻度线相切,若仰视刻度则使浓度___________。(“偏高”、“偏低”、“无影响”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com