
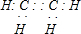 ,C的名称乙醛,
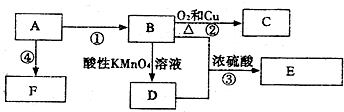
,C的名称乙醛,分析 A是来自石油的重要有机化工原料,A得到的F是一种高聚物,可制成多种包装材料,则A为CH2=CH2,CH2=CH2发生加聚反应生成高聚物F为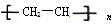 ,B发生催化氧化生成C,被酸性高锰酸钾溶液生成D,则B为醇,C为醛,D为羧酸,故CH2=CH2与水发生加成反应生成B为CH3CH2OH,CH3CH2OH发生催化氧化生成C为CH3CHO,B氧化生成D为CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成E为CH3COOCH2CH3,据此解答.
,B发生催化氧化生成C,被酸性高锰酸钾溶液生成D,则B为醇,C为醛,D为羧酸,故CH2=CH2与水发生加成反应生成B为CH3CH2OH,CH3CH2OH发生催化氧化生成C为CH3CHO,B氧化生成D为CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成E为CH3COOCH2CH3,据此解答.
解答 解:A是来自石油的重要有机化工原料,A得到的F是一种高聚物,可制成多种包装材料,则A为CH2=CH2,CH2=CH2发生加聚反应生成高聚物F为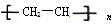 ,B发生催化氧化生成C,被酸性高锰酸钾溶液生成D,则B为醇,C为醛,D为羧酸,故CH2=CH2与水发生加成反应生成B为CH3CH2OH,CH3CH2OH发生催化氧化生成C为CH3CHO,B氧化生成D为CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成E为CH3COOCH2CH3,
,B发生催化氧化生成C,被酸性高锰酸钾溶液生成D,则B为醇,C为醛,D为羧酸,故CH2=CH2与水发生加成反应生成B为CH3CH2OH,CH3CH2OH发生催化氧化生成C为CH3CHO,B氧化生成D为CH3COOH,CH3COOH与CH3CH2OH发生酯化反应生成E为CH3COOCH2CH3,
(1)由上述分析可知,A是乙烯,电子式为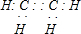 ,C为CH3CHO,其名称为乙醛,
,C为CH3CHO,其名称为乙醛,
故答案为: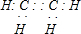 ,乙醛;
,乙醛;
(2)D是乙酸,分子含有羧基,取少量物质与试管中滴加石蕊试液,若溶液变为红色,说明该物质含有-COOH
故答案为:羧基,取少量物质与试管中滴加石蕊试液,若溶液变为红色,说明该物质含有-COOH;
(3)反应③是乙醇与乙酸发生酯化反应生成乙酸乙酯,反应方程式为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,
故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,酯化反应.
点评 考查有机物的推断,涉及烯、醇、羧酸等性质与转化,难度不大,是对有机知识的总运用,有机推断是高考不变的一个题型,每年高考中必考,经常给出某反应信息要求学生加以应用,能较好的考查考生的阅读、自学能力和思维能力,是热点题型.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:选择题
| A. | +92 | B. | -345.3 | C. | -92 | D. | +345.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
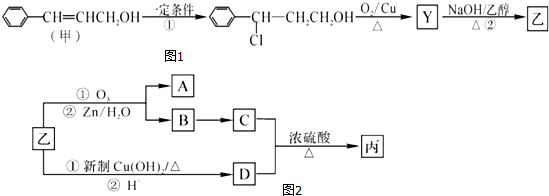
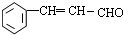 .
.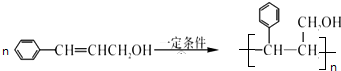 ;
;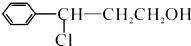 →Y:
→Y: .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
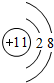 ,DA4的结构式为
,DA4的结构式为 ;
; ,D元素在周期表中的位置第二周期IVA族;
,D元素在周期表中的位置第二周期IVA族;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
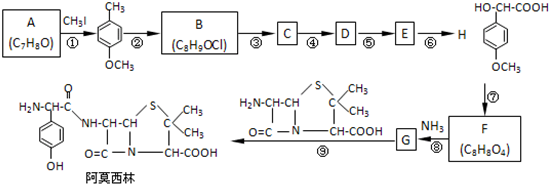
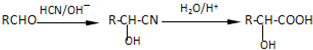
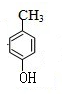 ;
;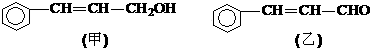
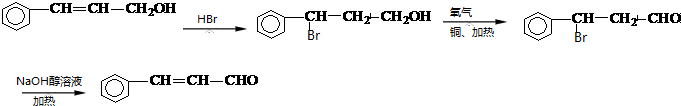
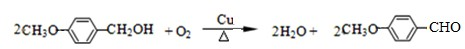 .
.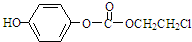 ,该物质在NaOH水溶液中加热反应时的化学方程式为
,该物质在NaOH水溶液中加热反应时的化学方程式为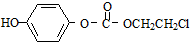 +5NaOH$→_{△}^{H_{2}O}$
+5NaOH$→_{△}^{H_{2}O}$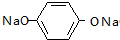 +HOCH2CH2OH+Na2CO3+NaCl+2H2O.
+HOCH2CH2OH+Na2CO3+NaCl+2H2O.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作及现象 | 结论 | |
| A | 向AgCl悬浊液中加入NaI溶液时出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| B | 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色 | 溶液中一定含有Fe2+ |
| C | 向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈橙红色 | Br-还原性强于Cl- |
| D | 向溶液X的稀溶液中滴加NaOH稀溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 溶液X中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com