
| A、标准状况下,22.4L一氯甲烷和二氯甲烷的混合物所含氯原子数介于NA至2NA之间 |
| B、1mol的Cu在一定条件下与足量硫粉反应,转移电子数目为2NA |
| C、3.65g液态氯化氢中分子的数目为0.1NA |
| D、常温下5.6g铁投入到足量的浓硝酸中,转移的电子数为0.3NA |


科目:高中化学 来源: 题型:
| A、甲烷、苯、乙醇和乙酸在一定条件下都能发生取代反应 |
| B、乙烯使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色的反应类型不同 |
| C、塑料、合成橡胶、合成纤维都属于合成有机高分子材料 |
| D、化学式均为(C6H10O5)n的淀粉和纤维素互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:W>Z>Y>X |
| B、Z元素在周期表的位置为第三周期第ⅡA族 |
| C、丁的稳定性小于甲烷 |
| D、丙的水溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol Na2O2与足量CO2充分反应转移的电子数为2NA |
| B、常温下,pH=1的醋酸溶液中,醋酸分子的数目一定大于0.1NA |
| C、向FeI2溶液中通入适量氯气,当有1molFe2+被氧化时,总共转移电子的数目为NA |
| D、t℃时,1L pH=6的纯水中,含1×10-6 NA个OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(NO3)3加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
| B、硫酸镁溶液与氢氧化钡溶液混合:SO42-+Ba2+═BaSO4↓ |
| C、等体积等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O |
| D、Cu溶于足量稀硝酸:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
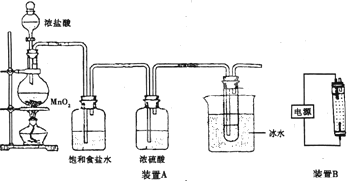
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、太阳能、地热能、核能等均属于新能源 |
| B、“低碳”是指采用含碳量低的烃类化合物作燃料 |
C、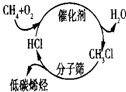 甲烷经一氯甲烷转化成低碳烯烃的途径体现了“节能减排”思想 |
| D、减少化石能源的使用能减少CO2的排放量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6.0g/mol |
| B、5.0g/mol |
| C、10.0g/mol |
| D、4.0g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
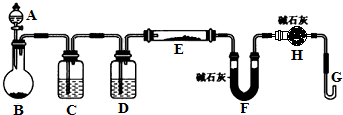 某课外小组利用H2还原黄色的WO3粉末测定W的相对原子质量,如图是测定装置的示意图.A中的试剂是盐酸.请回答下列问题:
某课外小组利用H2还原黄色的WO3粉末测定W的相对原子质量,如图是测定装置的示意图.A中的试剂是盐酸.请回答下列问题:| ①空E管的质量a; | ④反应前F管及内盛物的总质量d; |
| ②E管和WO3的总质量b; | ⑤反应后F管及内盛物的总质量e |
| ③反应后E管和W粉的总质量c(冷却后); |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com