
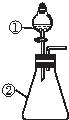
 用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )| 选項 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 氢氧化钠稀溶液 | 硫酸铝铵溶液 | 立即产生白色沉淀 |
| B | 氢氧化钠浓溶液 | 用砂纸打磨过的镁条 | 立即产生大量无色气体 |
| C | 浓硫酸 | 铜粉 | 立即产生刺激性气味气体 |
| D | 盐酸 | 较浓的硝酸亚铁溶液 | 无明显现象 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.先发生铝离子与NaOH的反应,再发生铵根离子与NaOH的反应,最后发生氢氧化铝与NaOH的反应;
B.Mg与NaOH溶液不反应;
C.Cu与浓硫酸反应需要加热;
D.酸性条件亚铁离子、硝酸根离子发生氧化还原反应.
解答 解:A.先发生铝离子与NaOH的反应,再发生铵根离子与NaOH的反应,最后发生氢氧化铝与NaOH的反应,则将①中溶液滴入②中,立即产生白色沉淀,故A选;
B.Mg与NaOH溶液不反应,则将①中溶液滴入②中,无现象,故B不选;
C.Cu与浓硫酸反应需要加热,则将①中溶液滴入②中,无现象,故C不选;
D.酸性条件亚铁离子、硝酸根离子发生氧化还原反应,则将①中溶液滴入②中,溶液由浅绿色变为黄色,故D不选;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应和现象为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:推断题


 、
、 、
、 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面,N2、H2中化学键断裂.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面,N2、H2中化学键断裂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5molAl与足量盐酸反应转移电子数为1NA | |
| B. | 标准状况下22.4LH2中含中子数为2 NA | |
| C. | 0.5mol CH4所含电子数为5 NA | |
| D. | 1L1 mol/L醋酸溶液中离子总数为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+ Na+ MnO4- SO42- | B. | Na+ CO32- Al3+ Cl- | ||
| C. | K+ Na+ Cl- SO42- | D. | K+ Cl- Ba2+ HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解食盐水若产生2g氢气,则转移的电子数目为NA | |
| B. | 电解精炼铜时转移0.1 NA个电子,则阳极溶解3.2g铜 | |
| C. | VL amol/L FeCl3 溶液中,若Fe3+数目为NA,则Cl-的数目大于3NA | |
| D. | 100mL 1mol/L的醋酸溶液中,CH3COO-离子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com