
 Fe(s)+CO2(g)
Fe(s)+CO2(g) | A£®ČōÉś³É1 mol Fe£¬ŌņĪüŹÕµÄČČĮæŠ”ÓŚa kJ |
| B£®ČōÉżøßĪĀ¶Č£¬Õż·“Ó¦ĖŁĀŹ¼Óæģ£¬Äę·“Ó¦ĖŁĀŹ¼õĀż£¬Ōņ»ÆŃ§Ę½ŗāÕżĻņŅĘ¶Æ |
| C£®ČōČŻĘ÷ÄŚŃ¹Ēæ²»Ėꏱ¼ä±ä»Æ£¬ŌņæÉŅŌÅŠ¶ĻøĆ·“Ó¦ŅŃ“ļµ½»ÆŃ§Ę½ŗāדĢ¬ |
| D£®“ļµ½»ÆŃ§Ę½ŗāדĢ¬Ź±£¬Čōc(CO)="0.100" mol/L£¬Ōņc(CO2)="0.0263" mol/L |
 Fe(s)+CO2(g) ”÷H="a" kJ/mol£Øa >0£©£¬¼“øĆ·“Ó¦ĪŖĪüČČ·“Ó¦£¬ĖłŅŌČōÉś³É1 mol Fe£¬ŌņĪüŹÕµÄČČĮæĪŖa kJ£¬¹ŹA“ķĪó£»ČōÉżøßĪĀ¶Č£¬Õż·“Ó¦ĖŁĀŹŗĶÄę·“Ó¦ĖŁĀŹ¶¼Ōö“ó£¬ÖŖŹ¶Õż·“Ó¦ĖŁĀŹŌö“óµÄ³Ģ¶Č“óÓŚÄę·“Ó¦ĖŁĀŹ£¬·“Ó¦ĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬ĖłŅŌB“ķĪó£»øĆ·“Ó¦“ÓæŖŹ¼·“Ó¦Ź±Ęš£¬ČŻĘ÷µÄŃ¹Ēæ¾ĶŅ»Ö±±£³Ö²»±ä£¬ĖłŅŌČŻĘ÷ÄŚŃ¹Ēæ²»Ėꏱ¼ä±ä»Æ£¬²»ÄÜÓĆĄ“ÅŠ¶Ļ·“Ó¦ŅŃ¾“ļµ½Ę½ŗāדĢ¬£¬¹ŹC“ķĪó£»ŌŚøĆĪĀ¶ČĻĀK = 0.263£¬ĖłŅŌ
Fe(s)+CO2(g) ”÷H="a" kJ/mol£Øa >0£©£¬¼“øĆ·“Ó¦ĪŖĪüČČ·“Ó¦£¬ĖłŅŌČōÉś³É1 mol Fe£¬ŌņĪüŹÕµÄČČĮæĪŖa kJ£¬¹ŹA“ķĪó£»ČōÉżøßĪĀ¶Č£¬Õż·“Ó¦ĖŁĀŹŗĶÄę·“Ó¦ĖŁĀŹ¶¼Ōö“ó£¬ÖŖŹ¶Õż·“Ó¦ĖŁĀŹŌö“óµÄ³Ģ¶Č“óÓŚÄę·“Ó¦ĖŁĀŹ£¬·“Ó¦ĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬ĖłŅŌB“ķĪó£»øĆ·“Ó¦“ÓæŖŹ¼·“Ó¦Ź±Ęš£¬ČŻĘ÷µÄŃ¹Ēæ¾ĶŅ»Ö±±£³Ö²»±ä£¬ĖłŅŌČŻĘ÷ÄŚŃ¹Ēæ²»Ėꏱ¼ä±ä»Æ£¬²»ÄÜÓĆĄ“ÅŠ¶Ļ·“Ó¦ŅŃ¾“ļµ½Ę½ŗāדĢ¬£¬¹ŹC“ķĪó£»ŌŚøĆĪĀ¶ČĻĀK = 0.263£¬ĖłŅŌ


| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
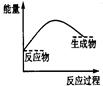
 2 CO2 (g) £«S (g)””¦¤H=" +8.0" kJ/molµÄ·“Ó¦Ą“¼õÉŁĪŪČ¾£¬Ź¹ÓĆŠĀŠĶ“߻ƼĮ¼Óæģ·“Ó¦”£ĻĀĮŠÓŠ¹ŲøĆ·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»ÆŹ¾ŅāĶ¼ÕżČ·µÄŹĒ
2 CO2 (g) £«S (g)””¦¤H=" +8.0" kJ/molµÄ·“Ó¦Ą“¼õÉŁĪŪČ¾£¬Ź¹ÓĆŠĀŠĶ“߻ƼĮ¼Óæģ·“Ó¦”£ĻĀĮŠÓŠ¹ŲøĆ·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»ÆŹ¾ŅāĶ¼ÕżČ·µÄŹĒ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā

 O2(g)= CO2(g)+2H2(g)”””÷H2
O2(g)= CO2(g)+2H2(g)”””÷H2 O2(g)=H2O(g)”””””÷H ="-241.8" kJ”¤mol-1
O2(g)=H2O(g)”””””÷H ="-241.8" kJ”¤mol-1²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā



²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 ӣ
”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 CH3OH(g)µÄÄÜĮæĒéæöČēĶ¼ĖłŹ¾£¬ĒśĻßIŗĶĒśĻߢņ·Ö±š±ķŹ¾²»Ź¹ÓĆ“ß»Æ¼ĮŗĶŹ¹ÓĆ“ß»Æ¼ĮµÄĮ½ÖÖĒéæö”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
CH3OH(g)µÄÄÜĮæĒéæöČēĶ¼ĖłŹ¾£¬ĒśĻßIŗĶĒśĻߢņ·Ö±š±ķŹ¾²»Ź¹ÓĆ“ß»Æ¼ĮŗĶŹ¹ÓĆ“ß»Æ¼ĮµÄĮ½ÖÖĒéæö”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
| A£®øĆ·“ Ó¦µÄ¦¤H£½+91kJ”¤mol-1 |
| B£®¼ÓČė“߻ƼĮ£¬øĆ·“Ó¦µÄ¦¤H±äŠ” |
| C£®·“Ó¦ĪļµÄ×ÜÄÜĮæ“óÓŚÉś³ÉĪļµÄ×ÜÄÜĮæ |
| D£®Čē¹ūøĆ·“Ӧɜ³ÉŅŗĢ¬CH3OH£¬Ōņ¦¤HŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®CH4+2O2 CO2+2H2O CO2+2H2O |
B£®CaCO3 CaO+CO2”ü CaO+CO2”ü |
C£®2H2O  2H2”ü + O2”ü 2H2”ü + O2”ü |
D£®Pb+PbO2+2H2SO4  2PbSO4+2H2O 2PbSO4+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 CO2(g) ¦¤H£½£437.3 kJ?mol£1
CO2(g) ¦¤H£½£437.3 kJ?mol£1 O2(g)
O2(g)  H2O(g) ¦¤H£½£285.8 kJ?mol£1
H2O(g) ¦¤H£½£285.8 kJ?mol£1 O2(g)
O2(g)  CO2(g) ¦¤H£½£283.0 kJ?mol£1
CO2(g) ¦¤H£½£283.0 kJ?mol£1²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 £Ø1£©H2£Øg£©+ O2£Øg£©===H2O£Øg£© ”÷H1=a kJ”¤mol-1
£Ø1£©H2£Øg£©+ O2£Øg£©===H2O£Øg£© ”÷H1=a kJ”¤mol-1 £Ø3£©H2£Øg£©+ O2£Øg£©===H2O£Øl£© ”÷H3=c kJ”¤mol-1
£Ø3£©H2£Øg£©+ O2£Øg£©===H2O£Øl£© ”÷H3=c kJ”¤mol-1| A£®a<c<0 | B£®b>d>0 | C£®2a=b<0 | D£®2c=d>0 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com